Дифиллоботриоз - Википедия - Diphyllobothriasis
| Дифиллоботриоз | |
|---|---|
| Специальность | Инфекционное заболевание |
Дифиллоботриоз инфекция вызвана ленточные черви рода Дифиллоботрий (обычно D. latum и D. nihonkaiense).
Дифиллоботриоз чаще всего встречается в регионах, где регулярно употребляется сырая рыба; Те, кто ест сырую рыбу, подвергаются риску заражения. Инфекция часто протекает бессимптомно и обычно проявляется лишь легкими симптомами, которые могут включать жалобы на желудочно-кишечный тракт, потерю веса и утомляемость. В редких случаях может возникнуть дефицит витамина B12 (который может привести к анемии) и желудочно-кишечные непроходимости. Без лечения инфекция может продолжаться долго. Дифиллоботриоз обычно диагностируется путем поиска яиц или сегментов ленточного червя в стуле. Лечение противопаразитарными препаратами простое, эффективное и безопасное.
Признаки и симптомы
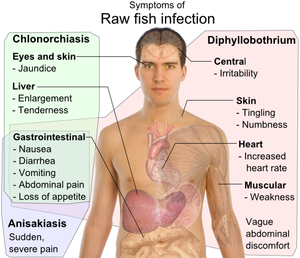
Большинство инфекций (~ 80%[6]) протекают бессимптомно.[6][7][8] Инфекции могут длиться долго,[7] сохраняющийся много лет[6] или десятилетия (до 25 лет)[7] если не лечить.
Симптомы (если они есть) обычно легкие.[9][8] Проявления могут включать боль и дискомфорт в животе, диарею, рвоту, запор, потерю веса и утомляемость.[9]
Сообщалось / описывалось о дополнительных симптомах, в том числе: диспепсия, вздутие живота (обычно в качестве жалобы), головная боль, миалгия и головокружение.[8]
Осложнения
Хотя инфекция обычно протекает в легкой форме, могут возникнуть осложнения. Осложнения связаны с бременем паразитов и обычно связаны с дефицитом витамина B12 и сопутствующими заболеваниями.[8]
Дефицит витамина B12 и анемия
Дефицит витамина B12 с последующим мегалобластная анемия (который неотличим от злокачественная анемия ) может возникать в некоторых случаях заболевания.[10] Анемия, в свою очередь, может привести к подострой комбинированной дегенерации спинного мозга и снижению когнитивных функций.[8]
D. latum конкурирует с хозяином за всасывание витамина B12,[11] поглощает около 80% пищевого рациона и в 40% случаев вызывает дефицит и мегалобластную анемию.[12] Поглощение витамина B12 обеспечивается положением паразита, который обычно оседает в тощей кишке.[13] Согласно исследованиям, дефицит витамина B12, наоборот, редко встречается у людей. D. pacificum инфекционное заболевание.[11]
Непроходимость желудочно-кишечного тракта
Редко массивные инфекции могут привести к кишечной непроходимости. Миграция проглоттидов может вызвать холецистит или же холангит.[7]
Причина
Дифиллоботриоз вызывается инфекцией несколькими видами рода Diphyllobothrium.[7]
Передача инфекции
Люди являются одним из основных хозяев ленточных червей Diphyllobothrium наряду с другими хищниками; Рыбоядные млекопитающие (включая псовых, кошачьих и медведей), морские млекопитающие (дельфины, морские свиньи и киты) и (некоторые) птицы (например, чайки) также могут служить в качестве окончательных хозяев.[7]
Окончательные хозяева выделяют яйца с фекалиями; затем яйца созревают примерно через 18–20 дней при благоприятных условиях. Ракообразные служат первыми промежуточными хозяевами, и развиваются личинки Diphyllobothrium. Личинки выпускаются, когда ракообразных поедают хищники, которые служат вторыми промежуточными хозяевами (в основном это мелкая рыба). Личинки перемещаются в более глубокие ткани второго промежуточного хозяина. Вторые промежуточные хозяева не служат важным источником заражения людей, поскольку их не употребляют в сыром виде. Потребление зараженных вторых промежуточных хозяев более крупными хищными рыбами, которые служат паратеническими хозяевами; паразиты вслед за этим мигрируют в мускулатуру в ожидании потребления окончательными хозяевами, у которых взрослые ленточные черви затем, наконец, разовьются в тонком кишечнике, выделяя до миллиона незрелых яиц в день на каждого паразита. Хозяева начинают выделять яйца через 5–6 недель после заражения.[7]
Патофизиология
Ленточные черви развиваются в тонком кишечнике. Взрослые особи прикрепляются к слизистой оболочке кишечника. Взрослые ленточные черви могут достигать более 10 м в длину и могут составлять более 3000 проглоттидов.[7] которые содержат наборы мужских и женских репродуктивных органов, обеспечивающие высокую плодовитость.[8] Яйца появляются с фекалиями через 5–6 недель после заражения.[7]
D. latum ленточные черви самые длинные и обычно достигают длины 4-15 м, но могут вырасти до 25 м в кишечнике человека. Скорость роста может превышать 22 см / сутки. У ленточных червей D. latum имеется передний конец (сколекс), на дорсальной и вентральной поверхностях которого имеются прикрепительные борозды.[8]
Взаимодействие хозяина-паразита
Постулируется, что дифиллоботриоз вызывает изменения концентраций нейромодуляторов в ткани и сыворотке хозяина. Было показано, что инфекция D. latum вызывает локальные изменения в организме хозяина, что приводит к изменению функции желудочно-кишечного тракта (включая подвижность) посредством нейроэндокринной модуляции.[8]
Дифиллоботриоз вызывает дегрануляцию тучных клеток и эозинофилов, что приводит к высвобождению провоспалительных цитокинов.[8]
Диагностика
Заподозрить инфекцию можно на основании рода занятий, хобби, привычек в еде и истории поездок пациента.[8] Во время диагностических процедур применяются стандартные меры безопасности. Яйца не заразны напрямую для человека (в отличие от некоторых других видов ленточных червей).[7]
Микроскопия
Диагноз обычно ставится путем выявления сегментов проглоттид или характерных яиц в фекалиях..[14] Яиц обычно много, и их можно продемонстрировать без техники концентрации. Морфологическое сравнение с другими кишечными паразитами может использоваться как дополнительный диагностический подход.[нужна цитата ]
Эти простые диагностические методы позволяют определить природу инфекции на уровне рода, что обычно бывает достаточно в клинических условиях.[6] Хотя трудно идентифицировать яйца или проглоттиды на уровне вида, различие не имеет большого клинического значения, потому что, как и большинство взрослых ленточных червей в кишечнике, все представители рода реагируют на одно и то же лечение.[нужна цитата ] Лечение может исказить морфологические характеристики тканей изгнанного патогена и затруднить последующие попытки морфологической диагностики.[7]
Генетическая идентификация
Когда необходимо определить точный вид (например, в эпидемиологических исследованиях), можно эффективно использовать полиморфизмы длины рестрикционных фрагментов. ПЦР может выполняться на образцах очищенных яиц или на образцах нативных фекалий после обработка ультразвуком яиц, чтобы высвободить их содержимое.[6] Молекулярная идентификация в настоящее время обычно используется только в исследованиях.[7]
Рентгенография
Потенциальным средством диагностики и лечения является контрастное вещество. гастрографин который при введении в двенадцатиперстную кишку позволяет визуализировать паразита, а также, как было показано, вызывает отслоение и передачу всего паразита.[15]
Профилактика
Следует избегать употребления в пищу сырой пресноводной рыбы. Правильное приготовление или замораживание пресноводной рыбы уничтожит инцистированные личинки солитера. Тщательно приготовленную, соленую или замороженную рыбу при -10 ° C в течение 24–48 часов также можно употреблять без риска D. latum инфекционное заболевание. Информационные кампании в области общественного здравоохранения могут использоваться для информирования общественности о рисках употребления неправильно приготовленной рыбы..[нужна цитата ]
Поскольку человеческие фекалии являются важным механизмом распространения яиц, правильная утилизация сточных вод может снизить риск заражения рыб (и, следовательно, людей).[нужна цитата ] Предотвращение загрязнения воды может быть достигнуто как путем повышения осведомленности общественности об опасностях дефекации в водоемах для отдыха, так и путем принятия основных санитарных мер, а также скрининга и успешного лечения людей, инфицированных паразитом.[6]
Уход
После постановки диагноза лечение простое и эффективное.[16][17][18]
Празиквантел
Стандартное лечение дифиллоботриоза (как и многих других инфекций ленточных червей) - это однократная доза празиквантел, 5–10 мг / кг перорально однократно для взрослых и детей.[16][17][18] Празиквантел не одобрен FDA для этого показания.[16] Празиквантел имеет несколько побочных эффектов, многие из которых похожи на симптомы дифиллоботриоза.[6]
Никлозамид
Альтернативное лечение никлозамид, 2 г перорально однократно для взрослых или 50 мг / кг (макс. 2 г) для детей.[16][17][18] Никлозамид недоступен для использования людьми или даже животными в Соединенных Штатах.[16] Побочные эффекты никлозамида возникают очень редко из-за того, что лекарство не всасывается в желудочно-кишечном тракте.[6]
Другой
Как сообщается, альбендазол также может быть эффективным.[19][20]
Гастрографин потенциально может использоваться как диагностическое, так и терапевтическое; при введении в двенадцатиперстную кишку он позволяет визуализировать паразита, а также, как было показано, вызывает отслоение и прохождение всего червя.[21][22]
Эпидемиология
Люди с высоким риском заражения традиционно - это те, кто регулярно потребляет сырую рыбу.[6] Хотя заболеть могут люди любого пола и возраста, большинство выявленных случаев произошло у мужчин среднего возраста.[8]
Географическое распределение
Дифиллоботриоз возникает в районах, где озера и реки сосуществуют с потреблением человеком сырой или недостаточно приготовленной пресноводной рыбы.[23] Такие области встречаются в Европа, новые независимые государства бывшего Советский союз, Северная Америка, Азия, Уганда, Перу (потому что севиче ), и Чили.[23] Многие региональные кухни включают сырые или недоваренные блюда, в том числе суши и сашими в японской кухне, carpaccio di persico по-итальянски, tartare maison у франкоговорящих народов, севиче в латиноамериканской кухне и маринованную сельдь в Скандинавии. С эмиграцией и глобализацией практика употребления в пищу сырой рыбы в этих и других блюдах принесла дифиллоботриоз в новые части мира и создала новые эндемические очаги болезней.[6]
Инфекции в Европе и Северной Америке традиционно ассоциировались с еврейскими женщинами из-за практики дегустации кусочков сырой рыбы во время приготовления Gefilte Fish блюдо,[24] а также происходило у скандинавских женщин по той же причине. Таким образом, дифиллоботриоз также называли «болезнью еврейской домохозяйки» или «болезнью скандинавской домохозяйки».[25]
Япония
Дифиллоботриоз nihonkaiense когда-то был эндемиком прибрежных провинций центральных и северных регионов. Япония, где процветал промысел лосося.[23] В последние десятилетия регионы с эндемическим nihonkaiense дифиллоботриоза исчезли из Японии, хотя случаи заболевания продолжают регистрироваться среди городских жителей, потребляющих суши или же сашими.[23] В Киото, по оценкам, среднегодовая заболеваемость за последние 20 лет составляла 0,32 случая на 100 000, а в 2008 г. - 1,0 случай на 100 000 населения, что позволяет предположить, что D. nihonkaiense инфекция так же распространена в Японии, как и D. latum есть в некоторых европейских странах.[23]
Соединенные Штаты
Заболевание в США встречается редко.[нужна цитата ]
История
Рыбный цепень имеет долгую задокументированную историю заражения людей, которые регулярно потребляют рыбу, и особенно тех, чьи обычаи включают потребление сырой или недоваренной рыбы. В 1970-е годы большинство известных случаев дифиллоботриоза приходилось на Европу (5 миллионов случаев) и Азию (4 миллиона случаев), меньшее количество случаев приходилось на Северную Америку и Южную Америку, а достоверных данных о случаях из Африки или Австралии не было.[6] Несмотря на относительно небольшое количество случаев заболевания, наблюдаемых сегодня в Южной Америке, некоторые из самых ранних археологических свидетельств дифиллоботриоза происходят из мест в Южной Америке. Доказательство того Diphyllobothrium spp. был обнаружен в человеческих останках возрастом от 4000 до 10000 лет на западном побережье Южной Америки.[26] Нет четкого момента времени, когда Дифиллоботрий латум и родственные виды были «открыты» у людей, но очевидно, что дифиллоботриоз был эндемическим заболеванием в человеческих популяциях в течение очень долгого времени. Из-за меняющихся привычек питания во многих частях мира, автохтонных или приобретенных на местном уровне, недавно были зарегистрированы случаи дифиллоботриоза в ранее неэндемичных регионах, таких как Бразилия.[27] Таким образом, дифиллоботриоз представляет собой возникающее инфекционное заболевание в определенных частях мира, где внедряются культурные традиции, связанные с употреблением в пищу сырой или недоваренной рыбы.[нужна цитата ]
Рекомендации
- ^ WaiSays: о потреблении сырой рыбы Проверено 14 апреля, 2009 г.
- ^ При хлонорхозе: Агентство общественного здравоохранения Канады> Clonorchis sinensis - Паспорта безопасности материалов (MSDS) Проверено 14 апреля, 2009 г.
- ^ Для анисакиоза: Неправильный диагноз: симптомы анизакиоза Проверено 14 апреля, 2009 г.
- ^ Для дифиллоботрия: MedlinePlus> Дифиллоботриоз Обновлено: Арнольд Л. Лентнек, доктор медицины. Проверено 14 апреля, 2009 г.
- ^ При симптомах дифиллоботрия из-за дефицита витамина B12 Медицинский центр Университета Мэриленда> Мегалобластическая (пагубная) анемия Проверено 14 апреля, 2009 г.
- ^ а б c d е ж грамм час я j k Шольц, Т; и другие. (2009). «Обновленная информация о человеческом ленточном черве (род Diphyllobothrium), включая клиническую значимость». Обзоры клинической микробиологии. 22 (1): 146–160. Дои:10.1128 / CMR.00033-08. ЧВК 2620636. PMID 19136438.
- ^ а б c d е ж грамм час я j k л «CDC - DPDx - Дифиллоботриоз». www.cdc.gov. 2019-05-14. Получено 2020-07-29.
- ^ а б c d е ж грамм час я j k Дуррани, Мухаммад I .; Басит, Хаджира; Блазар, Эрик (2020), «Diphyllobothrium Latum (Дифиллоботриоз)», StatPearls, Остров сокровищ (Флорида): StatPearls Publishing, PMID 31082015, получено 2020-07-29
- ^ а б «DPDx - Дифиллоботриоз». Dpd.cdc.gov. Архивировано из оригинал на 2007-11-16. Получено 2012-12-30.
- ^ Джон, Дэвид Т. и Петри, Уильям А. (2006)
- ^ а б Хименес, Хуан А .; Родригес, Сильвия; Гамбоа, Рикардо; Родригес, Лурдес; Гарсия, Гектор Х. (07.11.2012). «Инфекция Diphyllobothrium pacificum редко ассоциируется с мегалобластной анемией». Американский журнал тропической медицины и гигиены. 87 (5): 897–901. Дои:10.4269 / ajtmh.2012.12-0067. ISSN 0002-9637. ЧВК 3516266. PMID 22987655.
- ^ Шарма, Коника; Wijarnpreecha, Карн; Меррелл, Нэнси (июнь 2018 г.). «Diphyllobothrium latum, имитирующий подострый аппендицит». Гастроэнтерологические исследования. 11 (3): 235–237. Дои:10.14740 / gr989w. ISSN 1918-2805. ЧВК 5997473. PMID 29915635.
- ^ Бриани, Кьяра; Далла Торре, Кьяра; Читтон, Валентина; Манара, Ренцо; Помпанин, Сара; Бинотто, Джанни; Адами, Фаусто (2013-11-15). «Дефицит кобаламина: клиническая картина и рентгенологические данные». Питательные вещества. 5 (11): 4521–4539. Дои:10.3390 / nu5114521. ISSN 2072-6643. ЧВК 3847746. PMID 24248213.
- ^ http://web.gideononline.com/web/epidemiology/
- ^ Ко, С. «Наблюдение за процессом дегельминтизации кишечника. Дифиллоботрий латум паразитизм при введении гастрографина в тощую кишку через двухбаллонный энтероскоп ». (2008) из письма в редакцию; Американский журнал гастроэнтерологии, 103; 2149-2150.
- ^ а б c d е «Дифиллоботрий - ресурсы для специалистов в области здравоохранения». Паразиты - CDC. 2012-01-10. Получено 2015-09-05.
- ^ а б c «Гельминты: Цестодная (ленточная) инфекция: Никлозамид». Типовая информация о назначении ВОЗ: Лекарства, используемые при паразитарных заболеваниях - Второе издание. ВОЗ. 1995. Получено 2015-09-05.
- ^ а б c «Гельминты: цестодная (ленточная) инфекция: празиквантел». Типовая информация о назначении ВОЗ: Лекарства, используемые при паразитарных заболеваниях - Второе издание. ВОЗ. 1995. Получено 2015-09-05.
- ^ Молодожникова Н.М., Володин А.В., Бакулина Н.Г. (ноябрь – декабрь 1991 г.). «[Действие альбендазола на ленточного червя]». Медицинская паразитология и паразитарные болезни (на русском). Москва (6): 46–50. PMID 1818249.
- ^ Джексон И., Пасторе Р., Судре П., Лутан Л., Шаппюи Ф (декабрь 2007 г.). «Вспышка Diphyllobothrium latum из маринованного сырого окуня, Женевское озеро, Швейцария». Возникающие инфекционные заболевания. 13 (12): 1957–1958. Дои:10.3201 / eid1312.071034. ЧВК 2876774. PMID 18258060.
- ^ Ваки К., Ои Х, Такахаши С. и др. (1986). "Успешное лечение Дифиллоботрий латум и Taenia saginata инфицирование интрадуоденальным введением «Гастрографина» ». Ланцет. 2 (8516): 1124–6. Дои:10.1016 / S0140-6736 (86) 90532-5. PMID 2877274.
- ^ Ко, С. Б. (2008). «Наблюдение за процессом дегельминтизации кишечного паразитизма Diphyllobothrium latum путем введения гастрографина в тощую кишку через двухбаллонный энтероскоп». Американский журнал гастроэнтерологии. 103 (8): 2149–50. PMID 18796119.
- ^ а б c d е Аризоно, Наоки; Ямада, Минору; Накамура-Учияма, Фукуми; Охниши, Кендзи (июнь 2009 г.). «Дифиллоботриоз, связанный с употреблением в пищу сырого тихоокеанского лосося». Возникающие инфекционные заболевания. 15 (6): 866–870. Дои:10.3201 / eid1506.090132. ЧВК 2727320. PMID 19523283.
- ^ Кабельо, Фелипе С. (январь 2007 г.). «Аквакультура лосося и передача ленточного червя рыб». Возникающие инфекционные заболевания. 13 (1): 169–171. Дои:10.3201 / eid1301.060875. ISSN 1080-6040. ЧВК 2725803. PMID 17370539.
- ^ Уркин, Яков; Наймер, Соди (февраль 2015 г.). «Еврейские праздники и связанные с ними медицинские риски». Журнал общественного здоровья. 40 (1): 82–87. Дои:10.1007 / s10900-014-9899-6. ISSN 0094-5145.
- ^ Райнхард, KJ (1992). «Паразитология как инструмент интерпретации в археологии». Американская древность. 57 (2): 231–245. Дои:10.2307/280729. JSTOR 280729.
- ^ Ллагуно, Маурисио М. и др. «Дифиллоботрий латум инфекция в неэндемичной стране: отчет о болезни ». (2008) Revista da Sociedade Brasileira de Medicina Tropical, 41 (3), 301-303.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
- «Дифиллоботриоз». CDC - DPDx - Лабораторная идентификация паразитарных заболеваний, вызывающих озабоченность общественного здравоохранения. 2013-11-29. Получено 2015-09-05.
