Окисление вторичных спиртов до кетонов - Oxidation of secondary alcohols to ketones
В окисление вторичных спиртов до кетонов это важный окисление реакция в органическая химия.
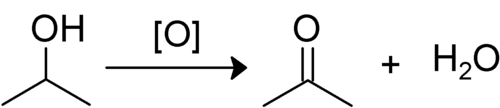
Где вторичный спирт окисляется, превращается в кетон. Водород из гидроксил группа теряется вместе с водородом, связанным со вторым углеродом. Оставшийся кислород затем образует двойные связи с углеродом. Остается кетон, так как R1–COR2. Кетоны обычно не могут окисляться дальше, потому что это повлечет за собой разрыв связи C – C, что требует слишком много энергии.[1]
Реакция может происходить с использованием различных окислителей.
Дихромат калия
Вторичный спирт можно окислить до кетона с помощью подкисленного дихромат калия и отопление под рефлюкс Оранжево-красный дихромат-ион Cr2О72−, сводится к зеленому Cr3+ ион. Эта реакция когда-то использовалась в тесте на алкоголь.
PCC (хлорхромат пиридиния)
PCC при использовании в органическом растворителе может быть использован для окисления вторичного спирта до кетона. Его преимущество заключается в том, что это происходит избирательно, без тенденции к чрезмерному окислению.
Окисление Десса-Мартина
В Десс – Мартин периодинан является мягким окислителем для превращения спиртов в альдегиды или кетоны.[2]
Реакцию проводят в стандартных условиях, при комнатной температуре, чаще всего в дихлорметан. Для завершения реакции требуется от получаса до двух часов. Затем продукт отделяется от отработанного периодинан.[3]
Окисление Сверна
Окисление Сверна окисляет вторичные спирты в кетоны с использованием оксалилхлорид и диметилсульфоксид. Также требуется органическая основа, такая как триэтиламин.
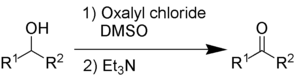
Побочные продукты диметилсульфид (Мне2S), монооксид углерода (CO), углекислый газ (CO2) и - если в качестве основания используется триэтиламин - хлорид триэтиламмония (C6ЧАС15NHCl). Диметилсульфид и окись углерода являются очень токсичными соединениями с неприятным запахом, поэтому реакцию и обработку необходимо проводить в вытяжной шкаф или на открытом воздухе.
Окисление Оппенауэра
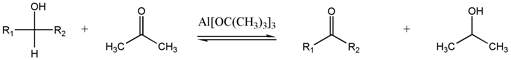
Фетизон окисление
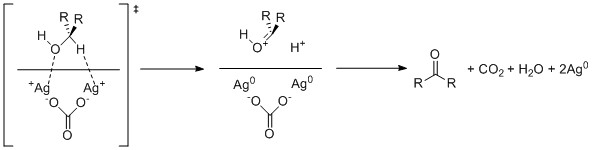
Карбонат серебра на целите окисляет спирты за счет одноэлектронного окисления катионами серебра.
Смотрите также
Рекомендации
- ^ Бертон, Джордж и др. (2000). Продвинутая химия Солтерса: химия (2-е изд.). Heinemann. ISBN 0-435-63120-9
- ^ Десс, Д. Б .; Мартин, Дж. К. Варенье. Chem. Soc. 1991, 113, 7277–87.
- ^ J. S. Yadav, et al. «Повторно используемые ионные жидкости 2-го поколения в качестве зеленых растворителей для окисления спиртов реагентами на основе гипервалентного йода», Тетраэдр, 2004, 60, 2131–35
