Перекись ацетона - Википедия - Acetone peroxide
 Примеры циклических димеров и тримеров | |||
| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК 3,3-диметил-1,2-диоксациклопропан (мономер) 3,3,6,6-тетраметил-1,2,4,5-тетраоксан (димер) 3,3,6,6,9,9-гексаметил- 3,3,6,6,9,9,12,12-октаметил- | |||
| Другие имена Трипероксид триацетона Пероксиацетон Мать сатаны | |||
| Идентификаторы | |||
3D модель (JSmol ) |
| ||
| ChemSpider | |||
| Номер E | E929 (глазури, ...) | ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C6ЧАС12О4 (димер) C9ЧАС18О6 (тример) C12ЧАС24О8 (тетрамер) | |||
| Молярная масса | 148,157 г / моль (димер) 222,24 г / моль (тример) | ||
| Внешность | Белое кристаллическое твердое вещество | ||
| Температура плавления | 131,5 до 133 ° C (димер)[1] 91 ° C (тример) | ||
| Точка кипения | От 97 до 160 ° C (от 207 до 320 ° F; от 370 до 433 K) | ||
| Нерастворимый | |||
| Опасности | |||
| Пиктограммы GHS |   | ||
| NFPA 704 (огненный алмаз) | |||
| Взрывоопасные данные | |||
| Чувствительность к ударам | Высокая / Высокая при намокании | ||
| Чувствительность к трению | Высокая / умеренная во влажном состоянии | ||
| Скорость детонации | 5300 РС при максимальной плотности (1,18 г / см3), около 2500–3000 м / с около 0,5 г / см3 17,384 фут / с 3,29 миль в секунду | ||
| RE фактор | 0.80 | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Перекись ацетона (также называемый APEX) является органический пероксид и начальный фугас. Он образуется в результате реакции ацетон и пероксид водорода чтобы получить смесь линейных мономер и циклический димер, тример, и тетрамер формы. Тример известен как трипероксид триацетона (ТАТП) или же пероксид трициклического ацетона (TCAP). Димер известен как дипероксид диацетона (ДАДФ). Перекись ацетона представляет собой белый кристаллический порошок с характерным отбеливать -подобный запах (в случае нечистоты) или фруктовый запах в чистом виде, и может сильно взорваться при воздействии тепла, трения, статического электричества, концентрированной серной кислоты, сильного УФ-излучения или шок. Примерно до 2015 года детекторы взрывчатых веществ не были настроены на обнаружение неазотистый взрывчатые вещества, поскольку большинство используемых взрывчатых веществ были на основе азота. Безазотный ТАТФ использовался в качестве предпочтительного взрывчатого вещества в нескольких террорист бомбовые атаки с 2001 года.
История
Перекись ацетона (в частности, трипероксид триацетона) была открыта в 1895 г. Ричард Вольфенштейн.[2][3][4] Вольфенштейн соединил ацетон и перекись водорода, а затем дал смеси постоять в течение недели при комнатной температуре, в течение этого времени выпадало небольшое количество кристаллов с температурой плавления 97 ° C (207 ° F).[5]
В 1899 г. Адольф фон Байер и Виктор Виллигер описал первый синтез димера и описал использование кислот для синтеза обоих пероксидов.[6][7][8][9][10] Байер и Виллигер получили димер путем объединения персульфат калия в диэтиловый эфир с ацетоном при охлаждении. После отделения эфирного слоя продукт очищали и обнаруживали, что он плавится при 132–133 ° C (270–271 ° F).[11] Они обнаружили, что тример можно приготовить, добавив соляная кислота к охлажденной смеси ацетона и пероксид водорода.[12] Используя снижение точек замерзания Чтобы определить молекулярные массы соединений, они также определили, что форма пероксида ацетона, которую они получили с помощью персульфата калия, была димером, тогда как пероксид ацетона, который был получен с помощью соляной кислоты, был тримером, как соединение Вольфенштейна.[13]
Работа над этой методологией и над различными полученными продуктами была дополнительно исследована в середине 20 века Миласом и Голубовичем.[14]
Химия
Химическое название пероксид ацетона чаще всего используется для обозначения циклического тримера, продукта реакции между двумя предшественники, перекись водорода и ацетон, в кислотномкатализированный нуклеофильное присоединение, хотя возможны различные другие мономерные и димерные формы.[нужна цитата ]
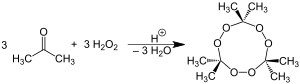
В частности, два димера, один циклический (C6ЧАС12О4)[нужна цитата ] и одна открытая цепь (C6ЧАС14О4)[нужна цитата ], а также мономер с открытой цепью (C3ЧАС8О4),[15] также могут быть сформированы; при определенных условиях концентрации реагента и кислотного катализатора циклический тример является первичным продуктом.[14] Также описана тетрамерная форма при различных каталитических условиях.[16] Синтез тетрамерного пероксида ацетона оспаривается.[17][18] Сообщается, что в нейтральных условиях реакция дает мономерный органический пероксид.[14]
Наиболее распространенный путь получения почти чистого ТАТФ - H2О2/ ацетон / HCl в молярном соотношении 1: 1: 0,25 с использованием 30% перекиси водорода. Этот продукт содержит очень мало или совсем не содержит DADP с очень небольшими следами хлорированных соединений. Продукт, содержащий большую долю DADP, может быть получен из 50% H2О2 используя большое количество конц. серная кислота в качестве катализатора или, альтернативно, с 30% H2О2 и огромное количество HCl в качестве катализатора.[19]
Продукт, полученный с использованием соляной кислоты, считается более стабильным, чем продукт, полученный с использованием серной кислоты. Известно, что следы серной кислоты, захваченные внутри образовавшихся кристаллов пероксида ацетона, приводят к нестабильности. Фактически, захваченная серная кислота может вызывать детонацию при температуре до 50 ° C (122 ° F), это наиболее вероятный механизм случайных взрывов пероксида ацетона, которые происходят во время сушки на нагретых поверхностях.[20]
Трипероксид триацетона образуется в 2-пропаноле при длительном стоянии в присутствии воздуха.[21]

Органические пероксиды в целом являются чувствительными, опасными взрывчатыми веществами, а все формы пероксида ацетона чувствительны к инициация.[нужна цитата ] ТАТФ разлагается со взрывом; экспертиза взрывчатого вещества разложение ТАТП на самом краю фронта детонации предсказывает «образование ацетон и озон как основные продукты разложения, а не интуитивно ожидаемые продукты окисления ».[22] Очень мало тепла создается взрывным разложением ТАТФ на самом краю фронта детонации; приведенный выше вычислительный анализ предполагает, что разложение TATP как энтропийный взрыв.[22] Однако эта гипотеза была оспорена как не соответствующая фактическим измерениям.[23] Утверждение об энтропийном взрыве было связано с событиями сразу за фронтом детонации. Авторы книги Дубникова и др. 2004 г. исследования подтверждают, что окончательная окислительно-восстановительная реакция (горение) озона, кислорода и химически активных веществ в воду, различные оксиды и углеводороды происходит в течение примерно 180 пс после начальной реакции - примерно в пределах одного микрона от детонационной волны. Детонирующие кристаллы ТАТФ в конечном итоге достигают температуры 2300 К (2030 ° C; 3680 ° F) и давления 80 кбар.[24] Конечная энергия детонации составляет около 2800 кДж / кг (измеряется в гелии) - этого достаточно, чтобы -кратко- повысить температуру газообразных продуктов до 2000 ° C (3630 ° F). Объем газов при STP составляет 855 л / кг для ТАТФ и 713 л / кг для ДАДФ (измеряется в гелии).[23]
Тетрамерная форма пероксида ацетона, полученная в нейтральных условиях с использованием банка катализатор в присутствии хелатор или общий ингибитор радикальная химия, как сообщается, является более химически стабильным, но все же очень опасным первичное взрывчатое вещество.[16] Его синтез оспаривается.[18]
И ТАТФ, и ДАДФ склонны к потере массы из-за сублимация. DADP имеет более низкий молекулярный вес и выше давление газа. Это означает, что DADP более подвержен сублимации, чем TATP.
Для анализа следов TATP можно использовать несколько методов,[25] включая газовую хроматографию / масс-спектрометрию (ГХ / МС),[26][27][28][29][30] высокоэффективная жидкостная хроматография / масс-спектрометрия (ВЭЖХ / МС),[31][32][33][34][35] и ВЭЖХ с постколоночной дериватизацией.[36]
Перекись ацетона растворима в толуоле, хлороформе, ацетоне, дихлорметане и метаноле.[37] Перекристаллизация первичных взрывчатых веществ может давать большие кристаллы, которые самопроизвольно взрываются из-за внутренней деформации.[38]
Промышленное использование
Кетон пероксиды, включая пероксид ацетона и пероксид метилэтилкетона, найти применение как инициаторы за полимеризация реакции, например, силикон или же полиэстер смолы, в создании стекловолокно -армированные композиты.[нужна цитата ] Для этих целей пероксиды обычно находятся в форме разбавленного раствора в органическом растворителе; Для этой цели чаще используется пероксид метилэтилкетона, так как он стабилен при хранении.[нужна цитата ]
Перекись ацетона используется как отбеливатель муки отбеливать и «выдерживать» муку.[39]
Пероксиды ацетона являются нежелательными побочными продуктами некоторых реакций окисления, например, используемых в фенол синтезы.[40] Из-за их взрывоопасной природы их присутствие в химических процессах и химических образцах создает потенциально опасные ситуации. Случайное происшествие при незаконном МДМА лаборатории возможно.[41] Для уменьшения их внешнего вида используются многочисленные методы, в том числе смещение pH на более щелочной, регулируя температуру реакции или добавляя ингибиторы их производства.[40] Например, пероксид триацетона является основным загрязнителем, содержащимся в диизопропиловый эфир в результате фотохимический окисление на воздухе.[42]
Использование в самодельных взрывных устройствах
TATP использовался при взрывах бомб и террористов-смертников, а также в самодельных взрывных устройствах, в том числе Взрывы в Лондоне 7 июля 2005 г., где четыре террориста-смертника убили 52 человека и ранили более 700 человек.[43][44][45][46] Это было одно из взрывных устройств, использованных "бомбардировщиком обуви". Ричард Рид[47][48][46] в его 2001 неудачная попытка бомбы из обуви и использовался террористами-смертниками в Ноябрь 2015 Атаки в Париже,[49] Взрывы в Брюсселе в 2016 году,[50] Взрыв Манчестер Арены, Атака в Брюсселе в июне 2017 г.,[51] Взрыв Парсонс-Грин,[52] то Взрывы в Сурабае,[53] и Взрывы на Пасху в Шри-Ланке в 2019 году.[54][55] Полиция Гонконга утверждают, что нашли 2 кг (4,4 фунта) ТАТФ среди оружия и материалов протеста в июле 2019 года, когда проходили массовые протесты против предложенного закона разрешение экстрадиции в материковый Китай.[56]
ТАТП ударная волна избыточное давление составляет 70% от значения для TNT, импульс положительной фазы составляет 55% от эквивалента TNT. ТАТФ при 0,4 г / см3 около одной трети бризантность тротила (1,2 г / см3) измеряется тестом Гесса.[57]
ТАТФ привлекателен для террористов, поскольку его легко приготовить из легко доступных розничных ингредиентов, таких как отбеливатель для волос и жидкость для снятия лака.[49] Он также смог избежать обнаружения, потому что это один из немногих взрывчатых веществ, не содержащих азот,[58] и поэтому мог пройти незамеченным через стандартные обнаружение взрывчатых веществ сканеры, которые до сих пор были разработаны для обнаружения азотсодержащих взрывчатых веществ.[59] К 2016 году детекторы взрывчатых веществ были модифицированы, чтобы они могли обнаруживать ТАТФ, и были разработаны новые типы.[60][61]
В Европейском союзе приняты законодательные меры по ограничению продажи концентрированной перекиси водорода до 12% и выше.[62]
Ключевым недостатком является высокая восприимчивость ТАТФ к случайной детонации, вызывающей несчастные случаи на рабочем месте и "собственные цели "среди незаконных изготовителей бомб, что привело к тому, что ТАТП стали называть" Матерью Сатаны ".[61][58] ТАТФ был обнаружен в результате случайного взрыва, предшествовавшего Теракты 2017 г. в Барселоне и окрестностях.[63]
Крупномасштабный синтез ТАТФ часто сопровождается чрезмерным запахом отбеливателя или фруктовым запахом. Этот запах может проникать даже в одежду и волосы в довольно заметных количествах. Человек, который делал ТАТФ, «пахнет химикатами»; об этом сообщается в Взрывы в Брюсселе в 2016 году.[64]
Рекомендации
- ^ Федерофф, Бэзил Т. и др., Энциклопедия взрывчатых веществ и сопутствующих товаров (Спрингфилд, Вирджиния: Национальная служба технической информации, 1960), т. 1, п. A41.
- ^ Вольфенштейн Р. (1895). "Uber die Einwirkung von Wasserstoffsuperoxyd auf Aceton und Mesityloxyd" [О действии перекиси водорода на ацетон и мезитилоксид]. Berichte der Deutschen Chemischen Gesellschaft (на немецком). 28 (2): 2265–2269. Дои:10.1002 / cber.189502802208. Вольфенштейн определил, что пероксид ацетона образует тример, и предложил его структурную формулу. С стр. 2266–2267: "Die Physikalischen Eigenschaften des Superoxyds, der feste Aggregatzustand, die Unlöslichkeit in Wasser и т. Д. Sprachen dafür, dass das Molekulargewicht desselben ein grösseres wäre, als dem einfachen ein grösseres wäre, als dem einfachen ein grösseres wäre, als dem einfachen ein grösseres wäre ... einfachen einfachen ein grösseres wäre ... indem sich die Bindungen zwischen je zwei Sauerstoffatomen lösen und zur Verknüpfung mit den Sauerstoffatomen eines benachbarten Moleküls dienen. Человек желает так zur folgenden Конституции: [схема предполагаемой молекулярной структуры тримера пероксида ацетона] . Diese eigenthümliche ringförmig constituirte Verbindung soll Tri-Cycloacetonsuperoxyd genannt werden ". (Физические свойства пероксида, его твердое агрегатное состояние, его нерастворимость в воде и т. Д. Предполагают, что его молекулярный вес будет больше [единицы], чем соответствует его простой эмпирической формуле ... Таким образом [результат молекулярного определение веса показало, что] присутствует трехмолекулярный пероксид ацетона, который может возникать из мономера в результате разрыва связей между каждой парой атомов кислорода [на одной молекуле пероксида ацетона] и служить связями с атомами кислорода соседнего Таким образом, приходим к следующей структурной формуле: [диаграмма предполагаемой молекулярной структуры тримеров пероксида ацетона]. Это странное кольцеобразное соединение будет называться «пероксид трициклоацетон».)
- ^ Wolfenstein R (1895) Deutsches Reichspatent 84953
- ^ Матяш Р., Пахман Дж. (2013). Первичные взрывчатые вещества. Берлин: Springer. п. 262. ISBN 978-3-642-28436-6.
- ^ (Вольфенштейн, 1895), стр. 2266.
- ^ Байер, Адольф и Виллигер, Виктор (1899) "Einwirkung des Caro'schen Reagens auf Ketone" (Влияние реактива Каро на кетоны [часть 1]), Berichte der deutschen chemischen Gesellschaft, 32 : 3625–3633, см. стр. 3632.
- ^ Байер А., Виллигер V (1900). "Über die Einwirkung des Caro'schen Reagens auf Ketone" [О действии реактива Каро на кетоны [часть 3]]. Berichte der Deutschen Chemischen Gesellschaft. 33 (1): 858–864. Дои:10.1002 / cber.190003301153.
- ^ Байер А., Виллигер V (1900). "Uber die Nomenclatur der Superoxyde und die Superoxyde der Aldehyde" [О номенклатуре пероксидов и пероксидов альдегидов]. Berichte der Deutschen Chemischen Gesellschaft. 33 (2): 2479–2487. Дои:10.1002 / cber.190003302185.
- ^ Федерофф, Бэзил Т. и др., Энциклопедия взрывчатых веществ и сопутствующих товаров (Спрингфилд, Вирджиния: Национальная служба технической информации, 1960), т. 1, п. A41.
- ^ Матяш, Роберт и Пахман, Иржи, ред. Первичные взрывчатые вещества (Берлин, Германия: Springer, 2013), стр. 257.
- ^ (Байер и Виллигер, 1899), стр. 3632.
- ^ (Байер и Виллигер, 1900), стр. 859.
- ^ (Байер и Виллигер, 1900), стр. 859. С п. 859: "Das mit dem Caro'schen Reagens dargestellte, bei 132–133 ° schmelzende Superoxyd gab bei der Molekulargewichtsbestimmung nach der Gefrierpunktsmethode Resultate, welche zeigen, dass es dimolekular ist. Um zu segeszomteo das, obäste das 90 - das segeszomte das. ° mit dem Wolffenstein'schen identityisch ist, wurde davon ebenfalls eine Molekulargewichtsbestimmung gemacht, welche auf Zahlen führte, die für ein trimolekulares Superoxyd стимулы ». (Пероксид, который был приготовлен с реактивом Каро и который плавился при 132–133 ° C (270–271 ° F), дал - согласно определению молекулярной массы методом точки замерзания - результаты, которые показывают, что он является димолекулярным. Чтобы увидеть, идентичен ли пероксид, полученный с соляной кислотой и имеющий температуру плавления 90–94 ° C (194–201 ° F), пероксиду Вольфенштейна, аналогичным образом было проведено определение его молекулярной массы, в результате чего были получены числа, которые верны для тримолекулярной перекиси.)
- ^ а б c Милас Н.А., Голубович А. (1959). «Исследования органических пероксидов. XXVI. Органические пероксиды, полученные из ацетона и пероксида водорода». Журнал Американского химического общества. 81 (24): 6461–6462. Дои:10.1021 / ja01533a033.
- ^ Это не тот DMDO мономер, упоминаемый в Chembox, а скорее дигидромономер с открытой цепью, описанный Milas & Goluboviç, op. соч.
- ^ а б Цзян Х., Чу Г, Гун Х., Цяо Кью (1999). «Катализируемое хлоридом олова окисление ацетона перекисью водорода до тетрамерного перекиси ацетона». Журнал химических исследований. 28 (4): 288–289. Дои:10.1039 / a809955c. S2CID 95733839.
- ^ Первичные взрывчатые вещества - Роберт Матяш, Иржи Пахман (авт.), Стр.275
- ^ а б Matya´sˇ, R., Pachman, J .: Изучение ТАТФ: Влияние условий реакции на состав продукта. Пропелленты Взрывчатые вещества Пиротехника 35, 31–37 (2010) Сообщается, что это вещество представляет собой тетраацетонтетрапероксид; 3,3,6,6,9,9,12,12-октаметил-1,2,4,5,7,8,10,11-октаоксациклододекан (TeATeP) Schulte-Ladbeck et al. [20], Pena Quevedo et al. [21] или как структурный конформер ТАТФ по Widmer et al. [22]. Дальнейший анализ этого побочного продукта мы не проводили. Удалить это вещество путем повторной перекристаллизации или сублимации было невозможно. Как мы обнаружили и опубликовали ранее [23, 24], можно уменьшить количество этого вещества путем длительной термической обработки при более высоких температурах.
- ^ Матяш Р., Пахман Дж. (10 ноября 2009 г.). «Изучение ТАТФ: Влияние условий реакции на состав продукта». Топливо, взрывчатые вещества, пиротехника. 35 (1): 31–37. Дои:10.1002 / преп.200800044.
- ^ Матиас Р., Пачман Дж. (1 июля 2007 г.). «Термическая стабильность трипероксида триацетона». Наука и технология энергетических материалов. 68: 111–116.
- ^ Пай, Кори (10 июня 2020 г.). «Химическая безопасность: образование ТАТФ в 2-пропаноле». ACS Химическое здоровье и безопасность. 27: 279–279. Дои:10.1021 / acs.chas.0c00061.CS1 maint: дата и год (связь)
- ^ а б Дубникова, Фаина; Кослофф, Ронни; Альмог, Джозеф; Зейри, Иегуда; Бозе, Роланд; Ицхаки, Харель; Альт, Аарон; Кейнан, Эхуд (2005). «Разложение трипероксида триацетона - энтропийный взрыв». Журнал Американского химического общества. 127 (4): 1146–1159. Дои:10.1021 / ja0464903. PMID 15669854.
- ^ а б Синдицкий В.П., Кольцов В.И., Егоршев В.Ю., Патрикеев Д.И., Дорофеева О.В. (2014). «Термохимия пероксидов циклического ацетона». Термохимика Акта. 585: 10–15. Дои:10.1016 / j.tca.2014.03.046.
- ^ Ван Дуин А.С., Зейри Ю., Дубникова Ф., Кослофф Р., Годдард В.А. (2005). "Моделирование в атомном масштабе начальных химических событий при термическом инициировании триацетонетрипероксида". Журнал Американского химического общества. 127 (31): 11053–62. Дои:10.1021 / ja052067y. PMID 16076213.
- ^ Schulte-Ladbeck R, Vogel M, Karst U (октябрь 2006 г.). «Современные методы определения взрывчатых веществ на основе пероксидов». Аналитическая и биоаналитическая химия. 386 (3): 559–65. Дои:10.1007 / s00216-006-0579-y. PMID 16862379. S2CID 38737572.
- ^ Мюллер Д., Леви А., Шелеф Р., Абрамович-Бар С., Зоненфельд Д., Тамири Т. (сентябрь 2004 г.). «Усовершенствованный метод обнаружения ТАТФ после взрыва». Журнал судебной медицины. 49 (5): 935–8. Дои:10.1520 / JFS2003003. PMID 15461093.
- ^ Стамбули А., Эль-Бури А., Буаюн Т., Беллимам Массачусетс (декабрь 2004 г.). «Обнаружение следов ТАТФ в поствзрывном мусоре с помощью газовой хроматографии / масс-спектрометрии над паром». Международная криминалистическая экспертиза. 146 Дополнение: S191–4. Дои:10.1016 / j.forsciint.2004.09.060. PMID 15639574.
- ^ Оксли Дж. К., Смит Дж. Л., Шинде К., Моран Дж. (2005). «Определение плотности паров трипероксида триацетона (ТАТФ) с использованием метода газовой хроматографии над свободным пространством». Топливо, взрывчатые вещества, пиротехника. 30 (2): 127. Дои:10.1002 / преп.200400094.
- ^ Sigman ME, Clark CD, Fidler R, Geiger CL, Clausen CA (2006). «Анализ трипероксида триацетона с помощью газовой хроматографии / масс-спектрометрии и газовой хроматографии / тандемной масс-спектрометрии с помощью электронной и химической ионизации». Быстрые коммуникации в масс-спектрометрии. 20 (19): 2851–7. Bibcode:2006RCMS ... 20.2851S. Дои:10.1002 / RCM.2678. PMID 16941533.
- ^ Romolo FS, Cassioli L, Grossi S, Cinelli G, Russo MV (январь 2013 г.). «Отбор проб с поверхности и анализ ТАТФ с помощью мазков и газовой хроматографии / масс-спектрометрии». Международная криминалистическая экспертиза. 224 (1–3): 96–100. Дои:10.1016 / j.forsciint.2012.11.005. PMID 23219697.
- ^ Видмер Л., Уотсон С., Шлаттер К., Кроусон А. (декабрь 2002 г.). «Разработка метода ЖХ / МС для анализа следов трипероксида триацетона (ТАТФ)». Аналитик. 127 (12): 1627–32. Bibcode:2002Ana ... 127.1627W. Дои:10.1039 / B208350G. PMID 12537371.
- ^ Сюй Х, ван де Краатс А.М., Кок Е.М., де Брюн П.С. (ноябрь 2004 г.). «Анализ следов пероксидных взрывчатых веществ с помощью высокоэффективной жидкостной хроматографии, химической ионизации и тандемной масс-спектрометрии при атмосферном давлении (HPLC-APCI-MS / MS) для судебно-медицинских исследований». Журнал судебной медицины. 49 (6): 1230–6. PMID 15568694.
- ^ Котте-Родригес I, Эрнандес-Сото Х., Чен Х., Cooks RG (март 2008 г.). «Обнаружение следов пероксидных взрывчатых веществ на месте путем десорбционной ионизации электрораспылением и десорбционной химической ионизации при атмосферном давлении». Аналитическая химия. 80 (5): 1512–9. Дои:10.1021 / ac7020085. PMID 18247583.
- ^ Sigman ME, Clark CD, Caiano T, Mullen R (2008). «Анализ трипероксида триацетона (ТАТФ) и синтетических промежуточных продуктов ТАТФ методом масс-спектрометрии с ионизацией электрораспылением». Быстрые коммуникации в масс-спектрометрии. 22 (2): 84–90. Bibcode:2008RCMS ... 22 ... 84S. Дои:10.1002 / RCM.3335. PMID 18058960.
- ^ Sigman ME, Clark CD, Painter K, Milton C, Simatos E, Frisch JL, McCormick M, Bitter JL (февраль 2009 г.). «Анализ олигомерных пероксидов в образцах синтетического трипероксида триацетона методом тандемной масс-спектрометрии». Быстрые коммуникации в масс-спектрометрии. 23 (3): 349–56. Bibcode:2009RCMS ... 23..349S. Дои:10.1002 / RCM.3879. PMID 19125413.
- ^ Шульте-Ладбек Р., Колла П., Карст У. (февраль 2003 г.). «Анализ следов взрывчатых веществ на основе перекиси водорода». Аналитическая химия. 75 (4): 731–5. Дои:10.1021 / ac020392n. PMID 12622359.
- ^ Кенде, Анико; Лебикс, Ференц; Эке, Жужанна; Торкос, Корнел (2008). «Идентификация следовых количеств триацетона-трипероксида с помощью SPME – GC-MS в модельных системах». Microchimica Acta. 163 (3–4): 335–338. Дои:10.1007 / s00604-008-0001-x. S2CID 97978057.
- ^ Первичные взрывчатые вещества - стр. 278, ISBN 9783642284359
- ^ Ferrari CG, Хигасиучи К., Подлиска Я. (1963). «Созревание и отбеливание муки с помощью ациклических пероксидов ацетон» (PDF). Зерновая химия. 40: 89–100.
- ^ а б США 5003109, Костантини, Мишель, "Разрушение пероксида ацетона", опубликовано 26 марта 1991 г.
- ^ Берк, Роберт А. (25 июля 2006 г.). Контртерроризм для аварийно-спасательных служб, второе издание. п. 213. ISBN 9781138747623.
- ^ Акри Ф, Халлер Х.Л. (1943). «Тримолекулярный пероксид ацетона в изопропиловом эфире». Журнал Американского химического общества. 65 (8): 1652. Дои:10.1021 / ja01248a501.
- ^ «Настоящая история 7/7», Наблюдатель, 7 мая 2006 г.
- ^ [1]Лондон бомбардировщики использовали бытовые материалы - США. полиция, Reuters, 4 августа 2005 г.
- ^ Нотон П. (15 июля 2005 г.). «ТАТП - излюбленное оружие террористов-смертников». The Times (Великобритания). Архивировано из оригинал 10 февраля 2008 г.
- ^ а б Винс Джи (15 июля 2005 г.). «Взрывчатые вещества, связанные с взрывами в Лондоне, определены». Новый ученый.
- ^ «Судья отказывает в освобождении под залог обвиняемого в бомбардировке обуви». CNN. 28 декабря 2001 г.
- ^ «Террористическое использование взрывчатого вещества ТАТП». officialconfusion.com. 25 июля 2005 г.
- ^ а б Каллимачи Р., Рубин А.Дж., Фурке Л. (19 марта 2016 г.). «Взгляд на эволюцию ИГИЛ в новых подробностях атак на Париж». Нью-Йорк Таймс.
- ^ "'La mère de Satan 'ou TATP, l'explosif preféré de l'EI " [«Мать сатаны» или ТАТП, предпочтительное взрывчатое вещество для СВУ]. LeVif.be Express (На французском). 23 марта 2016 г.
- ^ Доэрти Б. (25 мая 2017 г.). «В бомбе в Манчестере использовалось то же взрывчатое вещество, что и при терактах в Париже и Брюсселе, - говорит американский законодатель». Хранитель. Получено 16 сентября 2017.
- ^ Дирден, Лиззи (16 сентября 2017 г.). «Атака в Лондоне: бомбардировщики Парсонс-Грин« все еще там »спустя более 24 часов после взрыва на метро, предупреждают официальные лица». Независимый. Получено 5 ноября 2017.
- ^ "'Взрывчатые вещества Матери Сатаны, использованные при взрывах в церкви Сурабая: Полиция ». The Jakarta Post. 14 мая 2018. Получено 15 мая 2018.
- ^ Times, Азия. "Asia Times | Взрывное устройство" Мать Сатаны ", использованное во время взрывов в Шри-Ланке | Статья". Asia Times. Получено 24 апреля 2019.
- ^ Взрывчатка TATP, использованная в пасхальных атаках - бывший DIG Нимал Левке News First (Шри-Ланка), проверено 23 апреля 2019 года.
- ^ «Протесты в Гонконге: полиция проверяет связь с огромным вывозом взрывчатки». Новости BBC. 20 июля 2019.
- ^ Пахман, Дж; Matyáš, R; Кюнцель, М (2014). «Исследование ТАТП: характеристики взрыва и тротиловый эквивалент малых зарядов». Ударные волны. 24 (4): 439. Bibcode:2014ShWav..24..439P. Дои:10.1007 / s00193-014-0497-4. S2CID 122101166.
- ^ а б Glas K (6 ноября 2006 г.). «ТАТП: противостояние матери сатаны». Будущее вещей. Получено 24 сентября 2009.
Огромная разрушительная сила TATP, вместе с относительной легкостью его создания, а также сложностью его обнаружения сделали TATP одним из излюбленных видов оружия террористов.
- ^ «Федералы все мокрые о безопасности аэропорта». Star-Ledger. Ньюарк, Нью-Джерси. 24 августа 2006 г.. Получено 11 сентября 2009.
В настоящее время, по словам Уоттса, устройства для досмотра настроены на обнаружение взрывчатых веществ на основе азота, в категорию которых не входит TATP.
[постоянная мертвая ссылка ] - ^ Джейкоби, Митч (29 марта 2016 г.). «Взрывчатое вещество, используемое в Брюсселе, обнаружить несложно». Новости химии и машиностроения. Получено 28 января 2018.
- ^ а б Genuth I, Fresco-Cohen L (6 ноября 2006 г.). «ТАТП: противостояние матери сатаны». Будущее вещей. Получено 24 сентября 2009.
Огромная разрушительная сила TATP, вместе с относительной легкостью его создания, а также сложностью его обнаружения сделали TATP одним из излюбленных видов оружия террористов.
- ^ «Регламент (ЕС) № 98/2013 Европейского парламента и Совета от 15 января 2013 года о маркетинге и использовании прекурсоров взрывчатых веществ. Текст, имеющий отношение к ЕЭЗ».
- ^ Уоттс Дж., Бурген С. (21 августа 2017 г.). «Полиция расширяет охоту на подозреваемого в нападении в Барселоне по всей Европе». Хранитель. Получено 16 сентября 2017.
- ^ Эндрю Хиггинс; Кимико де Фрейтас-Тамура (26 марта 2016 г.). «В Брюссельском заговоре с бомбами - след не связанных точек». Нью-Йорк Таймс. Получено 28 марта 2016.
внешняя ссылка
 СМИ, связанные с Перекись ацетона в Wikimedia Commons
СМИ, связанные с Перекись ацетона в Wikimedia Commons- ChemSub Online: пероксид ацетона - трипероксид триацетона.