Бомбыколь - Bombykol
 | |
| Имена | |
|---|---|
| Название ИЮПАК (10E,12Z) -гексадека-10,12-диен-1-ол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C16ЧАС30О | |
| Молярная масса | 238.415 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бомбыколь это феромон выпущен женщиной тутовый шелкопряд моль для привлечения партнеров. Это также половой феромон у дикой шелковой моли (Бомбикс мандарина ).[1][2] Обнаружил Адольф Бутенандт в 1959 году это был первый феромон, химически охарактеризованный.[3]
Небольшие количества этого феромона можно использовать на акр земли, чтобы сбить с толку самцов насекомых о местонахождении их партнеров-самок. Таким образом, он может служить приманкой в ловушках для эффективного удаления насекомых без опрыскивания сельскохозяйственных культур большим количеством пестицидов. Бутенандт назвал вещество в честь латинского названия моли. Bombyx mori.[4]
В естественных условиях По-видимому, бомбикол является естественным лигандом для связывающего феромон белка, BmorPBP, который сопровождает феромон к рецептору феромона.[5]
Биосинтез
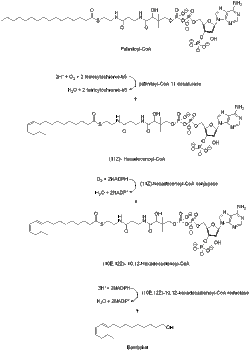
Известно, что бомбыкол получают из ацетил-КоА через C-16 жирный ацил пальмитоил-КоА.[6] Пальмитоил-КоА превращается в бомбикол на стадиях, которые включают десатурацию и восстановительную модификацию карбонильного углерода.[7] По сравнению с другими феромонами типа I, биосинтез бомбикола не требует укорочения цепи или какой-либо другой модификации концевой гидроксильной группы.
Фермент десатураза, кодируемый геном Bmpgdesat1 (Desat1), продуцирует моноен (11Z) -гексадеценоил-КоА, а также диен (10E, 12Z) -10,12-гексадекадиеноил-КоА. Эта десатураза - единственный фермент, необходимый для катализа этих двух последовательных стадий десатурации.[8]
Предшественник бомбыколацила (10E, 12Z) -10,12-гексадекадиеноат в основном обнаруживается в виде сложного эфира триацилглицерина в липидных каплях цитоплазмы клеток феромонной железы моли. А когда взрослые самки выходят из куколок, нейрогормон PBAN (нейропептид, активирующий биосинтез феромонов) запускает сигнальные события, которые помогают контролировать липолиз хранящихся триацилглицеринов, высвобождая (10E, 12Z) -10,12-гексадекадиеноат для его окончательной восстановительной модификации. .[9][10][11] Механизм липолитического высвобождения (10E, 12Z) -10,12-гексадекадиеноата из триацилглицеринов полностью не известен, но гены-кандидаты, кодирующие липазу, идентифицированы.[9][10]
Рекомендации
- ^ Кувахара, Ясумаса (1984). "Время полета самцов Bombyx mandarina к феромонной ловушке, наживленной бомбыколом". Прикладная энтомология и зоология. 19 (3): 400–401. Дои:10.1303 / aez.19.400.
- ^ Кувахара, Ясумаса; Мори, Наоки; Ямада, Шигеки; Немото, Тадаши (1984). «Оценка бомбыкола как полового феромона Bombyx mandarina (Lepidoptera: Bombycidae)». Прикладная энтомология и зоология. 19 (2): 265–267. Дои:10.1303 / aez.19.265.
- ^ Бутенандт, А.; Beckamnn, R .; Хеккер, Э. (1961). "Über den Sexuallockstoff des Seidenspinners .1. Der biologische Test und die Isolierung des reinen Sexuallockstoffes Bombykol". Hoppe-Seyler's Zeitschrift für Physiologische Chemie. 324: 71–83. Дои:10.1515 / bchm2.1961.324.1.71. PMID 13689417.
- ^ «Молекула недели». Американское химическое общество. 2004. Архивировано с оригинал 7 августа 2004 г.. Получено 2 марта, 2013.
- ^ Леал, Уолтер С. (2005). «Феромонный прием». В Шульце, Стефан (ред.). Химия феромонов и других полухимических веществ II. Springer. Дои:10.1007 / b98314. ISBN 9783540213086. Получено 2 марта, 2013.
- ^ Каспи и др., Nucleic Acids Research 42: D459-D471 2014.
- ^ Андо, Т; Hase, T; Arima, R; Учияма М. (1988). «Биосинтетический путь бомбикола, полового феромона самок тутового шелкопряда». Сельскохозяйственная и биологическая химия. 52 (2): 473–478. Дои:10.1271 / bbb1961.52.473.
- ^ Мото, К; Сузуки, MG; Халл, JJ; Kurata, R; Такахаши, S; Ямамото, М.; Окано, К; Имаи, К; Андо, Т; Мацумото, S (2004). «Вовлечение бифункциональной жирно-ацилдесатуразы в биосинтез шелкопряда, Bombyx mori, полового феромона». Труды Национальной академии наук. 101 (23): 8631–6. Bibcode:2004ПНАС..101.8631М. Дои:10.1073 / pnas.0402056101. ЧВК 423246. PMID 15173596.
- ^ а б Чжан, SD; Ли, Х; Бин, Z; Ду, МФ; Инь, ХМ; Ан, Ш (2014). «Молекулярная идентификация гена панкреатической липазы, участвующего в биосинтезе половых феромонов Bombyx mori». Наука о насекомых. 21 (4): 459–68. Дои:10.1111/1744-7917.12053. PMID 23955937.
- ^ а б Охниши, А; Кадзи, М; Хашимото, К; Мацумото, S (2011). «Скрининг генов, участвующих в биосинтезе бомбикола: идентификация и функциональная характеристика белка-носителя ацила Bombyx mori». Границы эндокринологии. 2: 92. Дои:10.3389 / fendo.2011.00092. ЧВК 3355880. PMID 22649392.
- ^ Мацумото, S; Одзава, Р. Учиуми, К; Курихара, М. (1996). «Бесклеточное производство полового феромона тутового шелкопряда бомбыкол». Биология, биотехнология и биохимия. 60 (2): 369–73. Дои:10.1271 / bbb.60.369. PMID 9063992.
