Псевдоген - Pseudogene

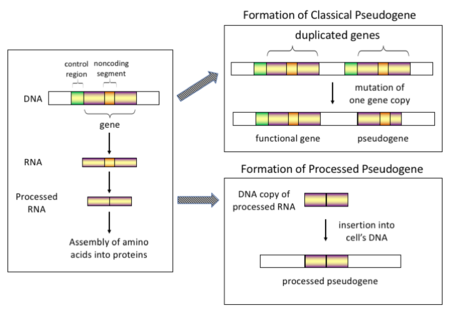
Псевдогены нефункциональные сегменты ДНК которые напоминают функциональные гены. Большинство из них возникают в виде избыточных копий функциональных генов либо непосредственно в результате дупликации ДНК, либо косвенно обратная транскрипция из мРНК стенограмма. Псевдогены обычно идентифицируются, когда анализ последовательности генома обнаруживает геноподобные последовательности, в которых отсутствуют регуляторные последовательности, необходимые для транскрипция или же перевод, или чьи кодовые последовательности явно дефектны из-за кадровые сдвиги или преждевременный стоп-кодоны.
Большинство небактериальных геномов содержат много псевдогенов, часто столько же, сколько функциональных генов. Это неудивительно, поскольку ожидается, что различные биологические процессы будут случайно создавать псевдогены, а специальных механизмов для их удаления из геномов не существует. В конце концов, псевдогены могут быть случайно удалены из своих геномов. Репликация ДНК или же Ремонт ДНК ошибок, или они могут накапливать так много мутационный изменения, которые больше не распознаются как бывшие гены. Анализ этих событий дегенерации помогает выяснить влияние неселективных процессов в геномах.
Последовательности псевдогена могут быть транскрибированы в РНК на низких уровнях из-за промоутер элементы, унаследованные от предкового гена или возникшие в результате новых мутаций. Хотя большинство из этих транскриптов не будут иметь большего функционального значения, чем случайные транскрипты из других частей генома, некоторые из них привели к появлению полезных регуляторных РНК и новых белков.
Характеристики
Псевдогены обычно характеризуются сочетанием гомология известному гену и потере некоторых функций. То есть, хотя каждый псевдоген имеет ДНК последовательность, которая похожа на некоторый функциональный ген, они обычно не могут производить функциональные конечные белковые продукты.[1] Псевдогены иногда трудно идентифицировать и охарактеризовать в геномах, потому что два требования - гомология и потеря функциональности - обычно подразумеваются посредством выравнивания последовательностей, а не биологически подтверждены.
- Гомология подразумевается идентичностью последовательностей между последовательностями ДНК псевдогена и родительского гена. После выравнивание две последовательности, процент идентичных пар оснований вычисляется. Высокая идентичность последовательностей означает, что весьма вероятно, что эти две последовательности отличаются от общей предковой последовательности (являются гомологичными), и весьма маловероятно, что эти две последовательности эволюционировали независимо (см. Конвергентная эволюция ).
- Нефункциональность может проявляться по-разному. Обычно ген должен пройти несколько этапов, чтобы стать полностью функциональным белком: Транскрипция, пре-мРНК обработка, перевод, и сворачивание белка являются обязательными частями этого процесса. Если какой-либо из этих шагов не удается, последовательность может считаться нефункциональной. При высокопроизводительной идентификации псевдогенов наиболее часто выявляемые нарушения являются преждевременными. стоп-кодоны и кадровые сдвиги, которые почти всегда предотвращают трансляцию функционального белкового продукта.
Псевдогены для РНК гены обычно труднее обнаружить, поскольку они не нуждаются в трансляции и, следовательно, не имеют «рамок считывания».
Псевдогены могут затруднять молекулярно-генетические исследования. Например, амплификация гена ПЦР может одновременно амплифицировать псевдоген, который имеет аналогичные последовательности. Это известно как смещение ПЦР или смещение амплификации. Точно так же псевдогены иногда аннотируются как гены в геном последовательности.
Обработанные псевдогены часто создают проблему для предсказание генов программы, часто ошибочно идентифицируемые как настоящие гены или экзоны. Было высказано предположение, что идентификация обработанных псевдогенов может помочь повысить точность методов прогнозирования генов.[2]
Недавно было показано, что 140 человеческих псевдогенов транслируются.[3] Однако функция белковых продуктов, если таковая имеется, неизвестна.
Виды и происхождение
Существует четыре основных типа псевдогенов, каждый из которых имеет различные механизмы происхождения и характерные особенности. Классификации псевдогенов следующие:
Обработанный

В высшем эукариоты, особенно млекопитающие, ретротранспозиция - довольно частое событие, оказавшее огромное влияние на состав генома. Например, где-то между 30–44% человеческий геном состоит из повторяющихся элементов, таких как СИНУСЫ и ЛИНИИ (видеть ретротранспозоны ).[6][7] В процессе ретротранспозиции часть мРНК или же hnRNA транскрипт гена спонтанно обратная расшифровка обратно в ДНК и вставлен в хромосомную ДНК. Хотя ретротранспозоны обычно создают копии самих себя, это было показано в in vitro система, что они также могут создавать ретротранспонированные копии случайных генов.[8] После того, как эти псевдогены вставляются обратно в геном, они обычно содержат поли-А хвост, и обычно имели свои интроны сращен; это обе отличительные черты кДНК. Однако, поскольку они происходят из продукта РНК, процессированные псевдогены также лишены вышестоящих промоторов нормальных генов; таким образом, они считаются «мертвыми по прибытии», становясь нефункциональными псевдогенами сразу после события ретротранспозиции.[9] Однако эти вставки иногда вносят экзоны в существующие гены, обычно через альтернативно сращенный стенограммы.[10] Еще одной характеристикой процессированных псевдогенов является обычное усечение 5'-конца по отношению к родительской последовательности, что является результатом относительно непроцессивного механизма ретротранспозиции, который создает процессированные псевдогены.[11] Обработанные псевдогены постоянно создаются у приматов.[12] Человеческие популяции, например, имеют разные наборы обработанных псевдогенов у своих индивидуумов.[13]
Необработанный

Необработанные (или дублированные) псевдогены. Дублирование гена - еще один общий и важный процесс в эволюции геномов. Копия функционального гена может возникнуть в результате дублирования гена, вызванного: гомологичная рекомбинация при, например, повторяющихся синус последовательности на смещенных хромосомах и впоследствии приобретают мутации которые приводят к тому, что копия теряет функцию исходного гена. Дублированные псевдогены обычно имеют все те же характеристики, что и гены, включая неповрежденный экзон -интрон структура и регуляторные последовательности. Утрата функции дублированного гена обычно мало влияет на состояние организма. фитнес, поскольку все еще существует неповрежденная функциональная копия. Согласно некоторым эволюционным моделям, общие дублированные псевдогены указывают на эволюционное родство человека и других приматов.[14] Если псевдогенизация происходит из-за дупликации гена, это обычно происходит в первые несколько миллионов лет после дупликации гена, при условии, что ген не подвергался никаким воздействиям. давление отбора.[15] Дублирование генов порождает функциональные избыточность и обычно невыгодно иметь два идентичных гена. Мутации, нарушающие структуру или функцию любого из двух генов, не являются вредными и не удаляются в процессе отбора. В результате мутировавший ген постепенно становится псевдогеном и будет либо невыраженным, либо лишенным функции. Такую эволюционную судьбу показывает популяция генетическое моделирование[16][17] а также анализ генома.[15][18] В соответствии с эволюционным контекстом эти псевдогены будут либо удалены, либо станут настолько отличными от родительских генов, что их больше нельзя будет идентифицировать. Относительно молодые псевдогены можно распознать по сходству их последовательностей.[19]
Унитарные псевдогены

Различные мутации (например, инделы и бессмысленные мутации ) может помешать нормальному записано или же переведено, и, таким образом, ген может стать менее или нефункциональным или «дезактивированным». Это те же самые механизмы, с помощью которых непроцессированные гены становятся псевдогенами, но разница в этом случае состоит в том, что ген не дублировался до псевдогенизации. Обычно такой псевдоген вряд ли закрепится в популяции, но различные эффекты популяции, такие как генетический дрейф, а узкое место населения, или, в некоторых случаях, естественный отбор, может привести к фиксации. Классическим примером унитарного псевдогена является ген, предположительно кодирующий фермент. L-гулоно-γ-лактоноксидаза (GULO) у приматов. У всех исследованных млекопитающих, кроме приматов (кроме морских свинок), GULO помогает в биосинтезе аскорбиновая кислота (витамин C), но он существует как отключенный ген (GULOP) у людей и других приматов.[20][21] Другой более свежий пример отключенного гена связывает деактивацию каспаза 12 ген (через бессмысленная мутация ) к положительному отбору у людей.[22]
Было показано, что процессированные псевдогены накапливают мутации быстрее, чем непроцессированные псевдогены.[23]
Псевдопсевдогены
Быстрое распространение Секвенирование ДНК технологии привели к идентификации многих очевидных псевдогенов с использованием предсказание генов техники. Псевдогены часто идентифицируют по появлению преждевременного стоп-кодон в предсказанной последовательности мРНК, которая теоретически предотвратит синтез (перевод ) нормального белок продукт исходного гена. Было несколько сообщений о трансляционном считывании таких преждевременных стоп-кодонов у млекопитающих, как описано в разделе "Переводное чтение "в статье стоп-кодона. Как указано на рисунке выше, небольшое количество белкового продукта такого считывания все еще может быть распознаваемым и функционировать на каком-то уровне. Если это так, псевдоген может подвергаться естественный отбор. Похоже, это произошло во время эволюции Дрозофила разновидность, как описано далее.
В 2016 году сообщалось, что 4 предсказанных псевдогена во множестве Дрозофила виды на самом деле кодируют белки с биологически важными функциями,[24] «предполагая, что такие« псевдопсевдогены »могут представлять собой широко распространенное явление». Например, функциональный белок ( обонятельный рецептор ) встречается только в нейроны. Это открытие тканеспецифичных биологически-функциональных генов, которые могли быть отклонены как псевдогены in silico Анализ усложняет анализ данных последовательности. По состоянию на 2012 год выяснилось, что в геноме человека имеется примерно 12 000–14 000 псевдогенов,[25] почти сопоставимо с часто цитируемым приблизительным значением в 20 000 генов в нашем геноме. Текущая работа также может помочь объяснить, почему мы можем жить от 20 до 100 человек. предполагаемый гомозиготный Потеря функции мутации в наших геномах.[26]
Благодаря повторному анализу более 50 миллионов пептидов, полученных от человека протеом и разделены масс-спектрометрии, сейчас (2016) выясняется, что существует не менее 19 262 человеческих белка, производимых из 16 271 гена или кластера генов. В результате этого анализа было идентифицировано 8 новых генов, кодирующих белок, которые ранее считались псевдогенами.[27]
Примеры псевдогенной функции
Дрозофила рецептор глутамата. Термин «псевдопсевдоген» был придуман для гена, кодирующего хемосенсорные ионотропный рецептор глутамата Ir75a из Drosophila sechellia, который несет кодон преждевременной терминации (PTC) и поэтому был классифицирован как псевдоген. Тем не мение, in vivo в D. sechellia Локус Ir75a продуцирует функциональный рецептор благодаря трансляционному считыванию PTC. Считывание обнаруживается только в нейронах и зависит от нуклеотидной последовательности ниже PTC.[24]
миРНК. Некоторые эндогенные миРНК по-видимому, происходят из псевдогенов, и, таким образом, некоторые псевдогены играют роль в регуляции транскриптов, кодирующих белок, как описано в обзоре.[28] Один из многих примеров - psiPPM1K. Обработка РНК, транскрибируемых из psiPPM1K, дает siRNA, которые могут подавлять наиболее распространенный тип рака печени, гепатоцеллюлярная карцинома.[29] Это и многие другие исследования вызвали большой интерес по поводу возможности воздействия на псевдогены с помощью / в качестве терапевтических агентов.[30]
пиРНК. Немного пиРНК происходят из псевдогенов, расположенных в кластерах пиРНК.[31] Эти piRNA регулируют гены посредством пути piRNA в семенниках млекопитающих и имеют решающее значение для ограничения сменный элемент повреждение генома.[32]

микроРНК. Есть много сообщений о псевдогенных транскриптах, действующих как микроРНК приманки. Возможно, самым ранним определенным примером такого псевдогена, участвующего в раке, является псевдоген BRAF. Ген BRAF - это протоонкоген который, будучи видоизмененным, связан со многими видами рака. Обычно количество белка BRAF контролируется в клетках за счет действия miRNA. В нормальных ситуациях количество РНК из BRAF и псевдогена BRAFP1 конкурирует за miRNA, но баланс двух РНК таков, что клетки растут нормально. Однако, когда экспрессия РНК BRAFP1 увеличивается (экспериментально или в результате естественных мутаций), меньше miRNA доступно для контроля экспрессии BRAF, и повышенное количество белка BRAF вызывает рак.[33] Такого рода конкуренция за регуляторные элементы со стороны РНК, эндогенных для генома, породила термин ceРНК.
PTEN. В PTEN ген известен ген-супрессор опухоли. Псевдоген PTEN, PTENP1, представляет собой процессированный псевдоген, который очень похож по своей генетической последовательности на ген дикого типа. Однако у PTENP1 есть миссенс-мутация, которая устраняет кодон для инициирующий метионин и таким образом предотвращает трансляцию нормального белка PTEN.[34] Несмотря на это, PTENP1, по-видимому, играет роль в онкогенез. 3 ' UTR мРНК PTENP1 действует как приманка для мРНК PTEN путем нацеливания микро РНК из-за его сходства с геном PTEN и сверхэкспрессия 3'-UTR приводила к увеличению уровня белка PTEN.[35] То есть сверхэкспрессия 3 'UTR PTENP1 приводит к усилению регуляции и подавлению раковых опухолей. Биология этой системы в основном противоположна описанной выше системе BRAF.
Potogenes. Псевдогены могут на эволюционных временных масштабах участвовать в преобразование гена и другие мутационные события, которые могут привести к появлению новых или новых функциональных генов. Это привело к концепции, что псевдогены можно рассматривать как горшокogenes: горшокважные гены эволюционной диверсификации.[36]
Неправильно идентифицированные псевдогены
Иногда гены считаются псевдогенами, как правило, на основании биоинформатического анализа, но затем оказываются функциональными генами. Примеры включают Дрозофила Цзинвэй ген[37][38] который кодирует функционал алкогольдегидрогеназа фермент in vivo.[39]
Другой пример - человек кодирование генов фосфоглицератмутаза[40] который считался псевдогеном, но оказался функциональным геном,[41] теперь назван PGAM4. Мутации в нем вызывают бесплодие.[42]
Бактериальные псевдогены
Псевдогены находятся в бактерии.[43] Большинство из них содержится в несвободных бактериях; то есть они либо симбионты или же облигатные внутриклеточные паразиты. Таким образом, они не требуют множества генов, которые необходимы свободноживущим бактериям, таких как ген, связанный с метаболизмом и репарацией ДНК. Однако не существует порядка, в котором функционал гены теряются первыми. Например, самые старые псевдогены в Mycobacterium laprae находятся в РНК-полимеразы и биосинтез из вторичные метаболиты в то время как самые старые в Шигелла флекснери и Шигелла тифа находятся в Репликация ДНК, рекомбинация и ремонт.[44]
Поскольку большинство бактерий, несущих псевдогены, являются либо симбионтами, либо облигатными внутриклеточными паразитами, размер генома со временем уменьшается. Ярким примером является геном Mycobacterium leprae, облигатный паразит и возбудитель проказа. Сообщается, что у него 1133 псевдогена, которые дают примерно 50% его транскриптом.[44] Эффект псевдогенов и редукции генома можно еще увидеть по сравнению с Mycobacterium marinum, а возбудитель из той же семьи. Mycobacteirum marinum имеет больший геном по сравнению с Mycobacterium laprae поскольку он может выживать вне хозяина, геном должен содержать гены, необходимые для этого.[45]
Хотя сокращение генома фокусируется на том, какие гены не нужны, избавляясь от псевдогенов, давление отбора со стороны хозяина может повлиять на то, что сохраняется. В случае симбионта из Веррукомикробия phylum существует семь дополнительных копий гена, кодирующего путь манделалида.[46] Хозяин, виды из Lissoclinum, используйте манделалиды как часть его защитного механизма.[46]
Отношения между эпистаз и теория потери генов домино наблюдалась в Buchnera aphidicola. Теория домино предполагает, что если один ген клеточного процесса становится неактивным, то отбор в других вовлеченных генах ослабляется, что приводит к потере гена.[47] При сравнении Buchnera aphidicola и кишечная палочка, было обнаружено, что положительный эпистаз способствует потере генов, а отрицательный - препятствует.
Смотрите также
Рекомендации
- ^ Мигелл А.Дж., Смит Н.Р., Робинсон П.А., Маркхэм А.Ф. (февраль 2000 г.). «Псевдогены позвоночных». Письма FEBS. 468 (2–3): 109–14. Дои:10.1016 / S0014-5793 (00) 01199-6. PMID 10692568. S2CID 42204036.
- ^ ван Барен MJ, Brent MR (май 2006 г.). «Итеративное предсказание генов и удаление псевдогенов улучшает аннотацию генома». Геномные исследования. 16 (5): 678–85. Дои:10.1101 / гр. 4766206. ЧВК 1457044. PMID 16651666.
- ^ Ким, MS; и другие. (2014). «Эскизная карта протеома человека». Природа. 509 (7502): 575–581. Bibcode:2014Натура.509..575K. Дои:10.1038 / природа13302. ЧВК 4403737. PMID 24870542.
- ^ Макс EE (1986). «Плагиат ошибок и молекулярная генетика». Журнал Creation Evolution. 6 (3): 34–46.
- ^ Чандрасекаран К., Бетран Э (2008). «Истоки новых генов и псевдогенов». Природное образование. 1 (1): 181.
- ^ Юрка Дж (декабрь 2004 г.). «Эволюционное влияние повторяющихся элементов Alu человека». Текущее мнение в области генетики и развития. 14 (6): 603–8. Дои:10.1016 / j.gde.2004.08.008. PMID 15531153.
- ^ Деваннье М, Хайдманн Т (2005). «LINE, SINE и обработанные псевдогены: паразитарные стратегии для моделирования генома». Цитогенетические и геномные исследования. 110 (1–4): 35–48. Дои:10.1159/000084936. PMID 16093656. S2CID 25083962.
- ^ Деванье М., Эсно С., Хайдманн Т. (сентябрь 2003 г.). «LINE-опосредованная ретротранспозиция меченых последовательностей Alu». Природа Генетика. 35 (1): 41–8. Дои:10,1038 / ng1223. PMID 12897783. S2CID 32151696.
- ^ Граур Д., Шуали Ю., Ли У.Х. (апрель 1989 г.). «Делеции в обработанных псевдогенах у грызунов накапливаются быстрее, чем у людей». Журнал молекулярной эволюции. 28 (4): 279–85. Bibcode:1989JMolE..28..279G. Дои:10.1007 / BF02103423. PMID 2499684. S2CID 22437436.
- ^ Бэрч Р., Диханс М., Кент В. Дж., Хаусслер Д., Брозиус Дж. (Октябрь 2008 г.). «Вклад ретрокопии в эволюцию генома человека». BMC Genomics. 9: 466. Дои:10.1186/1471-2164-9-466. ЧВК 2584115. PMID 18842134.
- ^ Павличек А., Пейсес Дж., Зика Р., Хейнар Дж. (Октябрь 2002 г.). «Распределение длин длинных вкраплений нуклеотидных элементов (LINE) и обработанных псевдогенов эндогенных ретровирусов человека: последствия для ретротранспозиции и обнаружения псевдогенов». Ген. 300 (1–2): 189–94. Дои:10.1016 / S0378-1119 (02) 01047-8. PMID 12468100.
- ^ ФК Наварро, Галанте, Пенсильвания (июль 2015 г.). «Полногеномный ландшафт ретрокопий в геномах приматов». Геномная биология и эволюция. 7 (8): 2265–75. Дои:10.1093 / gbe / evv142. ЧВК 4558860. PMID 26224704.
- ^ Schrider DR, Navarro FC, Galante PA, Parmigiani RB, Camargo AA, Hahn MW, de Souza SJ (2013-01-24). «Полиморфизм числа копий гена, вызванный ретротранспозицией у людей». PLOS Genetics. 9 (1): e1003242. Дои:10.1371 / journal.pgen.1003242. ЧВК 3554589. PMID 23359205.
- ^ Макс EE (2005-05-05). «Плагиат ошибок и молекулярная генетика». Архив TalkOrigins. Получено 2008-07-22.
- ^ а б Линч М., Конери Дж. С. (ноябрь 2000 г.). «Эволюционная судьба и последствия дублирования генов». Наука. 290 (5494): 1151–5. Bibcode:2000Sci ... 290.1151L. Дои:10.1126 / science.290.5494.1151. PMID 11073452.
- ^ Уолш Дж. Б. (январь 1995 г.). «Как часто дублированные гены развивают новые функции?». Генетика. 139 (1): 421–8. ЧВК 1206338. PMID 7705642.
- ^ Линч М., О'Хели М., Уолш Б., Force A (декабрь 2001 г.). «Вероятность сохранения вновь возникшего дубликата гена». Генетика. 159 (4): 1789–804. ЧВК 1461922. PMID 11779815.
- ^ Харрисон П.М., Хеги Х., Баласубраманиан С., Ласкомб Н.М., Бертон П., Эчолс Н., Джонсон Т., Герштейн М. (февраль 2002 г.). «Молекулярные окаменелости в геноме человека: идентификация и анализ псевдогенов в хромосомах 21 и 22». Геномные исследования. 12 (2): 272–80. Дои:10.1101 / гр.207102. ЧВК 155275. PMID 11827946.
- ^ Чжан Дж (2003). «Эволюция путем дупликации генов: обновление». Тенденции в экологии и эволюции. 18 (6): 292–298. Дои:10.1016 / S0169-5347 (03) 00033-8.
- ^ Нишикими М., Кавай Т., Яги К. (октябрь 1992 г.). «Морские свинки обладают сильно мутированным геном L-гулоно-гамма-лактоноксидазы, ключевого фермента биосинтеза L-аскорбиновой кислоты, отсутствующего у этого вида». Журнал биологической химии. 267 (30): 21967–72. PMID 1400507.
- ^ Нишикими М., Фукуяма Р., Миношима С., Симидзу Н., Яги К. (май 1994 г.). «Клонирование и хромосомное картирование человеческого нефункционального гена L-гулоно-гамма-лактоноксидазы, фермента биосинтеза L-аскорбиновой кислоты, отсутствующего у человека». Журнал биологической химии. 269 (18): 13685–8. PMID 8175804.
- ^ Сюэ И., Дейли А., Ингвадоттир Б., Лю М., Коуп Дж., Ким И., Сабети П., Чен И., Сталкер Дж., Хакл И., Бертон Дж., Леонард С., Роджерс Дж., Тайлер-Смит К. (апрель 2006 г.). «Распространение неактивной формы каспазы-12 у людей связано с недавним положительным отбором». Американский журнал генетики человека. 78 (4): 659–70. Дои:10.1086/503116. ЧВК 1424700. PMID 16532395.
- ^ Zheng D, Frankish A, Baertsch R, Kapranov P, Reymond A, Choo SW, Lu Y, Denoeud F, Antonarakis SE, Snyder M, Ruan Y, Wei CL, Gingeras TR, Guigó R, Harrow J, Gerstein MB (июнь 2007 г. ). «Псевдогены в регионах ENCODE: консенсусная аннотация, анализ транскрипции и эволюции». Геномные исследования. 17 (6): 839–51. Дои:10.1101 / гр.5586307. ЧВК 1891343. PMID 17568002.
- ^ а б Прието-Годино Л.Л., Ритц Р., Барджетон Б., Абуин Л., Аргуэлло Дж. Р., Пераро М. Д., Бентон Р. (ноябрь 2016 г.). «Псевдопсевдогены обонятельных рецепторов». Природа. 539 (7627): 93–97. Bibcode:2016Натура.539 ... 93П. Дои:10.1038 / природа19824. ЧВК 5164928. PMID 27776356.
- ^ Пей Б., Сису С., Франкиш А., Ховальд С., Хабеггер Л., Му XJ, Харт Р., Баласубраманиан С., Танзер А., Диханс М., Реймонд А., Хаббард Т. Дж., Харроу Дж., Герштейн М.Б. (сентябрь 2012 г.). «Псевдогенный ресурс GENCODE». Геномная биология. 13 (9): R51. Дои:10.1186 / gb-2012-13-9-r51. ЧВК 3491395. PMID 22951037.
- ^ Макартур Д.Г., Баласубраманиан С., Франкиш А., Хуанг Н., Моррис Дж., Уолтер К. и др. (Февраль 2012 г.). «Систематический обзор вариантов потери функции в генах, кодирующих белки человека». Наука. 335 (6070): 823–8. Bibcode:2012Sci ... 335..823M. Дои:10.1126 / science.1215040. ЧВК 3299548. PMID 22344438.
- ^ Райт Дж. К., Мадж Дж., Вайссер Х., Барзин М. П., Гонсалес Дж. М., Бразма А., Чоудхари Дж. С., Харроу Дж. (Июнь 2016 г.). «Улучшение аннотации референсного гена GENCODE с использованием высокоточного процесса протеогеномики». Nature Communications. 7: 11778. Bibcode:2016 НатКо ... 711778W. Дои:10.1038 / ncomms11778. ЧВК 4895710. PMID 27250503.
- ^ Чан WL, Чанг JG (2014). «Произведенные из псевдогена эндогенные миРНК и их функции». Псевдогены. Методы молекулярной биологии. 1167. С. 227–39. Дои:10.1007/978-1-4939-0835-6_15. ISBN 978-1-4939-0834-9. PMID 24823781.
- ^ Чан В.Л., Юо Ц.Й., Ян В.К., Хунг С.И., Чанг Ю.С., Чиу С.К., Йе К.Т., Хуанг HD, Чанг Дж.Г. (апрель 2013 г.). «Транскрибируемый псевдоген ψPPM1K генерирует эндогенную миРНК для подавления роста онкогенных клеток в гепатоцеллюлярной карциноме». Исследования нуклеиновых кислот. 41 (6): 3734–47. Дои:10.1093 / nar / gkt047. ЧВК 3616710. PMID 23376929.
- ^ Робертс Т.К., Моррис К.В. (декабрь 2013 г.). «Не так уж и псевдо: псевдогены как терапевтические мишени». Фармакогеномика. 14 (16): 2023–34. Дои:10.2217 / стр.13.172. ЧВК 4068744. PMID 24279857.
- ^ Оловников И., Ле Томас А., Аравин А.А. (2014). «Основа для манипуляции кластером piRNA». PIWI-взаимодействующие РНК. Методы молекулярной биологии. 1093. С. 47–58. Дои:10.1007/978-1-62703-694-8_5. ISBN 978-1-62703-693-1. PMID 24178556.
- ^ Сиоми М.К., Сато К., Пезич Д., Аравин А.А. (апрель 2011 г.). «PIWI-взаимодействующие малые РНК: авангард защиты генома». Обзоры природы Молекулярная клеточная биология. 12 (4): 246–58. Дои:10.1038 / nrm3089. PMID 21427766. S2CID 5710813.
- ^ Karreth FA, Reschke M, Ruocco A, Ng C, Chapuy B, Leopold V, Sjoberg M, Keane TM, Verma A, Ala U, Tay Y, Wu D, Seitzer N, Velasco-Herrera Mdel C, Bothmer A, Fung J , Langellotto F, Rodig SJ, Elemento O, Shipp MA, Adams DJ, Chiarle R, Pandolfi PP (апрель 2015 г.). «Псевдоген BRAF функционирует как конкурентная эндогенная РНК и индуцирует лимфому in vivo». Клетка. 161 (2): 319–32. Дои:10.1016 / j.cell.2015.02.043. ЧВК 6922011. PMID 25843629.
- ^ Дахиа П.Л., Фитцджеральд М.Г., Чжан Х, Марш Д.Д., Чжэн З., Пич Т., фон Даймлинг А., Халуска Ф.Г., Хабер Д.А., Энг С. (май 1998 г.). «Высококонсервативный процессированный псевдоген PTEN расположен на полосе хромосомы 9p21». Онкоген. 16 (18): 2403–6. Дои:10.1038 / sj.onc.1201762. PMID 9620558.
- ^ Полисено Л., Салмена Л., Чжан Дж., Карвер Б., Хавеман В. Дж., Пандольфи П. П. (июнь 2010 г.). «Независимая от кодирования функция мРНК генов и псевдогенов регулирует биологию опухолей». Природа. 465 (7301): 1033–8. Bibcode:2010Натура.465.1033П. Дои:10.1038 / природа09144. ЧВК 3206313. PMID 20577206.
- ^ Балакирев Е.С., Аяла Ф.Дж. (2003). «Псевдогены:« мусор »или функциональная ДНК?». Ежегодный обзор генетики. 37: 123–51. Дои:10.1146 / annurev.genet.37.040103.103949. PMID 14616058.
- ^ Джеффс П., Эшбернер М. (май 1991 г.). «Обработанные псевдогены у дрозофилы». Труды: Биологические науки.. 244 (1310): 151–9. Дои:10.1098 / rspb.1991.0064. PMID 1679549. S2CID 1665885.
- ^ Ван В., Чжан Дж., Альварес К., Ллопарт А, Лонг М. (сентябрь 2000 г.). «Происхождение гена Jingwei и сложная модульная структура его родительского гена, yellow emperor, у Drosophila melanogaster». Молекулярная биология и эволюция. 17 (9): 1294–301. Дои:10.1093 / oxfordjournals.molbev.a026413. PMID 10958846.
- ^ Лонг М., Лэнгли СН (апрель 1993 г.). «Естественный отбор и происхождение jingwei, химерного процессированного функционального гена у Drosophila». Наука. 260 (5104): 91–5. Bibcode:1993Наука ... 260 ... 91Л. Дои:10.1126 / science.7682012. PMID 7682012.
- ^ Диерик Х.А., Мерсер Дж. Ф., Гловер Т.В. (октябрь 1997 г.). «Псевдоген изоформы головного мозга фосфоглицератмутазы (PGAM 1) локализован в гене болезни Менкеса человека (ATP7 A)». Ген. 198 (1–2): 37–41. Дои:10.1016 / s0378-1119 (97) 00289-8. PMID 9370262.
- ^ Бетран Э, Ван В., Джин Л., Лонг М. (май 2002 г.). «Эволюция гена, обработанного фосфоглицератмутазой, у человека и шимпанзе, раскрывающая происхождение нового гена приматов». Молекулярная биология и эволюция. 19 (5): 654–63. Дои:10.1093 / oxfordjournals.molbev.a004124. PMID 11961099.
- ^ Окуда Х., Цудзимура А., Ирие С., Ямамото К., Фукухара С., Мацуока Ю., Такао Т., Миягава И., Нономура Н., Вада М., Танака Х (2012). «Однонуклеотидный полиморфизм в новом сцепленном с полом ретротранспозированном гене PGAM4, связанный с семенником, влияет на мужскую фертильность человека». PLOS ONE. 7 (5): e35195. Bibcode:2012PLoSO ... 735195O. Дои:10.1371 / journal.pone.0035195. ЧВК 3348931. PMID 22590500.
- ^ Goodhead I, Darby AC (февраль 2015 г.). «Извлечение псевдогенов из псевдогенов». Текущее мнение в микробиологии. 23: 102–9. Дои:10.1016 / j.mib.2014.11.012. PMID 25461580.
- ^ а б Даган, Тал; Блехман, Ран; Граур, Дэн (19 октября 2005 г.). "Теория домино" смерти гена: постепенное и массовое исчезновение генов в трех линиях обязательных симбиотических бактериальных патогенов ". Молекулярная биология и эволюция. 23 (2): 310–316. Дои:10.1093 / molbev / msj036. PMID 16237210.
- ^ Мальхотра, Sony; Ведитхи, Сандип Чайтанья; Бланделл, Том Л. (30 августа 2017 г.). «Расшифровка сходства и различий между видами микобактерий». PLOS забытые тропические болезни. 11 (8): e0005883. Дои:10.1371 / journal.pntd.0005883. ЧВК 5595346. PMID 28854187.
- ^ а б Лопера, Хуан; Миллер, Ян Дж; Макфейл, Керри Л.; Кван, Джейсон К. (21 ноября 2017 г.). «Повышенная дозировка биосинтетических генов в защитном бактериальном симбионте с уменьшенным геномом». mSystems. 2 (6): 1–18. Дои:10.1128 / msystems.00096-17. ЧВК 5698493. PMID 29181447.
- ^ Даган, Тал; Блехман, Ран; Граур, Дэн (19 октября 2005 г.). "Теория домино" смерти гена: постепенное и массовое исчезновение генов в трех линиях обязательных симбиотических бактериальных патогенов ". Молекулярная биология и эволюция. 23 (2): 310–316. Дои:10.1093 / molbev / msj036. PMID 16237210.
дальнейшее чтение
- Герштейн М., Чжэн Д. (август 2006 г.). «Реальная жизнь псевдогенов». Scientific American. 295 (2): 48–55. Bibcode:2006SciAm.295b..48G. Дои:10.1038 / scientificamerican0806-48. PMID 16866288.
- Торрентс Д., Суяма М., Здобавов Е., Борк П. (декабрь 2003 г.). «Полногеномный обзор псевдогенов человека». Геномные исследования. 13 (12): 2559–67. Дои:10.1101 / гр.1455503. ЧВК 403797. PMID 14656963.
- Bischof JM, Chiang AP, Scheetz TE, Stone EM, Casavant TL, Sheffield VC, Braun TA (июнь 2006 г.). «Полногеномная идентификация псевдогенов, способных вызывать болезненную конверсию генов». Человеческая мутация. 27 (6): 545–52. Дои:10.1002 / humu.20335. PMID 16671097.