Аминометилфосфоновая кислота - Википедия - Aminomethylphosphonic acid
 | |
| Имена | |
|---|---|
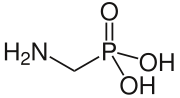
| Название ИЮПАК (Аминометил) фосфоновая кислота | |
| Другие имена Аминометанфосфоновая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| Сокращения | AMPA; AMeP |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.152.014 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| CЧАС6NО3п | |
| Молярная масса | 111.037 г · моль−1 |
| Внешность | Твердый |
| Температура плавления | От 338 до 344 ° C (от 640 до 651 ° F, от 611 до 617 K) |
| Кислотность (пKа) | 0.4 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Аминометилфосфоновая кислота (AMPA) слабый органическая кислота с фосфоновая кислота группа. Это один из основных продуктов разложения гербицид глифосат.[1]AMPA обладает токсичностью, сравнимой с токсичностью глифосата, и поэтому считается, что он имеет такую же токсикологическую ценность (вреден в концентрации более 0,5 частей на миллиард), что и сам глифосат.[2] AMPA может быть разбита на оксид марганца Однако в лабораторных условиях в почве оксид марганца обычно присутствует только в следовых количествах.[3] Микробная деградация AMPA - более вероятный путь деградации, при котором он распадается на фосфорная кислота[4][5] и в конечном итоге углекислый газ и неорганические фосфат.[6]

Структуры AMPA в различных диапазонах pH[7]
Рекомендации
- ^ Экологическая судьба глифосата В архиве 2012-04-20 в Wayback Machine, Джефф Шютт, Департамент регулирования пестицидов, Калифорния
- ^ Остатки пестицидов в продуктах питания - 1997 г., Группа экспертов ФАО по остаткам пестицидов в продуктах питания и окружающей среде и Основная группа оценки ВОЗ
- ^ К. А. Барретт и М. Б. Макбрайд. Окислительное разложение глифосата и аминометилфосфоната оксидом марганца. Environ. Sci. Technol., 2005, 39 (23), с. 9223–9228.
- ^ Pipke R, Amrhein N. (1988) Выделение и характеристика мутанта Arthrobacter sp. штамм GLP-1, который использует гербицид глифосат в качестве единственного источника фосфора и азота. Прикладная и экологическая микробиология 54 (11): 2868-2870.
- ^ Форлани Г., Манджиагалли А., Нильсен Э., Суарди К.М. (1999) Разложение глифосата фосфонатного гербицида в почве: данные о возможном участии некультивируемых микроорганизмов. Биология и биохимия почвы 31: 991-997
- ^ Справочная информация: глифосат не разлагается до фосфористой кислоты в окружающей среде. Монсанто. 2005 г.
- ^ Зулианг Чен, Вэньсян Хе, Майкл Бир, Маллаварапу Мегарадж, Равендра Найду (15 мая 2009 г.). «Определение глифосата, фосфата и аминометилфосфоновой кислоты в почвенных экстрактах с помощью ионной хроматографии с масс-спектрометрией с индуктивно связанной плазмой с октопольной реакционной системой». Таланта. 78 (3): 852. Дои:10.1016 / j.talanta.2008.12.052.CS1 maint: несколько имен: список авторов (связь)
