Денитрификация - Denitrification
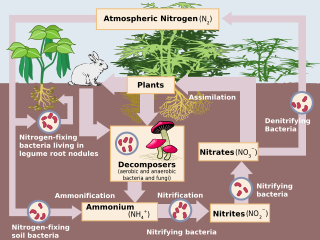
Денитрификация это микробиологический процесс, в котором нитрат (NO3−) уменьшается и в конечном итоге производит молекулярные азот (N2) через ряд промежуточных газообразных продуктов оксида азота. Факультативные анаэробные бактерии выполняют денитрификацию как тип дыхания, уменьшает окисленные формы азота в ответ на окисление донор электронов Такие как органическая материя. Предпочтительный азот акцепторы электронов в порядке от наиболее до наименее термодинамически благоприятных включают нитрат (НЕТ3−), нитрит (НЕТ2−), оксид азота (НЕТ), оксид азота (N2O), в конечном итоге приводя к производству диазот (N2) завершение азотный цикл. Денитрифицирующие микробы требуют очень низкой концентрации кислорода менее 10%, а также органический C для энергии. Поскольку денитрификация может удалить NO3−, уменьшая ее выщелачивание до грунтовых вод, его можно стратегически использовать для очистки сточных вод или остатков животных с высоким содержанием азота. Денитрификация может привести к утечке азота2O, который является озоноразрушающее вещество и парниковый газ которые могут иметь значительное влияние на глобальное потепление.
Процесс выполняется в первую очередь гетеротрофный бактерии (Такие как Paracoccus denitrificans и различные псевдомонады ),[1] хотя также были идентифицированы автотрофные денитрификаторы (например, Тиобациллы денитрификаторы).[2] Денитрификаторы представлены во всех основных филогенетических группах.[3] Обычно несколько видов бактерий участвуют в полном восстановлении нитратов до азота.2, и в процессе восстановления было идентифицировано более одного ферментативного пути.[4]
Прямое восстановление от нитратов до аммоний, процесс, известный как диссимиляционное восстановление нитрата до аммония или же DNRA,[5] также возможно для организмов, у которых есть nrf-ген.[6][7] Это менее распространено, чем денитрификация в большинстве экосистем как средство снижения содержания нитратов. Другие гены, известные у денитрифицирующих микроорганизмов, включают: нир (нитритредуктаза) и нет (закись азота редуктаза) среди других;[3] организмы, идентифицированные как имеющие эти гены, включают Alcaligenes faecalis, Alcaligenes xylosoxidans, многие в роду Псевдомонады, Bradyrhizobium japonicum, и Blastobacter denitrificans.[8]
Обзор
Половина реакции
Денитрификация обычно протекает через некоторую комбинацию следующих полуреакций, при этом фермент, катализирующий реакцию, указан в скобках:
- НЕТ3− + 2 часа+ + 2 е−→ НЕТ
2− + H2O (нитратредуктаза) - НЕТ
2− + 2 часа+ + е− → NO + H2O (нитритредуктаза) - 2 НО + 2 ч+ + 2 е− → N
2О + H2O (редуктаза оксида азота) - N
2О + 2 часа+ + 2 е− → N
2 + H2O (редуктаза закиси азота)
Полный процесс может быть выражен как чистая сбалансированная редокс реакция, где нитрат (НЕТ3−) полностью сводится к диазот (N2):
- 2 НЕТ3− + 10 e− + 12 часов+ → N2 + 6 часов2О
Условия денитрификации
В природе денитрификация может происходить как на суше, так и на море. экосистемы.[9] Обычно денитрификация происходит в бескислородной среде, где концентрация растворенного и свободно доступного кислорода снижена. В этих областях нитрат (NO3−) или нитрит (НЕТ
2−) можно использовать в качестве замены терминального акцептора электронов вместо кислород (O2), более энергетически выгодный акцептор электронов. Терминальный акцептор электронов - это соединение, которое восстанавливается в реакции за счет получения электронов. Примеры бескислородных сред могут включать: почвы,[10] грунтовые воды,[11] водно-болотные угодья, нефтяные резервуары,[12] плохо вентилируемые уголки океана и донные отложения.
Кроме того, денитрификация может происходить и в кислородной среде. Высокая активность денитрификаторов наблюдается в приливных зонах, где приливные циклы вызывают колебания концентрации кислорода в песчаных прибрежных отложениях.[13] Например, бактериальные виды Paracoccus denitrificans участвует в денитрификации одновременно в кислородных и аноксических условиях. Под воздействием кислорода бактерии могут использовать редуктаза закиси азота, фермент, катализирующий последнюю стадию денитрификации.[14] Аэробные денитрификаторы - это в основном грамотрицательные бактерии, относящиеся к типу Proteobacteria. Ферменты NapAB, NirS, NirK и NosZ расположены в периплазме, широком пространстве, ограниченном цитоплазмой и внешней мембраной у грамотрицательных бактерий.[15]
Денитрификация может привести к состоянию, называемому изотопное фракционирование в почвенной среде. Два стабильных изотопа азота, 14N и 15Оба N присутствуют в профилях отложений. Более легкий изотоп азота, 14N является предпочтительным во время денитрификации, оставляя более тяжелый изотоп азота, 15N в остаточном веществе. Эта селективность приводит к обогащению 14N в биомассе по сравнению с 15Н.[16] Более того, относительное обилие 14N можно анализировать, чтобы отличить денитрификацию от других процессов в природе.
Использование при очистке сточных вод
Денитрификация обычно используется для удаления азота из сточные воды и муниципальные Сточные Воды. Это также инструментальный процесс в построенные водно-болотные угодья[17] и прибрежный зоны[18] для предотвращения загрязнение подземных вод с нитратами в результате чрезмерного использования в сельскохозяйственных или жилых удобрение использование.[19]Биореакторы на древесной стружке изучаются с 2000-х годов и эффективно удаляют нитраты из сельскохозяйственных стоков[20] и даже навоз.[21]
Восстановление в бескислородных условиях также может происходить посредством процесса, называемого анаэробным окислением аммония (анаммокс ):[22]
- NH4+ + НЕТ2− → N2 + 2 часа2О
В некоторых очистные сооружения сточных вод, соединения, такие как метанол, этиловый спирт, ацетат, глицерин, или патентованные продукты добавляются в сточные воды, чтобы обеспечить источник углерода и электронов для денитрифицирующих бактерий.[23] Микробная экология таких искусственно созданных процессов денитрификации определяется природой донора электронов и рабочими условиями процесса.[24][25] Процессы денитрификации также используются при лечении промышленные сточные воды.[26] Многие типы и конструкции денитрифицирующих биореакторов коммерчески доступны для промышленного применения, в том числе Электро-биохимические реакторы (ЭБР), мембранные биореакторы (MBR) и биореакторы с подвижным слоем (MBBR).
Аэробная денитрификация, проводимая аэробными денитрификаторами, может дать возможность устранить необходимость в отдельных резервуарах и снизить выход ила. Существуют менее строгие требования к щелочности, поскольку щелочность, образующаяся во время денитрификации, может частично компенсировать потребление щелочности при нитрификации.[15]
Смотрите также
- Аэробная денитрификация
- Анаэробное дыхание
- Биоремедиация
- Изменение климата
- Гипоксия (экологическая)
- Фиксация азота
- Одновременная нитрификация-денитрификация
Рекомендации
- ^ Carlson, C.A .; Ингрэм, Дж. Л. (1983). "Сравнение денитрификации Pseudomonas stutzeri, Синегнойная палочка, и Paracoccus denitrificans". Appl. Environ. Микробиол. 45 (4): 1247–1253. Дои:10.1128 / AEM.45.4.1247-1253.1983. ЧВК 242446. PMID 6407395.
- ^ Baalsrud, K .; Баальсруд, Кьеллрун С. (1954). "Исследования по Thiobacillus denitrificans". Archiv für Mikrobiologie. 20 (1): 34–62. Дои:10.1007 / BF00412265. PMID 13139524. S2CID 22428082.
- ^ а б Zumft, W.G. (1997). «Клеточная биология и молекулярные основы денитрификации». Обзоры микробиологии и молекулярной биологии. 61 (4): 533–616. Дои:10.1128/.61.4.533-616.1997. ЧВК 232623. PMID 9409151.
- ^ Атлас, Р.М., Бартас, Р. Экология микробов: основы и приложения. 3-е изд. Бенджамин-Каммингс Паблишинг. ISBN 0-8053-0653-6
- ^ An, S .; Гарднер, WS (2002). «Диссимиляционное восстановление нитратов до аммония (DNRA) как азотного звена по сравнению с денитрификацией как сток в мелководном устье (Лагуна Мадре / Баффинова залив, Техас)». Серия "Прогресс морской экологии". 237: 41–50. Bibcode:2002MEPS..237 ... 41A. Дои:10,3354 / meps237041.
- ^ Кайперс, МММ; Маршан, Гонконг; Картал, Б (2011). "Сеть микробного цикла азота". Обзоры природы Микробиология. 1 (1): 1–14. Дои:10.1038 / nrmicro.2018.9. PMID 29398704. S2CID 3948918.
- ^ Спэннинг, Р., Дельгадо, М. и Ричардсон, Д. (2005). «Азотный цикл: денитрификация и ее связь с N2 Установка ». Фиксация азота: происхождение, применение и результаты исследований. С. 277–342. Дои:10.1007/1-4020-3544-6_13. ISBN 978-1-4020-3542-5.
Можно встретить DNRA, когда источником углерода является ферментируемый субстрат, например глюкоза, поэтому, если вы хотите избежать DNRA, используйте неферментируемый субстрат.
CS1 maint: несколько имен: список авторов (связь) - ^ Лю, X .; Tiquia, S.M .; Ольгин, Г .; Wu, L .; Nold, S.C .; Devol, A.H .; Луо, К .; Palumbo, A. V .; Tiedje, J.M .; Чжоу, Дж. (2003). «Молекулярное разнообразие денитрифицирующих генов в континентальных отложениях в кислородно-дефицитной зоне у тихоокеанского побережья Мексики». Appl. Environ. Микробиол. 69 (6): 3549–3560. CiteSeerX 10.1.1.328.2951. Дои:10.1128 / aem.69.6.3549-3560.2003. ЧВК 161474. PMID 12788762.
- ^ Зейтцингер, S .; Харрисон, Дж. А .; Bohlke, J. K .; Боуман, А. Ф .; Lowrance, R .; Петерсон, Б .; Tobias, C .; Дрехт, Г. В. (2006). "Денитрификация ландшафтов и водных ландшафтов: синтез". Экологические приложения. 16 (6): 2064–2090. Дои:10.1890 / 1051-0761 (2006) 016 [2064: dalawa] 2.0.co; 2. HDL:1912/4707. PMID 17205890.
- ^ Scaglia, J .; Lensi, R .; Шаламе, А. (1985). «Взаимосвязь между фотосинтезом и денитрификацией в посевной почве». Растение и почва. 84 (1): 37–43. Дои:10.1007 / BF02197865. S2CID 20602996.
- ^ Кором, Скотт Ф. (1992). «Естественная денитрификация в насыщенной зоне: обзор». Исследование водных ресурсов. 28 (6): 1657–1668. Bibcode:1992WRR .... 28.1657K. Дои:10.1029 / 92WR00252.
- ^ Корнуолл Шартау, С. Л .; Юркив, М .; Lin, S .; Григорян, А. А .; Lambo, A .; Park, H. S .; Lomans, B.P .; Van Der Biezen, E .; Jetten, M. S. M .; Воордоу, Г. (2010). «Концентрации аммония в добываемых водах мезотермического нефтяного месторождения, подвергнутого закачке нитратов, снижаются за счет образования денитрифицирующей биомассы и активности анаммокса». Прикладная и экологическая микробиология. 76 (15): 4977–4987. Дои:10.1128 / AEM.00596-10. ЧВК 2916462. PMID 20562276.
- ^ Торговец; и другие. (2017). «Денитрифицирующее сообщество в прибрежных отложениях одновременно выполняет аэробное и анаэробное дыхание». Журнал ISME. 11 (8): 1799–1812. Дои:10.1038 / ismej.2017.51. ЧВК 5520038. PMID 28463234.
- ^ Qu; и другие. (2016). «Транскрипционная и метаболическая регуляция денитрификации у Paracoccus denitrificans допускает низкую, но значительную активность редуктазы закиси азота в кислородных условиях». Экологическая микробиология. 18 (9): 2951–63. Дои:10.1111/1462-2920.13128. PMID 26568281.
- ^ а б Джи, Бин; Ян, Кай; Чжу, Лэй; Цзян Юй; Ван, Хунъюй; Чжоу, Цзюнь; Чжан, Хуининг (2015). «Аэробная денитрификация: обзор важных достижений последних 30 лет». Биотехнология и биотехнология. 20 (4): 643–651. Дои:10.1007 / s12257-015-0009-0. S2CID 85744076.
- ^ Dähnke K .; Тамдруп Б. (2013). «Динамика изотопов азота и фракционирование во время денитрификации осадка в Бокнис Экк, Балтийское море». Биогеонауки. 10 (5): 3079–3088. Bibcode:2013BGeo ... 10.3079D. Дои:10.5194 / bg-10-3079-2013 - через Copernicus Publications.
- ^ Bachand, P.A.M .; Хорн, А. Дж. (1999). «Денитрификация в водно-болотных угодьях со свободной водой: II. Влияние растительности и температуры». Экологическая инженерия. 14 (1–2): 17–32. Дои:10.1016 / s0925-8574 (99) 00017-8.
- ^ Martin, T. L .; Кошик, Н. К .; Trevors, J. T .; Уайтли, Х. Р. (1999). «Обзор: Денитрификация в прибрежных зонах умеренного климата». Загрязнение воды, воздуха и почвы. 111: 171–186. Bibcode:1999WASP..111..171M. Дои:10.1023 / а: 1005015400607. S2CID 96384737.
- ^ Mulvaney, R.L .; Хан, С. А .; Mulvaney, C. S. (1997). «Азотные удобрения способствуют денитрификации». Биология и плодородие почв. 24 (2): 211–220. Дои:10.1007 / s003740050233. S2CID 18518.
- ^ Ghane, E; Fausey, NR; Браун, LC (январь 2015 г.). «Моделирование удаления нитратов в денитрификационном слое». Вода Res. 71C: 294–305. Дои:10.1016 / j.watres.2014.10.039. PMID 25638338. (требуется подписка)
- ^ Карни К.Н., Роджерс М; Лоулор, PG; Жан, X (2013). «Обработка отделенного жидкого анаэробного дигестата свиноводства с использованием биофильтров из щепы». Технология Environ. 34 (5–8): 663–70. Дои:10.1080/09593330.2012.710408. PMID 23837316. S2CID 10397713. (требуется подписка)
- ^ Dalsgaard, T .; Thamdrup, B .; Кэнфилд, Д. Э. (2005). «Анаэробное окисление аммония (анаммокс) в морской среде». Исследования в области микробиологии. 156 (4): 457–464. Дои:10.1016 / j.resmic.2005.01.011. PMID 15862442.
- ^ Chen, K.-C .; Линь, Ю.-Ф. (1993). «Взаимосвязь между денитрифицирующими бактериями и метаногенными бактериями в системе смешанной культуры акклиматизированных илов». Водные исследования. 27 (12): 1749–1759. Дои:10.1016 / 0043-1354 (93) 90113-в.
- ^ Байтшток, Владимир; Лу, Хуэйцзе; Парк, Хункын; Ким, Сонгпё; Ю, Ран; Чандран, Картик (15 апреля 2009 г.). «Влияние различных доноров электронов на молекулярную микробную экологию и биокинетику метилотрофных денитрифицирующих бактерий». Биотехнологии и биоинженерия. 102 (6): 1527–1536. Дои:10.1002 / бит. 22213. PMID 19097144. S2CID 6445650.
- ^ Лу, Хуэйцзе; Чандран, Картик; Стенсел, Дэвид (ноябрь 2014 г.). «Микробная экология денитрификации при биологической очистке сточных вод». Водные исследования. 64: 237–254. Дои:10.1016 / j.watres.2014.06.042. PMID 25078442.
- ^ Константин, H .; Фик, М. (1997). «Влияние источников углерода на скорость денитрификации промышленных сточных вод с высокой концентрацией нитратов». Водные исследования. 31 (3): 583–589. Дои:10.1016 / с0043-1354 (96) 00268-0.
