Диоксины и диоксиноподобные соединения - Dioxins and dioxin-like compounds
Диоксины и диоксиноподобные соединения (DLC) являются группой химические соединения которые настойчивы экологический загрязняющие вещества (СОЗ). Некоторые из них очень токсичны, но токсичность среди них варьируется в 30 000 раз. Они сгруппированы вместе, потому что механизм их действия одинаков. Они активируют рецептор арильных углеводородов (Рецептор AH), хотя и с очень разными аффинностями связывания, что приводит к большим различиям в токсичности и других эффектах. В основном это побочные продукты горения или различных промышленных процессов - или, в случае диоксиноподобных веществ. Печатные платы и ПБД, нежелательные второстепенные компоненты намеренно произведенных смесей.[1][2] Они включают:[1][3][4]
- Полихлорированный дибензо-п-диоксины (ПХДД) или просто диоксины. ПХДД являются производными дибензо-п-диоксин. Всего 75 PCDD сородичи, различающихся количеством и расположением атомов хлора, причем 7 из них являются специфически токсичными, наиболее токсичным из которых является 2,3,7,8-тетрахлордибензодиоксин (TCDD).
- Полихлорированные дибензофураны (ПХДФ) или фураны. ПХДФ являются производными дибензофуран. Всего 135 изомеров; 10 обладают диоксиноподобными свойствами.
- Полихлорированные бифенилы (ПХБ), полученные из бифенил, из которых 12 являются «диоксиноподобными». При определенных условиях ПХД могут образовывать дибензофураны в результате частичного окисления.
- Полибромированные соединения вышеперечисленных классов могут иметь аналогичные эффекты.
- Диоксин может относиться к 1,4-диоксин или п-диоксин, основная химическая единица более сложных диоксинов. Это простое соединение не является стойким и не имеет токсичности, подобной ПХДД.
Диоксины обладают разной токсичностью в зависимости от количества и положения хлор атомы. Поскольку диоксины относятся к такому широкому классу соединений, которые широко различаются по токсичности, концепция коэффициент токсической эквивалентности (TEF) был разработан для облегчения оценки рисков и нормативного контроля. TEF существуют для семи сородичи диоксинов, десяти фуранов и двенадцати ПХБ. Эталонный конгенер представляет собой наиболее токсичный диоксин TCDD, который по определению имеет TEF, равный единице.[5] По сути, умножение количества конкретного конгенера на его TEF дает количество токсикологически эквивалентное TCDD, и после этого преобразования все диоксиноподобные конгенеры могут быть суммированы, и полученное количество эквивалента токсичности (TEQ) дает приблизительное значение токсичности смесь измеряется как TCDD.
Диоксины практически не растворимы в воде, но обладают относительно высокой растворимостью в липиды. Следовательно, они имеют тенденцию ассоциироваться с органическими веществами, такими как планктон, листья растений и животный жир. Кроме того, они имеют тенденцию адсорбироваться неорганическими частицами, такими как зола и почва.[6]
Диоксины чрезвычайно стабильны и, следовательно, имеют тенденцию накапливаться в пищевая цепочка. Они очень медленно выводятся из организма животных, например Период полураспада TCDD у человека составляет от 7 до 9 лет.[4][7][8] Об инцидентах загрязнения ПХД часто сообщают как случаи заражения диоксином поскольку они вызывают наибольшую озабоченность общественности и регулирующих органов.[9][1]
Химия
Существует 75 возможных конгенеров полихлорированного дибензо-п-диоксины, но только 7 из них имеют сродство к рецептору AH и токсичны по этому механизму. Важнейшими структурами являются так называемые боковые хлорины в положениях 2, 3, 7 и 8. Эти 4 хлора также делают конгенеры устойчивыми, поскольку они предотвращают микробную деградацию. Дополнительный хлор снижает эффективность соединений, но в основном эффекты остаются такими же, хотя и при более высоких дозах. Существует 135 возможных дибензофуранов и 10, в которых боковые хлорины являются диоксиноподобными.[5]

Всего 209 соединений ПХБ. Аналогично PCDD, по крайней мере, два боковых хлора в каждом кольце в положениях 3, 4 и / или 5 необходимы для диоксиноподобной активности. Поскольку рецептор AH требует плоской (плоской) структуры, только те конгенеры PCB, которые могут свободно вращаться вдоль оси C-C между кольцами, могут присоединяться к рецептору. Заместители в орто-положениях 2 и 6 предотвращают вращение и, таким образом, мешают молекуле занять плоское положение. Моно-орто конгенеры (один Cl в 2, 2 ', 6 или 6') обладают минимальной активностью. Не было замечено значительных диоксиноподобных активностей, если присутствуют два или более о-хлора.[5] Бромированные диоксины и бифенилы обладают схожими свойствами, но они изучены гораздо меньше.[5]

Многие природные соединения обладают очень высоким сродством к рецепторам AH. К ним относятся индолы, флавоны, бензофлавоны, имидазолы и пиридины.[10][1] Эти соединения быстро метаболизируются, но постоянное поступление с пищей может вызвать активацию рецепторов, аналогичную фоновым уровням диоксинов.[11] Однако они не достигают концентраций, вызывающих типичную диоксиноподобную токсичность.
Механизм действия
Рецептор AH - это древний рецептор, многие функции которого были обнаружены только недавно.[12][13][14] Это белок возрастом более 600 миллионов лет, встречающийся у всех позвоночных, и его гомологи были обнаружены у беспозвоночных и насекомых. Это принадлежит базовый Helix-Loop-Helix -PAS белки и действует как фактор транскрипции, модифицирующий транскрипцию ряда генов (см. Рисунок).[15][16] Активность рецепторов АГ необходима для нормального развития и многих физиологических функций. Мыши, у которых отсутствует рецептор AH (нокаут), болеют гипертрофией сердца, фиброзом печени, репродуктивными проблемами и нарушением иммунологии.[1]

Рецептор AH важен в токсикологии по двум очень разным причинам. Во-первых, он индуцирует несколько ферментов, важных для метаболизма чужеродных веществ, так называемых ксенобиотики. К ним относятся как окислительные ферменты фазы I, так и конъюгативные ферменты фазы II, например CYP 1A2, CYP1B1, CYP2S1, CYP2A5, ALDH3, GSTA1, UGT1A1, UGT1A6, UGT1A7 и NQO1.[17] По сути, это защитная функция, предотвращающая токсические или канцерогенные эффекты ксенобиотиков, но в некоторых условиях она также может приводить к образованию реактивных метаболитов, которые являются мутагенными и канцерогенными. Эта индукция фермента может быть инициирована многими природными или синтетическими соединениями, например, канцерогенный полициклические углеводороды, такие как бензо(а)пирен,[17] несколько природных соединений,[10] и диоксины.[1] Во-вторых, рецепторы AH участвуют в активации или заглушении генов, что приводит к токсическим эффектам высоких доз диоксинов.[1] Поскольку TCDD в высоких дозах может влиять на транскрипцию, возможно, сотен генов, гены, имеющие решающее значение для множества токсических эффектов диоксинов, все еще не очень хорошо известны.[18]
Связывание диоксиноподобных соединений с рецептором AH позволило измерить общую диоксиноподобную активность образца с использованием CALUX (Экспрессия гена химически активированной люциферазы) биотест. Результаты были сопоставимы с уровнями TEQ, измеренными с помощью гораздо более дорогостоящей газовой хроматографии с масс-спектрометрией высокого разрешения в пробах окружающей среды.[19]
Токсичность
Токсичность диоксина основана на неправильной активации физиологически важного рецептора, и поэтому необходимо тщательно учитывать дозозависимость.[1] Неправильная стимуляция многих рецепторов приводит к токсическим последствиям, например передозировка витамин А приводит к неправильной активации ретиноидные рецепторы в результате, например, пороки развития и передозировки кортикостероиды или половые гормоны приводят к множеству побочных эффектов. Следовательно, важно отделить эффекты низких доз, вызывающих активацию рецептора в физиологическом диапазоне, от эффектов высоких токсичных доз. Это тем более важно из-за больших различий в экспозиции даже среди людей. Сегодня западное население подвергается воздействию диоксинов в дозах, ведущих к концентрации от 5 до 100 пикограмм / г (как ТЭ в теле), а самые высокие концентрации при случайных или преднамеренных отравлениях составляют от 10 000 до 144 000 пг / г, что приводит к серьезным, но не смертельным последствиям. результаты.[1]
Наиболее значимыми токсическими последствиями воздействия диоксинов для человека и животных являются рак и последствия для развития потомства. Оба были зарегистрированы в высоких дозах, наиболее точно в экспериментах на животных. Что касается эффектов развития, существует согласие, что нынешние уровни диоксинов во многих популяциях не очень далеки от тех, которые вызывают некоторые эффекты, но пока нет единого мнения о безопасном уровне.[1][20] Что касается рака, то существуют разногласия относительно того, как экстраполировать риск от высоких токсичных доз на нынешнее низкое воздействие.[1]
Хотя сродство диоксинов и связанных с ними промышленных токсичных веществ к рецептору Ah не может полностью объяснить все их токсические эффекты, включая иммунотоксичность, эндокринный эффекты и продвижение опухоли токсические реакции, по-видимому, обычно зависят от дозы в определенных диапазонах концентраций. Многофазный доза-реакция также сообщалось, что приводит к неуверенности и спорам об истинной роли диоксинов в заболеваемости раком.[21] Считается, что эндокринная разрушающая активность диоксинов возникает как нисходящая функция активации рецепторов АГ, причем статус щитовидной железы, в частности, является чувствительным маркером воздействия. TCDD, наряду с другими PCDD, PCDF и диоксиноподобными копланарными PCB, не являются прямыми агонистами или антагонистами гормонов и не активны в анализах, которые непосредственно проверяют эти активности, например ER-CALUX и AR-CALUX. Эти соединения также не имеют прямого мутагенный или генотоксичный Мероприятия.[22] Их основное действие в возникновении рака - развитие рака. Смесь печатных плат, таких как Ароклор могут содержать соединения ПХД, которые известны агонисты эстрогенов но не классифицируются как диоксиноподобные с точки зрения токсичности. Мутагенные эффекты были установлены для некоторых химикатов с низким содержанием хлора, таких как 3-хлордибензофуран, который не является стойким и не агонистом рецепторов АГ.[23]
Токсичность для животных
Высокие дозы. Симптомы, которые, как сообщается, связаны с токсичностью диоксина в исследованиях на животных, невероятно разнообразны как по объему пораженных биологических систем, так и по диапазону доз, необходимых для их появления.[4][1][3] Острые эффекты однократного воздействия высоких доз диоксина включают снижение потребления корма и синдром истощения и, как правило, отсроченная смерть животного через 1-6 недель.[16] Безусловно, большинство исследований токсичности было выполнено с использованием 2,3,7,8-тетрахлордибензо-п-диоксин.
В LD50 TCDD сильно различается между видами и даже штаммами одного и того же вида, причем наиболее заметное различие наблюдается между внешне похожими видами хомяк и морская свинка. Устный LD50 для морских свинок составляет от 0,5 до 2 мкг / кг массы тела, тогда как пероральный LD50 для хомяков может достигать от 1 до 5 мг / кг массы тела.[4] Даже между разными линиями мышей или крыс острая токсичность может отличаться от десяти до тысячи раз. Многие патологические находки видны в печень, вилочковая железа и другие органы. Некоторые эффекты, такие как атрофия тимуса, характерны для многих видов, но, например, печеночная токсичность характерна для кроликов.[4]
Низкие дозы. У взрослых животных после приема низких доз выявляется очень мало признаков токсичности, но при низких уровнях диоксина могут наблюдаться эффекты развития, в том числе плод, неонатальный, и, возможно, стадии полового созревания.[24] Хорошо известные эффекты развития волчья пасть, гидронефроз, нарушения в развитие зубов и половое развитие а также эндокринный эффекты.[24] Удивительно, но индукция ферментов, некоторые эффекты развития и отвращение к новым продуктам питания наблюдаются при одинаковых уровнях доз у животных, которые по-разному реагируют на острую токсичность в высоких дозах. Поэтому было предложено разделить эффекты диоксина на эффекты типа I (индукция ферментов и т. Д.) И эффекты типа II (летальность, повреждение печени, анорексия и развитие опухоли).[1] Причина может заключаться в различных требованиях к структуре домена трансактивации рецептора AH для разных генов. Некоторые из этих эффектов низких доз на самом деле можно интерпретировать как защитные, а не токсические (индукция ферментов, отвращение к новым продуктам).[1]
Человеческая токсичность
Высокие дозы. Токсичность диоксинов в высоких дозах была хорошо задокументирована после аварий, умышленных отравлений, эпизодов заражения пищевых продуктов и высоких промышленных воздействий.[1][25] Три женщины в Вене, Австрия, были отравлены большими дозами ТХДД в 1998 году. Самая высокая концентрация ТХДД в жировой ткани составила 144 000 пг / г, что является самым высоким показателем среди людей. Главной особенностью было хлоракне, серьезное кожное заболевание. Жертва выжила, и другие симптомы были умеренными после первоначального желудочно-кишечный симптомы и аменорея.[26] Еще один острый инцидент - умышленное отравление Виктор Ющенко, тогдашний кандидат в президенты Украины, в 2004 году. Концентрация ТХДД в жире составляла 108 000 пг / г. Также в этом случае наиболее заметным симптомом было хлоракне после начальной боли в животе, указывающей на гепатит и панкреатит.[27] Эти эпизоды показывают, что человек не так чувствителен, как наиболее чувствительные животные, поскольку дозы должны быть до 25 мкг / кг.
Две серьезные аварии с загрязнением пищевых продуктов были вызваны ПХБ-маслами, используемыми в теплообменниках.[1] Масло ПХБ просочилось в масло из рисовых отрубей, которое потребляют тысячи людей в Японии (Болезнь Юшо 1968) и Тайвань (Болезнь Юй-чэн 1979). Токсические эффекты приписываются диоксиноподобным ПХБ и ПХДФ. Их ежедневное потребление было в 100 000 раз выше среднего в настоящее время.[1] Было много проблем с кожей, хлоракне, отек век и гиперсекреция Мейбомиевые железы в глазах. Младенцы, рожденные матерями Юшо и Ю-чэн, были меньше нормального размера, у них была темная пигментация, а иногда и зубы при рождении и деформации зубов. Смерть плода и выкидыши были обычным явлением.[28]
Возможно, самая известная авария с диоксином произошла в Севезо, Италия, в 1976 году. хлорфенолы выпустил в воздух его содержимое, в том числе многие килограммы TCDD, и загрязнило большую часть города. Самые высокие уровни ТХДД были обнаружены у детей - до 56 000 пг / г жира. Острые эффекты были ограничены хлоракне, хотя многие животные, такие как кролики, погибли после употребления в пищу зараженной травы.[29] Зубные аберрации были обнаружены через 25 лет у лиц, подвергшихся облучению в детстве, а через 35 лет был подтвержден незначительный повышенный риск рака.[1]
Согласно исследованиям на животных, влияние на развитие может быть намного более важным, чем воздействие на взрослых. К ним относятся нарушения зуб развитие,[30] и полового развития.[31]
Пример вариации ответов четко прослеживается в исследовании, проведенном после Катастрофа Севезо указывая, что сперма количество и подвижность подвергались различным воздействиям у мужчин, подвергшихся воздействию, в зависимости от того, подвергались ли они воздействию до, во время или после полового созревания.[32]
В производственных условиях наблюдались многие симптомы, но всегда было воздействие множества химических веществ, включая хлорфенолы, гербициды хлорфеноксикислоты, и растворители. Таким образом, было трудно получить окончательные доказательства того, что диоксины являются причинными факторами. Безусловно, лучший доказанный эффект - хлоракне. Предполагаемые эффекты у взрослых - это повреждение печени и изменения в гем метаболизм, сыворотка липид уровни щитовидная железа функции, а также сахарный диабет и иммунологические эффекты.[29]
Низкие выдержки. Эффекты после слабого воздействия, например, от еды, трудно доказать. Уровни диоксинов у современного населения составляют от 5 до 20 пг / г (ТЭ в жире) и от 50 до 100 пг у пожилых людей.[33][34] или как минимум в 1000 раз ниже, чем при отравлениях (см. выше). Деформации зубов считались вероятными после длительного кормления грудью, когда концентрации диоксинов были высокими в 1970-х и 1980-х годах.[35] Когда концентрации снизились в течение 1990-х и 2000-х годов, эффекты больше не наблюдались.[1] Согласно исследованию, проведенному в России, количество сперматозоидов у молодых мужчин 18-19 лет было ниже, когда уровень диоксина был выше в возрасте от 8 до 9 лет.[36] Это произошло в промышленных условиях, в результате чего мальчики и их матери подверглись относительно высокому воздействию.[1] Панель загрязнения Европейское агентство по безопасности пищевых продуктов (EFSA) рекомендовал уменьшить допустимое недельное потребление (TWI) уровни на основе исследования российских детей.[20] Эта рекомендация может быть оспорена, поскольку она не учитывает должным образом конкурирующие риски, связанные с упущенной пользой от важных и здоровых продуктов питания, таких как определенная рыба.[1] Уровни TWI не применяются для грудного вскармливания, поскольку считается, что польза от грудного молока гораздо более важна, чем отдаленные риски диоксинов.[37] Общий вывод может заключаться в том, что пределы безопасности не очень велики в отношении эффектов развития, но токсические эффекты маловероятны при нынешних уровнях диоксинов в популяции.
Количество поперечные исследования показали ассоциации между диабет 2 типа и несколько соединений СОЗ, включая диоксины.[38] Такие наблюдательные исследования не могут доказать причинно-следственную связь, т.е. может существовать ассоциация, которая не доказывает, что одно является причиной другого. Основная проблема в том, что похожие ассоциации можно найти со многими совершенно разными СОЗ, которые имеют только период полураспада и тенденция к общему накоплению в липидах. Это говорит о том, что все они могут быть связаны с диетой и ожирением, которые на сегодняшний день являются наиболее частыми причинами диабета 2 типа.[1]
На протяжении многих лет высказывались предположения о различных эффектах диоксинов на эндометриоз, половое развитие, функция печени, гормон щитовидной железы уровни лейкоцит уровни невосприимчивый функции, и даже обучение и интеллект. Хотя некоторые из этих эффектов могут быть возможны после сильного воздействия (например, во время катастрофы в Севезо), эти утверждения основаны только на потенциальных воздействиях на население, а не на фактических измерениях концентраций диоксинов.[29] Например. абсорбция из отбеленных тампонов, предположительно связанная с эндометриозом[39] незначительно по сравнению с дневным поступлением диоксина с пищей.[33]
Канцерогенность
Диоксины хорошо известны канцерогены в исследованиях на животных, хотя точный механизм не ясен. Диоксины не являются мутагенный или генотоксичный.[1][22][40] В Агентство по охране окружающей среды США классифицировал диоксин и смесь веществ, связанных с источниками токсичности диоксина, как «вероятный канцероген для человека».[41] В Международное агентство по изучению рака классифицировал TCDD как канцероген для человека (класс 1) на основании очевидной канцерогенности для животных и ограниченных данных о людях,[42] а затем также 2,3,4,7,8-ПХДФ и ПХБ 126 как канцерогены класса 1.[43] Считается, что этот механизм заключается в основном в продвижении, то есть диоксины могут ускорять образование опухолей, вызванных другими факторами, и отрицательно влиять на нормальные механизмы ингибирования роста опухоли.[22] Некоторые исследователи также предположили, что диоксин вызывает прогрессирование рака через совсем другой митохондриальный путь.[44]
Как и в случае со многими токсическими конечными точками диоксина, трудно установить четкую зависимость доза-реакция. Имеются данные о канцерогенности для человека после случайного или сильного профессионального воздействия.[45][46] Рост заболеваемости раком был скромным, на самом деле достичь статистической значимости было трудно даже после высоких аварийных или профессиональных воздействий, таких как отравления Юшо и Ючэн, несчастный случай Севезо и комбинированные профессиональные группы.[1] Поэтому разногласия по поводу риска рака при низких уровнях диоксинов в популяции понятны.[1][21][45][34] Проблема с оценками IARC[43] заключается в том, что они оценивают только опасность, то есть канцерогенность в любой дозе. Вероятно, что существует практический безопасный порог для негенотоксичных диоксинов, и нынешние уровни популяции не имеют никакого риска рака. Таким образом, существует определенное соглашение о том, что риск рака также принимается во внимание, если установлены пределы суточного потребления для защиты от последствий для развития.[37][1] Среди рыбаков с высокими концентрациями диоксинов в организме смертность от рака снизилась, а не увеличилась.[47] Все это означает, что в случае важных полезных продуктов питания и грудного вскармливания перед установлением пределов необходим тщательный анализ пользы / риска, чтобы избежать увеличения других рисков или потери пользы.[48]
Оценка рисков
Неопределенность и вариабельность зависимости доза-реакция диоксинов с точки зрения их токсичности, а также способности диоксинов к биоаккумулировать, привели к тому, что эксперты ВОЗ рекомендуют очень низкие допустимая суточная доза (TDI) диоксина, 1-4 пг / кг массы тела в день, т.е. 7х10−11 до 2,8x10−10г на 70 кг человека в день, чтобы учесть эту неопределенность и обеспечить общественную безопасность во всех случаях.[37] Затем власти установили еженедельный или ежемесячный уровень потребления, равный 2 пг / кг.[1] Поскольку диоксины удаляются очень медленно, бремя тела накопленные в течение всего срока службы высоки по сравнению с дневными дозами, и случайные незначительные превышения предельных значений не сильно его меняют. Поэтому длительный прием намного важнее ежедневного.[1] В частности, была проведена оценка TDI, чтобы гарантировать безопасность детей, рожденных от матерей, подвергавшихся такому ежедневному потреблению диоксинов на протяжении всей своей жизни до беременности.[37] Вполне вероятно, что TDI для других групп населения может быть выше.
Одной из важных причин различий в разных оценках является канцерогенность. Если доза-реакция TCDD вызывает рак линейна, это может быть реальным риском. Если доза-реакция пороговый или J-образной формы, при нынешних концентрациях риск незначителен или отсутствует. Есть надежда, что лучшее понимание механизмов токсичности повысит надежность оценки риска.[2][49] Недавно также была проведена переоценка влияния на развитие группы контаминации Европейское агентство по безопасности пищевых продуктов (EFSA). Они предлагают уменьшить допустимое недельное потребление (TWI) от 14 пг / кг до 2 пг / кг.[20] Это, вероятно, вызовет еще одну полемику, прежде чем будет принято европейскими странами.[1] Потребление диоксина и его уровни в грудном молоке в 1970-х и 1980-х годах были в 5-10 раз выше, чем в настоящее время, и было обнаружено очень мало эффектов, возможно, умеренное влияние на развитие зубов.[1]
Полемика
Гринпис и некоторые другие экологические группы призвали к прекращению производства хлора.[50][51][52] Однако сторонники хлорной промышленности говорят, что «запрет хлора будет означать, что миллионы людей в третьем мире умрут от недостатка дезинфицированной воды».[53] Шэрон Бедер и другие утверждали, что полемика по поводу диоксинов была очень политической и что крупные компании пытались преуменьшить серьезность проблем, связанных с диоксином.[51][52][54] Участвующие компании часто говорят, что кампания против диоксина основана на «страхе и эмоциях», а не на науке.[55]
Потребление человеком и уровни
Большая часть диоксиноподобных химических веществ поступает с пищей животного происхождения: преобладают мясо, молочные продукты или рыба, в зависимости от страны.[1][56] Ежедневное потребление диоксинов и диоксиноподобных ПХБ в виде TEQ составляет порядка 100 пг / день, то есть 1-2 пг / кг / день.[1] Во многих странах как абсолютное, так и относительное значение молочных продуктов и мяса снизились из-за строгого контроля выбросов, что привело к снижению общего потребления. Например. в Соединенном Королевстве общее потребление ПХДД / Ф в 1982 г. составляло 239 пг / день, а в 2001 г. - только 21 пг / день (WHO-TEQ).[3] Поскольку периоды полураспада очень велики (например, TCDD 7-8 лет), нагрузка на организм будет увеличиваться почти на протяжении всей жизни. Следовательно, с 20 до 60 лет концентрации могут увеличиваться в 5-10 раз.[1][57][58] По той же причине кратковременное более высокое потребление, например, после случаев заражения пищевых продуктов, не имеет решающего значения, если оно не является чрезвычайно высоким или длится несколько месяцев или лет.[1]

Наибольшая нагрузка на тело была обнаружена в Западной Европе в 1970-х и начале 1980-х годов.[1][59][60] и тенденции были аналогичными в США.[61] Самый полезный способ измерения временных тенденций - это концентрация в грудном молоке, измеряемая на протяжении десятилетий.[33][59] Во многих странах концентрации снизились примерно до одной десятой от уровня 1970-х годов, а общие концентрации ТЭ сейчас составляют порядка 5-30 пг / г жира.[1][59] (обратите внимание, что единицы измерения, пг / г совпадают с нг / кг или нестандартным выражением ppt, которое иногда используется в Америке).[3] Снижение связано со строгим контролем выбросов, а также контролем концентраций в пищевых продуктах.[62][63] В молодом взрослом женском населении США (возрастная группа 20-39 лет) концентрация липидов в 2001-2002 годах составляла 9,7 пг / г (среднее геометрическое).[58]
Некоторые профессии, такие как натуральные рыбаки в некоторых областях подвергаются исключительно высокому содержанию диоксинов и родственных веществ.[64] Это наряду с высоким уровнем промышленного воздействия может быть наиболее ценным источником информации о рисках для здоровья диоксинов.[47]
Судьба диоксинов в организме человека
Диоксины хорошо всасываются из пищеварительного тракта, если они растворены в жирах или маслах (например, в рыбе или мясе).[4] С другой стороны, диоксины имеют тенденцию прочно адсорбироваться частицами почвы, и абсорбция может быть довольно низкой: было абсорбировано 13,8% заданной дозы ТЭ в загрязненной почве.[65]
Те же свойства, которые вызывают стойкость диоксинов в окружающей среде, также вызывают очень медленное выведение из организма человека и животных. Из-за низкой растворимости в воде почки не могут выделять их с мочой как таковые. Они должны метаболизироваться до более водорастворимых метаболитов, но метаболизм, особенно у людей, очень медленный. Это приводит к биологическому период полураспада нескольких лет для всех диоксинов. Срок действия ТХДД оценивается в 7-8 лет, а для других ПХДД / Ф от 1,4 до 13 лет, ПХДФ в среднем немного короче, чем ПХДД.[1][3][66]
У млекопитающих диоксины содержатся в основном в жире. Концентрации жира кажутся относительно похожими, будь то жир сыворотки, жир жировой ткани или молочный жир. Это позволяет измерять содержание диоксинов путем анализа грудного молока.[59] Однако первоначально, по крайней мере, у лабораторных животных, после однократной дозы высокие концентрации обнаруживаются в печени, но через несколько дней будет преобладать жировая ткань. Однако в печени крысы высокие дозы вызывают индукцию фермента CYP1A2, который связывает диоксины. Таким образом, в зависимости от дозы соотношение концентраций жира и ткани печени у грызунов может значительно различаться.[4]
Использует
Диоксины не имеют общего применения. Они производятся в небольших количествах для химических и токсикологических исследований, но в основном существуют как побочные продукты промышленных процессов, таких как отбеливание бумажная пульпа, пестицид производство и процессы сжигания, такие как сжигание отходов. Дефолиант Агент апельсин содержал диоксины.[67] Производство и использование диоксинов было запрещено Стокгольмская конвенция в 2001.
Источники
Источники окружающей среды
ПХДД / F-соединения никогда не синтезировались для каких-либо целей, за исключением небольших количеств для научных исследований.[16] Небольшие количества ПХДД / Ф образуются всякий раз, когда органические вещества, кислород и хлор доступны при подходящей температуре.[1] Это дополняется металлическими катализаторами, такими как медь. Оптимальный температурный диапазон от 400 ° C до 700 ° C. Это означает, что образование является самым высоким, когда органический материал сжигается в менее чем оптимальных условиях, таких как открытый огонь, пожары в зданиях, домашние камины и плохо эксплуатируемые и / или разработанные печи для сжигания твердых отходов.[3] Исторически сложилось так, что сжигание бытовых и медицинских отходов было самым важным источником ПХДД / Ф.
ПХБ-соединения, всегда содержащие низкие концентрации диоксиноподобных ПХБ и ПХДФ, были синтезированы для различных технических целей (см. Полихлорированные бифенилы ). Они попали в окружающую среду в результате аварий, таких как пожары или утечки из трансформаторов или теплообменников, или из-за продуктов, содержащих ПХБ, на свалках или во время сжигания. Поскольку ПХБ в некоторой степени летучие, их также перевозили на большие расстояния по воздуху, в результате чего глобальное распространение включая Арктику. Лишь небольшая часть ПХБ в смесях подобна диоксину.[1]
Другие источники ПХДД / Ф включают:
- Неконтролируемое горение, особенно открытое сжигание отходов («горение бочки на заднем дворе»), случайные пожары, лесные пожары. В настоящее время это наиболее важные источники.[1]
- Выплавка и рафинирование металлов
- Отбеливание целлюлозы и бумаги хлором - исторически важный источник попадания ПХДД / Ф в водные пути.[68]
- Побочные продукты синтеза нескольких химических веществ, особенно ПХД, хлорфенолы, гербициды хлорфеноксикислоты и гексахлорофен.[42]
- (Исторический) Двигатели, использующие этилированное топливо, который содержал добавки 1,2-дихлорэтан и 1,2-дибромэтан.
При сжигании отходов
Улучшения и изменения были внесены почти во все промышленные источники для сокращения производства ПХДД / Ф. Что касается сжигания отходов, широкая огласка и озабоченность по поводу диоксиноподобных соединений в течение 1980-х - 1990-х годов продолжают проникать в общественное сознание, особенно когда новые сжигания и превращение отходов в энергию объекты предлагаются. В результате этих проблем процессы сжигания были улучшены за счет повышения температуры горения (более 1000 ° C), лучшего управления печью и достаточного времени пребывания, выделенного для обеспечения полного окисления органических соединений. В идеале процесс сжигания окисляет весь углерод до CO2 и превращает весь хлор в HCl или неорганические хлориды до прохождения газов через температурный интервал 700-400 ° C, где возможно образование ПХДД / Ф. Эти вещества не могут легко образовывать органические соединения, а HCl легко и безопасно нейтрализуется в скруббер а CO2 выбрасывается в атмосферу. Неорганические хлориды включаются в золу.
Системы очистки и удаления твердых частиц позволяют улавливать часть ПХДД / Ф, образующихся даже на сложных мусоросжигательных заводах. Эти ПХДД / Ф обычно не уничтожаются, а перемещаются в летучая зола. Каталитический разработаны системы, которые разрушают ПХДД / Ф в паровой фазе при относительно низких температурах. Эта технология часто сочетается с рукавный фильтр или SCR система в хвостовой части мусоросжигательного завода.
Пределы Европейского Союза для концентрации диоксиноподобных соединений в отходящих дымовых газах составляют 0,1 нг / Нм³ ТЭ.[70][71]
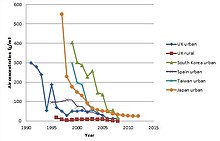
Оба в Европе[72] и в США,[73] выбросы резко снизились с 1980-х годов, даже на 90% (см. рисунок). Это также привело к снижению нагрузки на организм человека, что четко демонстрируется снижением концентрации диоксина в грудном молоке.[59] В связи со значительным сокращением выбросов от мусоросжигательных заводов, другие потенциально крупные источники диоксиноподобных соединений, например, от лесов и лесных пожаров, увеличились по сравнению с промышленными источниками.[74] Однако они не включены в общую инвентаризацию из-за неточностей в имеющихся данных.[75] Более недавнее исследование экологических последствий аварийных пожаров, в том числе: лесной пожар, по оценке, выбросы диоксинов (ПХДД / Ф) примерно эквивалентны выбросам от транспортных средств и сжигания городских отходов.[76]
Открытое сжигание отходов (сжигание бочек на заднем дворе) не уменьшилось эффективно, и в США сейчас это самый важный источник диоксинов. Общие годовые выбросы в США снизились с 14 кг в 1987 году до 1,4 кг в 2000 году. Однако сжигание бочек на заднем дворе снизилось лишь незначительно, с 0,6 кг до 0,5 кг, в результате чего в 2000 году только сжигание на заднем дворе привело к образованию более одной трети всех диоксинов.[73]
Низкие концентрации диоксинов были обнаружены в некоторых почвах без какого-либо антропогенного загрязнения. Загадочный случай заражения молока был обнаружен в Германии. Источником был каолин, добавляемый в корм для животных. Диоксины неоднократно обнаруживались в глинах из Европы и США с 1996 года, причем загрязнение глины предполагалось результатом древних лесных пожаров или аналогичных природных явлений с концентрацией ПХДД / Ф во время осаждения глины.[77]
Диоксины и сахарный тростник
При выращивании сахарного тростника оставшиеся жмых после экстракции сахар используется в больших количествах для производства энергии, и на местном уровне считается замечательным источником диоксинов[78] Это в основном указывает на то, что при сжигании органических материалов образуются диоксины, и это должно происходить при достаточно высоких температурах и при надлежащей фильтрации дымовых газов. Для очистки газов и загрязняющих веществ в производстве сахарного тростника часто используются мокрые газоочистители, такие как Вентури тип. Кроме того, используются и другие лечебные системы. электрофильтр и карманные фильтры.[79] Этих методов может быть недостаточно[78][79][80]
Стойкость в окружающей среде и биоаккумуляция
Все группы диоксиноподобных соединений устойчивы в окружающей среде.[81] Очень немногие почвенные микробы и животные способны эффективно разрушать ПХДД / Ф с помощью бокового хлора (позиции 2, 3, 7 и 8). Это вызывает очень медленное выведение. Однако ученые Университет Мартина Лютера Недавно было обнаружено, что разновидность бактерий Dehalococcoides CBDB1 может извлекать хлор из диоксиновых соединений в отсутствие кислорода.[82][83] Ультрафиолетовый свет может медленно разрушать эти соединения. Липофильность (склонность к образованию жироподобных сред) и очень плохая растворимость в воде заставляют эти соединения перемещаться из водной среды в живые организмы, имеющие структуру липидных клеток. Это называется биоаккумуляция. Увеличение хлорирования увеличивает как стабильность, так и липофильность. Однако соединения с очень высоким числом хлора (например, октахлородибензо-п-диоксин) настолько плохо растворимы, что это препятствует их биоаккумуляции.[81] За биоаккумуляцией следует биомагнификация. Жирорастворимые соединения сначала накапливаются в микроскопических организмах, таких как фитопланктон (планктон растительного характера, например, водоросли). Фитопланктон потребляется животным планктоном, беспозвоночными, такими как насекомые, мелкой рыбой, а также крупной рыбой и тюленями. На каждом этапе или трофический уровень концентрация выше, потому что стойкие химические вещества не «сжигаются», когда высший организм использует жир организма жертвы для производства энергии.
Из-за биоаккумуляции и биомагнификации виды, находящиеся на вершине трофическая пирамида наиболее уязвимы для диоксиноподобных соединений. В Европе орлан-белохвост а некоторые виды тюленей приблизились к исчезновению из-за отравления стойкими органическими загрязнителями.[84] Точно так же в Америке население лысые орлы снизился из-за СОЗ, вызывающих истончение яичной скорлупы и других репродуктивных проблем.[85] Обычно неудачу приписывают в основном ДДТ, но диоксины также являются возможной причиной репродуктивных эффектов. И в Америке, и в Европе многие водоплавающие птицы имеют высокие концентрации диоксинов, но обычно недостаточно высокие, чтобы помешать их репродуктивному успеху.[84][86] Благодаря подкормке зимой и другим мерам орлан-белохвост выздоравливает (см. Орлан-белохвост ). Также восстанавливается кольчатая нерпа в Балтийском море.
Люди также находятся на вершине трофической пирамиды, особенно новорожденные. По оценкам, новорожденные, находящиеся на исключительно грудном вскармливании, подвергались в общей сложности 800 пг ТЭ / день, что привело к расчетной дозе, основанной на массе тела, в 242 пг ТЭ / кг / день.[87] Из-за множества пищевых источников воздействие на взрослых людей в среднем намного меньше, составляя 1 пг ТЭ / кг в день,[87] и концентрации диоксина у взрослых намного меньше и составляют 10-100 пг / г по сравнению с 9000-340000 пг / г (ТЭ в липидах) у орлов.[84] или тюлени, питающиеся почти исключительно рыбой.
Из-за различных физико-химических свойств не все конгенеры диоксиноподобных соединений одинаково хорошо попадают в организм человека. В качестве TEQ доминирующими конгенерами в тканях человека являются 2,3,7,8-TCDD, 1,2,3,7,8-PeCDD, 1,2,3,6,7,8-HxCDD и 2,3 , 4,7,8-ПеХДФ.[3] Это сильно отличается от большинства источников, где могут преобладать гепта- и окта-конгенеры. Группа ВОЗ, проводившая повторную оценку значений TEF в 2005 г., выразила озабоченность по поводу того, что выбросы не следует некритически измерять как TEQ, поскольку не все конгенеры одинаково важны.[5] Они заявили, что «когда оценка риска для человека должна быть сделана на основе абиотических матриц, следует особо учитывать такие факторы, как судьба, перенос и биодоступность каждой матрицы».[5]
Все СОЗ плохо растворяются в воде, особенно диоксины. Таким образом, загрязнение грунтовых вод не представляло проблемы даже в случае серьезного загрязнения основными химическими веществами, такими как хлорфенолы.[88]В поверхностных водах диоксины связаны с органическими и неорганическими частицами.
Источники воздействия на человека
Наиболее важным источником воздействия на человека является жирная пища животного происхождения (см. Потребление человека выше),[33] и грудное молоко.[87] По наиболее важным пунктам в разных странах существуют большие различия. В США и Центральной Европе молоко, молочные продукты и мясо были наиболее важными источниками. В некоторых странах, особенно в Финляндии и в некоторой степени в Швеции, рыба имеет важное значение из-за загрязненной балтийской рыбы и очень низкого потребления из любых других источников.[3] В большинстве стран произошло значительное снижение потребления диоксинов из-за более строгого контроля за последние 20 лет.
Исторически серьезной проблемой было воздействие диоксинов на рабочем месте.[42] Диоксины образуются как важные побочные токсичные продукты при производстве Печатные платы, хлорфенолы, гербициды хлорфеноксикислоты, и другие хлорированные органические химические вещества. Это привело к очень сильному воздействию на рабочих в плохо контролируемых гигиенических условиях. Многие рабочие имели хлоракне. В NIOSH В исследовании, проведенном в США, средняя концентрация ТХДД у лиц, подвергшихся воздействию, составляла 233 нг / кг (в липидах сыворотки), в то время как у рабочих, не подвергавшихся воздействию, она составляла 7 нг / кг, хотя воздействие было 15–37 лет назад.[42] Это указывает на огромную предыдущую экспозицию. Фактически, точный обратный расчет обсуждается, и концентрации могут быть даже в несколько раз выше, чем первоначально предполагалось.[89]
Обработка и опрыскивание гербициды хлорфеноксикислоты может также вызывать довольно сильное воздействие, что ясно продемонстрировали пользователи Агент апельсин в Малайский Emergency и в война во Вьетнаме. Самые высокие концентрации были обнаружены у нелетящего военнослужащего (например, при заполнении баков самолетов), хотя колебания были огромными, от 0 до 618 нг / кг ТХДД (в среднем 23,6 нг / кг).[42] Прочие профессиональные воздействия (работающие на бумажных и целлюлозных заводах, сталелитейных заводах и мусоросжигательных заводах) были значительно ниже.[42]
В некоторых случаях случайные воздействия были огромными. Самые высокие концентрации у людей после Авария Севезо составили 56000 нг / кг, а самый высокий уровень воздействия, когда-либо зарегистрированный, был обнаружен в Австрии в 1998 году, 144000 нг / кг (см. TCDD ).[26] Это эквивалентно дозе от 20 до 30 мкг / кг TCDD, доза, которая была бы смертельной для морских свинок и некоторых линий крыс.
Воздействие загрязненной почвы возможно, если диоксины выбрасываются в пыль или дети поедают грязь. Вдыхание было ясно продемонстрировано в Миссури в 1970-х годах, когда отработанные масла использовались в качестве средства подавления пыли на конных аренах. Многие лошади и другие животные погибли из-за отравления.[90] Диоксины не являются ни летучими, ни водорастворимыми, поэтому воздействие на человека зависит от прямого поедания почвы или образования пыли, которая несет это химическое вещество. Загрязнение грунтовых вод или вдыхаемых паров химического вещества вряд ли вызовет значительное воздействие. В настоящее время в США насчитывается 126 Суперфонд участки с завершенным путем воздействия, загрязненные диоксинами.
Кроме того, известно, что ПХД проходят через очистные сооружения и накапливаются в ил который используется на сельскохозяйственных полях в некоторых странах. В 2011 году в Южной Каролине SCDHEC ввел в действие правила аварийного отстоя после того, как было обнаружено, что ПХД сбрасываются на очистные сооружения.[91]
Также известно, что ПХД вымываются из промышленности и с земли (иначе говоря, отстойных полей), загрязняя рыбу,[92] как у них есть вверх и вниз по реке Катоба в Северной и Южной Каролине. Государственные органы опубликовали рекомендации по потреблению рыбы из-за накопления ПХБ в тканях рыбы.[93]
Было несколько эпизодов заражения пищевых продуктов, один из самых известных произошел в Бельгия в 1999 году.[1] Резервуар переработанных жиров, собранных для производства кормов для животных, был загрязнен маслом ПХБ, содержащим около 1 г диоксинов и 2 г DL-ПХБ. Это вызвало серьезную тревогу в Европейском Союзе, но из-за относительно быстрой реакции и медленного накопления диоксинов в организме людей не было никакого воздействия на здоровье.[1] В 2008 году была аналогичная заболеваемость в Ирландии. В 2008 году Чили пережила свиной кризис вызвано высокими концентрациями диоксинов в их экспорте свинины. Было установлено, что заражение произошло из-за оксида цинка, используемого в кормах для свинины, и вызвало репутационные и финансовые потери страны, а также привело к введению новых правил безопасности пищевых продуктов.[94] Эти эпизоды подчеркивают важность контроля за пищевыми продуктами, а раннее обнаружение гарантирует, что очень медленно накапливающиеся диоксины не увеличиваются у людей до уровней, вызывающих токсические эффекты.
Значения TEF и эквиваленты токсичности
Все диоксиноподобные соединения имеют общий механизм действия через арилуглеводородный рецептор (AHR), но их эффективность сильно различается. Это означает, что все они вызывают схожие эффекты, но требуются гораздо большие дозы некоторых из них, чем TCDD. Связывание с AHR, а также стойкость в окружающей среде и в организме зависит от присутствия так называемых «боковых хлоринов», в случае диоксинов и фуранов, заместителей хлора в положениях 2, 3, 7 и 8.[3] Каждый дополнительный нелатеральный хлор снижает эффективность, но качественно эффекты остаются аналогичными. Следовательно, простая сумма различных конгенеров диоксинов не является значимым показателем токсичности. Чтобы сравнить токсичность различных конгенеров и сделать возможным получение токсикологически значимой суммы смеси, была создана концепция эквивалентности токсичности (TEQ).[5]
Каждому сородичу дали коэффициент эквивалентности токсичности (TEF).[5][68] Это указывает на его относительную токсичность по сравнению с TCDD. Большинство TEF были извлечены из in vivo данные о токсичности для животных, но если они отсутствуют (например, в случае некоторых ПХБ), менее надежны in vitro данные были использованы.[5] После умножения фактического количества или концентрации родственного соединения на его TEF, продукт представляет собой виртуальное количество или концентрацию TCDD, оказывающую воздействие той же степени, что и рассматриваемое соединение. Это умножение выполняется для всех соединений в смеси, и эти «эквиваленты TCDD» затем могут быть просто добавлены, что дает TEQ, количество или концентрацию TCDD, токсикологически эквивалентную смеси.
Преобразование TEQ позволяет использовать все исследования наиболее изученного TCDD для оценки токсичности смеси. Это наиболее полезно в нормативной работе, но может также использоваться в научных исследованиях.[95] Это похоже на обычную меру для всех алкогольных напитков: пиво, вино и виски можно сложить вместе как абсолютный алкоголь, и эта сумма дает токсикологически значимую меру общего воздействия.
TEQ применяется только к диоксиноподобным эффектам, опосредованным AHR. Некоторые токсические эффекты (особенно ПХД) могут быть независимыми от AHR, и они не принимаются во внимание при использовании TEQ.
TEF также являются приближениями с определенным количеством научных суждений, а не с научными фактами. Следовательно, они могут время от времени пересматриваться. С 1980-х годов было выпущено несколько версий TEF. Самая последняя переоценка была проведена группой экспертов Всемирной организации здравоохранения в 2005 г.

| Класс | Конгенер | Фактор токсической эквивалентности[5] |
|---|---|---|
| Полихлорированные диоксины | 2,3,7,8-TCDD | 1 |
| 1,2,3,7,8-PeCDD | 1 | |
| 1,2,3,4,7,8-HxCDD | 0.1 | |
| 1,2,3,6,7,8-HxCDD | 0.1 | |
| 1,2,3,7,8,9-HxCDD | 0.1 | |
| 1,2,3,4,6,7,8-HpCDD | 0.01 | |
| OCDD | 0.0003 | |
| Полихлорированные дибензофураны | 2,3,7,8-ТХДФ | 0.1 |
| 1,2,3,7,8-ПеХДФ | 0.03 | |
| 2,3,4,7,8-ПеХДФ | 0.3 | |
| 1,2,3,4,7,8-HxCDF | 0.1 | |
| 1,2,3,6,7,8-HxCDF | 0.1 | |
| 1,2,3,7,8,9-HxCDF | 0.1 | |
| 2,3,4,6,7,8-HxCDF | 0.1 | |
| 1,2,3,4,6,7,8-HpCDF | 0.01 | |
| 1,2,3,4,7,8,9-HpCDF | 0.01 | |
| OCDF | 0.0003 | |
| Неортозамещенные печатные платы | 3,3 ’, 4,4’-TCB (77) | 0.0001 |
| 3,4,4 ’, 5-ТХБ (81) | 0.0003 | |
| 3,3 ’, 4,4’, 5-ПеХБ (126) | 0.1 | |
| 3,3 ’, 4,4’, 5,5’-HxCB (169) | 0.03 | |
| Моно-орто-замещенные печатные платы | 2,3,3 ’, 4,4’-ПеХБ (105) | 0.00003 |
| 2,3,4,4 ’, 5-ПеХБ (114) | 0.00003 | |
| 2,3 ’, 4,4’, 5-ПеХБ (118) | 0.00003 | |
| 2 ’, 3,4,4’, 5-ПеХБ (123) | 0.00003 | |
| 2,3,3 ’, 4,4’, 5-HxCB (156) | 0.00003 | |
| 2,3,3 ’, 4,4’, 5’-HxCB (157) | 0.00003 | |
| 2,3 ’, 4,4’, 5,5’-HxCB (167) | 0.00003 | |
| 2,3,3 ’, 4,4’, 5,5’-HpCB (189) | 0.00003 |
- (T = тетра, Pe = пента, Hx = гекса, Hp = гепта, O = окта)
использованная литература
 Некоторое содержание этой статьи было извлечено из Диоксины и диоксиноподобные соединения: токсичность для людей и животных, источники и поведение в окружающей среде в Викиверситете, который находится под лицензией Лицензия Creative Commons Attribution-Share Alike 3.0 (Unported) (CC-BY-SA 3.0).
Некоторое содержание этой статьи было извлечено из Диоксины и диоксиноподобные соединения: токсичность для людей и животных, источники и поведение в окружающей среде в Викиверситете, который находится под лицензией Лицензия Creative Commons Attribution-Share Alike 3.0 (Unported) (CC-BY-SA 3.0).
Версия этой статьи 2019 года была обновлена внешним экспертом в соответствии с моделью двойной публикации. Соответствующие академическая экспертная оценка статья была опубликована в WikiJournal of Медицина и может быть процитирован как: Йоуко Туомисто (2019), Кейт Брейн; Томас Шафи (ред.), «Диоксины и диоксиноподобные соединения: токсичность для людей и животных, источники и поведение в окружающей среде» (PDF), WikiJournal of Медицина, 6 (1): 8, Дои:10.15347 / WJM / 2019.008, ISSN 2002-4436, Викиданные Q83503827 |
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль я ан ао ap водный Tuomisto, Jouko (2019) Диоксины и диоксиноподобные соединения: токсичность для людей и животных, источники и поведение в окружающей среде. WikiJournal of Medicine 6 (1): 8 | https://doi.org/10.15347/wjm/2019.008
- ^ а б «Являются ли диоксины самыми опасными химическими веществами в нашей окружающей среде?». opasnet.org.
- ^ а б c d е ж г час я Сводка по диоксинам и ПХБ
- ^ а б c d е ж г Похьянвирта Р., Туомисто Дж. (Декабрь 1994 г.). «Краткосрочная токсичность 2,3,7,8-тетрахлордибензо-п-диоксина у лабораторных животных: эффекты, механизмы и модели на животных». Фармакологические обзоры. 46 (4): 483–549. PMID 7899475.
- ^ а б c d е ж г час я j k л м п Ван ден Берг М., Бирнбаум Л.С., Денисон М., Де Вито М., Фарланд В., Фили М. и др. (Октябрь 2006 г.). «Переоценка Всемирной организацией здравоохранения 2005 г. факторов токсической эквивалентности диоксинов и диоксиноподобных соединений для человека и млекопитающих». Токсикологические науки. 93 (2): 223–241. Дои:10.1093 / toxsci / kfl055. ЧВК 2290740. PMID 16829543.
- ^ Вебер Р., Гаус К., Тайсклинд М., Джонстон П., Фортер М., Холлерт Х., Хайниш Е., Холубек И., Ллойд-Смит М., Масунага С., Моккарелли П., Сантилло Д., Сейке Н., Саймон Р., Торрес Дж. П., Верта М., Варбелов Г., Виджген Дж., Уотсон А., Костнер П., Вельц Дж., Вайциск П., Зеннегг М. (2008) Сайты, загрязненные диоксинами и СОЗ - актуальность и проблемы в современном и будущем: обзор истории, целей и масштабов серии. Environ Sci Pollut Res Int. Июл; 15 (5): 363-393. DOI: 10.1007 / s11356-008-0024-1. Epub 2008 3 июля.
- ^ Агентство регистрации токсичных веществ и заболеваний (ATSDR) (1998). Заявление об общественном здравоохранении хлорированные дибензо-п-диоксины (ХДД) (Отчет). Атланта, Джорджия: Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения. Получено 2019-04-23.
- ^ Xu J, Ye Y, Huang F, Chen H, Wu H, Huang J и др. (Ноябрь 2016 г.). «Связь между диоксином и заболеваемостью и смертностью от рака: метаанализ». Научные отчеты. 6: 38012. Bibcode:2016НатСР ... 638012X. Дои:10.1038 / srep38012. ЧВК 5126552. PMID 27897234.
- ^ Вебер Р., Тайсклинд М., Гаус С. (март 2008 г.). «Диоксин - современные и будущие вызовы исторического наследия. Посвящается профессору доктору Отто Хутцингеру, основателю серии конференций DIOXIN». Международная ассоциация экологических наук и исследований загрязнения. 15 (2): 96–100. Дои:10.1065 / espr2008.01.473. PMID 18380226.
- ^ а б Денисон М.С., Надь С.Р. (2003). «Активация арилуглеводородного рецептора структурно разнообразными экзогенными и эндогенными химическими веществами». Ежегодный обзор фармакологии и токсикологии. 43: 309–334. Дои:10.1146 / annurev.pharmtox.43.100901.135828. PMID 12540743.
- ^ Коннор К.Т., Харрис М.А., Эдвардс М.Р., Будинский Р.А., Кларк Г.К., Чу А.С. и др. (Июль 2008 г.). «Активность агониста рецептора AH в крови человека, измеренная с помощью клеточного биоанализа: доказательства наличия лигандов рецептора AH естественного происхождения in vivo». Журнал экспозиции и эпидемиологии окружающей среды. 18 (4): 369–380. Дои:10.1038 / sj.jes.7500607. PMID 17912254.
- ^ Похьянвирта, Раймо, изд. (2011). Рецептор AH в биологии и токсикологии. Вайли. Дои:10.1002/9781118140574. ISBN 9781118140574.
- ^ Hahn, Mark E .; Кархнер, Сибель И. (2011). «Структурная и функциональная диверсификация AHR во время эволюции многократных животных». Рецептор AH в биологии и токсикологии. John Wiley & Sons, Ltd., стр. 387–403. ISBN 9781118140574
- ^ Bock, KW (1 апреля 2017 г.). «Арилуглеводородный рецептор человека и грызунов (AHR): от медиатора токсичности диоксина до физиологических функций AHR и терапевтических возможностей». Биологическая химия 398 (4): 455-464. DOI: 10.1515 / hsz-2016-0303
- ^ Poellinger L (апрель 2000 г.). «Механистические аспекты - рецептор диоксина (арилуглеводорода)». Пищевые добавки и загрязняющие вещества. 17 (4): 261–266. Дои:10.1080/026520300283333. PMID 10912240.
- ^ а б c d Линден Дж., Ленсу С., Туомисто Дж., Похьянвирта Р. (октябрь 2010 г.). «Диоксины, рецепторы арилуглеводородов и центральная регуляция энергетического баланса». Границы нейроэндокринологии. 31 (4): 452–478. Дои:10.1016 / j.yfrne.2010.07.002. PMID 20624415.
- ^ а б Окей AB (июль 2007 г.). "Одиссея рецепторов арилуглеводородов к берегам токсикологии: лекция Дайхмана, Международный конгресс токсикологии-XI". Токсикологические науки. 98 (1): 5–38. Дои:10.1093 / toxsci / kfm096. PMID 17569696.
- ^ Тиджет Н., Бутрос П.С., Моффат И.Д., Окей А.Б., Туомисто Дж., Похьянвирта Р. (январь 2006 г.). «Арилуглеводородный рецептор регулирует отдельные диоксин-зависимые и диоксиннезависимые генные батареи». Молекулярная фармакология. 69 (1): 140–153. Дои:10.1124 / моль.105.018705. PMID 16214954.
- ^ Браун Д. Д., Орелен Дж., Гордон Дж. Д., Чу А.С., Чу М.Д., Накамура М., Ханда Х., Каяма Ф., Денисон М.С., Кларк Г.К. (июнь 2007 г.). «Математическая модель, разработанная для образцов окружающей среды: прогноз TEQ диоксина ГХ / МС на основе данных биотеста XDS-CALUX». Экологические науки и технологии. 41 (12): 4354–4360. Bibcode:2007EnST ... 41.4354B. Дои:10.1021 / es062602 +. ЧВК 2877589. PMID 17626436.
- ^ а б c Панель EFSA по загрязняющим веществам в пищевой цепочке (2018). «Риск для здоровья животных и человека, связанный с присутствием диоксинов и диоксиноподобных ПХБ в кормах и пищевых продуктах». Журнал EFSA. 16 (11): 5333. Дои:10.2903 / j.efsa.2018.5333.
- ^ а б Каяджанян GM (январь 2002 г.). «J-образная кривая зависимости реакции от дозы диоксина». Экотоксикология и экологическая безопасность. 51 (1): 1–4. Дои:10.1006 / eesa.2001.2115. PMID 11800543.
Этот комментарий является ответом на недавнюю статистическую обработку данных о заболеваемости раком у отдельных рабочих, подвергшихся воздействию диоксина, из более раннего исследования химического завода NIOSH. Вопреки новым открытиям авторов NIOSH, реакция заболеваемости раком на увеличение воздействия диоксина имеет J-образную форму, как и в двух основных наборах данных, на которые они не смогли сослаться или объяснить. Статистическая обработка NIOSH скрыла значительное снижение заболеваемости раком, которое происходит при низком уровне воздействия диоксинов. Несмотря на то, что заболеваемость раком может увеличиваться при высоком воздействии диоксинов, такому увеличению при более низком воздействии может предшествовать значительное снижение.
- ^ а б c Драган Ю.П., Шренк Д. (апрель 2000 г.). «Исследования на животных, посвященные канцерогенности TCDD (или родственных соединений) с упором на развитие опухоли». Пищевые добавки и загрязняющие вещества. 17 (4): 289–302. Дои:10.1080/026520300283360. PMID 10912243.
- ^ Мацумото М, Андо М (1991). «Мутагенность 3-хлордибензофурана и его метаболическая активация». Экологический и молекулярный мутагенез. 17 (2): 104–111. Дои:10.1002 / em.2850170207. PMID 2009865.
- ^ а б Бирнбаум Л.С., Туомисто Дж. (Апрель 2000 г.). «Неканцерогенные эффекты TCDD у животных». Пищевые добавки и загрязняющие вещества. 17 (4): 275–88. Дои:10.1080/026520300283351. PMID 10912242.
- ^ КТО информационный бюллетень: Диоксины и их влияние на здоровье человека, Май 2010 г.
- ^ а б Геусау А., Абрахам К., Гейсслер К., Сатор М.О., Стингл Г., Чахлер Э. (август 2001 г.). «Тяжелая интоксикация 2,3,7,8-тетрахлордибензо-п-диоксином (TCDD): клинические и лабораторные эффекты». Перспективы гигиены окружающей среды. 109 (8): 865–9. Дои:10.1289 / ehp.01109865. ЧВК 1240417. PMID 11564625.
- ^ Сорг О., Зеннегг М., Шмид П., Федосюк Р., Валихновский Р., Гайде О. и др. (Октябрь 2009 г.). «Отравление 2,3,7,8-тетрахлордибензо-п-диоксином (ТХДД) у Виктора Ющенко: идентификация и измерение метаболитов ТХДД». Ланцет. 374 (9696): 1179–85. Дои:10.1016 / с0140-6736 (09) 60912-0. PMID 19660807.
- ^ Митома С., Учи Х., Цукимори К., Ямада Х., Акахане М., Имамура Т. и др. (Сентябрь 2015 г.). «Юшо и его последние результаты - обзор исследований, проведенных Yusho Group». Environment International. 82: 41–8. Дои:10.1016 / j.envint.2015.05.004. PMID 26010306.
- ^ а б c Суини MH, Mocarelli P (апрель 2000 г.). «Влияние на здоровье человека после воздействия 2,3,7,8-ТХДД». Пищевые добавки и загрязняющие вещества. 17 (4): 303–16. Дои:10.1080/026520300283379. PMID 10912244.
- ^ Алалуусуа С., Кальдерара П., Герту П.М., Лукинмаа П.Л., Коверо О., Нидхэм Л. и др. (Сентябрь 2004 г.). «Аберрации развития зубов после аварии с диоксином в Севезо». Перспективы гигиены окружающей среды. 112 (13): 1313–8. Дои:10.1289 / ehp.6920. ЧВК 1247522. PMID 15345345.
- ^ Mocarelli P, Gerthoux PM, Ferrari E, Patterson DG, Kieszak SM, Brambilla P, Vincoli N, Signorini S, Tramacere P, Carreri V, Sampson EJ, Turner WE, Needham LL (май 2000 г.). «Отцовские концентрации диоксина и соотношение полов в потомстве». Ланцет. 355 (9218): 1858–63. Дои:10.1016 / S0140-6736 (00) 02290-X. HDL:10281/16136. PMID 10866441.
- ^ Mocarelli P, Gerthoux PM, Patterson DG, Milani S, Limonta G, Bertona M, Signorini S, Tramacere P, Colombo L, Crespi C, Brambilla P, Sarto C, Carreri V, Sampson EJ, Turner WE, Needham LL (январь 2008 г. ). «Воздействие диоксинов с младенчества до полового созревания вызывает эндокринные нарушения и влияет на качество спермы человека». Перспективы гигиены окружающей среды. 116 (1): 70–7. Дои:10.1289 / ehp.10399. ЧВК 2199303. PMID 18197302.
- ^ а б c d Лием А.К., Фюрст П., Рапп С. (апрель 2000 г.). «Воздействие диоксинов и родственных соединений на население». Пищевые добавки и загрязняющие вещества. 17 (4): 241–59. Дои:10.1080/026520300283324. PMID 10912239.
- ^ а б Туомисто Дж., Пекканен Дж., Кивиранта Х., Тукиайнен Э., Вартиайнен Т., Туомисто Дж. (Март 2004 г.). «Саркома мягких тканей и диоксин: исследование случай-контроль». Международный журнал рака. 108 (6): 893–900. Дои:10.1002 / ijc.11635. PMID 14712494.
- ^ Алалуусуа С., Лукинмаа П.Л., Вартиайнен Т., Партанен М., Торппа Дж., Туомисто Дж. (Май 1996 г.). «Полихлорированные дибензо-п-диоксины и дибензофураны, поступающие с материнским молоком, могут вызывать дефекты развития зубов у ребенка». Экологическая токсикология и фармакология. 1 (3): 193–7. Дои:10.1016/1382-6689(96)00007-5. PMID 21781681.
- ^ Мингес-Аларкон Л., Сергеев О., Бернс Дж. С., Уильямс П. Л., Ли М. М., Коррик С. А. и др. (Март 2017 г.). «Продольное исследование концентраций хлорорганических соединений в перипубертатной сыворотке и параметров спермы у молодых мужчин: российское исследование детей». Перспективы гигиены окружающей среды. 125 (3): 460–466. Дои:10.1289 / EHP25. ЧВК 5332179. PMID 27713107.
- ^ а б c d «Консультации по оценке риска для здоровья диоксинов; переоценка допустимой суточной дозы (TDI): краткое изложение». Пищевые добавки и загрязняющие вещества. 17 (4): 223–40. Апрель 2000 г. Дои:10.1080/713810655. PMID 10912238.
- ^ Мальяно Д. Д., Ло В. Х., Хардинг Д. Л., Боттон Д., Шоу Д. Е. (февраль 2014 г.). «Стойкие органические загрязнители и диабет: обзор эпидемиологических данных». Диабет и метаболизм. 40 (1): 1–14. Дои:10.1016 / j.diabet.2013.09.006. PMID 24262435.
- ^ «ERC отвечает на недавнее исследование эндометриоза». Центр исследования эндометриоза. Архивировано из оригинал на 02.02.2016. Получено 2016-01-10.
- ^ Шренк Д., Чопра М. «Диоксин активировал AHR и рак у лабораторных животных». В Pohjanvirta R (ред.). Рецептор АГ в биологии и токсикологии. Вайли. ISBN 9780470601822.
- ^ «Методы оценки канцерогенных рисков для здоровья от диоксиноподобных соединений». Министерство здравоохранения Миннесоты. Октябрь 2006 г. Архивировано с оригинал на 2010-07-08. Получено 2010-09-08.
- ^ а б c d е ж Монографии МАИР по оценке канцерогенных рисков для человека, том 69, Лион, 1997 г.
- ^ а б Рабочая группа МАИР по оценке канцерогенного риска для человека (2012 г.). 2,3,7,8-тетрахлордибензопара-диоксин, 2,3,4,7,8-пентахлордибензофуран и 3,3 ', 4,4', 5-пентахлорбифенил. 100F. Международное агентство по изучению рака. С. 339–378.
- ^ FN ISI Export Format VR 1.0 PT J TI Рак и TCDD: митохондриальная связь AU Mead, MN SO ПЕРСПЕКТИВЫ ЗДОРОВЬЯ ОКРУЖАЮЩЕЙ СРЕДЫ VL 116 IS 3 BP A112 EP A112 PY 2008 TC 0 UT WOS: 000253670600010 SN 0091-6765 ER EF
- ^ а б Кожевинас М (апрель 2000 г.). «Исследования рака у человека». Пищевые добавки и загрязняющие вещества. 17 (4): 317–24. Дои:10.1080/026520300283388. PMID 10912245.
- ^ Pesatori AC, Consonni D, Rubagotti M, Grillo P, Bertazzi PA (сентябрь 2009 г.). «Заболеваемость раком среди населения, подвергшегося воздействию диоксина после« аварии Севезо »: двадцать лет наблюдения». Состояние окружающей среды. 8: 39. Дои:10.1186 / 1476-069X-8-39. ЧВК 2754980. PMID 19754930.
- ^ а б Турунен А.В., Веркасало П.К., Кивиранта Х., Пуккала Э., Юла А., Мяннистё С. и др. (Октябрь 2008 г.). «Смертность в когорте с высоким потреблением рыбы». Международный журнал эпидемиологии. 37 (5): 1008–17. Дои:10.1093 / ije / dyn117. PMID 18579573.
- ^ Туомисто Дж. Т., Асикайнен А., Мериляйнен П., Хаапасаари П. (январь 2020 г.). «Влияние питательных веществ и загрязнителей окружающей среды на здоровье балтийской сельди и лосося: количественная оценка пользы и риска». BMC Public Health. 20 (1): 64. Дои:10.1186 / s12889-019-8094-1. ЧВК 6964011. PMID 31941472.
- ^ Туомисто Дж. (Сентябрь 2005 г.). «Помогает ли механистическое понимание в оценке риска - на примере диоксинов». Токсикология и прикладная фармакология. 207 (2 Дополнение): 2–10. Дои:10.1016 / j.taap.2005.01.053. PMID 15996698.
- ^ "Споры о диоксинах - что такое диоксины?". uow.edu.au.
- ^ а б Шэрон Бедер. 'Споры о диоксинах: распространились на школы', Журнал австралийских учителей естественных наук, Ноябрь 1998 г., стр. 28–34.
- ^ а б Шэрон Бедер (2000). Global Spin: корпоративная атака на защиту окружающей среды, Scribe Publications, главы 9 и 13.
- ^ Шэрон Бедер (2000) Global Spin: корпоративная атака на защиту окружающей среды, Scribe Publications, стр. 153.
- ^ Рональд Кристальди. Рецензия на книгу Лоис Мари Гиббс `` Умирать от диоксина '' В архиве 2013-10-29 в Wayback Machine Журнал землепользования и экологического права, 1996.
- ^ Бедер С. (март 2002 г.). Глобальный подход: корпоративная атака на защиту окружающей среды. Девон: Зеленые книги. п. 154.
- ^ Диоксины и диоксиноподобные соединения в пищевых продуктах: стратегии снижения воздействия Совет по пищевым продуктам и питанию (FNB), Институт медицины
- ^ Кивиранта Х., Туомисто Дж. Т., Туомисто Дж., Тукиайнен Э., Вартиайнен Т. (август 2005 г.). «Полихлорированные дибензо-п-диоксины, дибензофураны и бифенилы среди населения Финляндии в целом». Атмосфера. 60 (7): 854–69. Bibcode:2005Чмсп..60..854К. Дои:10.1016 / j.chemosphere.2005.01.064. PMID 15992592.
- ^ а б Паттерсон Д.Г., Тернер В.Е., Кодилл С.П., Нидхэм Л.Л. (август 2008 г.). «Общий референсный диапазон ТЭ (ПХДД, ПХДФ, cPCB, моно-ПХБ) для населения США в 2001-2002 гг.». Атмосфера. 73 (1 приложение): С261-77. Bibcode:2008Чмсп..73С.261П. Дои:10.1016 / j.chemosphere.2007.08.074. PMID 18511103.
- ^ а б c d е «Информационный бюллетень ВОЗ по СОЗ» (PDF). who.int. Архивировано из оригинал (PDF) на 2011-02-08. Получено 2011-01-31.
- ^ Норен К., Мейроните Д. (2000). «Определенные хлорорганические и броморганические загрязнители в шведском грудном молоке в перспективе последних 20-30 лет». Атмосфера. 40 (9–11): 1111–23. Bibcode:2000Чмсп..40.1111Н. Дои:10.1016 / с0045-6535 (99) 00360-4. PMID 10739053.
- ^ Schecter A, Päpke O, Tung KC, Joseph J, Harris TR, Dahlgren J (март 2005 г.). «Антипирены на основе полибромированных дифениловых эфиров в населении США: текущие уровни, временные тенденции и сравнение с диоксинами, дибензофуранами и полихлорированными бифенилами». Журнал профессиональной и экологической медицины. 47 (3): 199–211. Дои:10.1097 / 01.jom.0000158704.27536.d2. PMID 15761315.
- ^ Fürst P (октябрь 2006 г.). «Диоксины, полихлорированные бифенилы и другие галоорганические соединения в материнском молоке. Уровни, корреляции, тенденции и воздействие при грудном вскармливании». Молекулярное питание и пищевые исследования. 50 (10): 922–33. Дои:10.1002 / mnfr.200600008. PMID 17009213.
- ^ Лигнелл С., Ауне М., Дарнеруд П.О., Кнаттингиус С., Глинн А. (август 2009 г.). "Стойкие хлорорганические и броморганические соединения в материнском молоке из Швеции 1996-2006 гг .: временные тенденции для конкретных соединений". Экологические исследования. 109 (6): 760–7. Bibcode:2009ER .... 109..760L. Дои:10.1016 / j.envres.2009.04.011. PMID 19477439.
- ^ Кивиранта Х, Вартиайнен Т, Туомисто Дж. (Апрель 2002 г.). «Полихлорированные дибензо-п-диоксины, дибензофураны и бифенилы у рыбаков в Финляндии». Перспективы гигиены окружающей среды. 110 (4): 355–61. Дои:10.1289 / ehp.02110355. ЧВК 1240798. PMID 11940453.
- ^ Виттсипе Дж., Эрленкемпер Б., Велге П., Хак А, Вильгельм М. (апрель 2007 г.). «Биодоступность ПХДД / Ф из загрязненной почвы у молодых мини-свиней Геттингена». Атмосфера. 67 (9): С355-64. Bibcode:2007Chmsp..67S.355W. Дои:10.1016 / j.chemosphere.2006.05.129. PMID 17223170.
- ^ Милбрат МО, Венгер Ю., Чанг К. В., Эмонд С., Гарабрант Д., Гиллеспи Б. В., Джоллит О. (март 2009 г.). «Видимые периоды полураспада диоксинов, фуранов и полихлорированных бифенилов в зависимости от возраста, жира в организме, статуса курения и кормления грудью». Перспективы гигиены окружающей среды. 117 (3): 417–25. Дои:10.1289 / ehp.11781. ЧВК 2661912. PMID 19337517.
- ^ Диоксины - ToxFAQ: информационные бюллетени по химическим агентам (CABS)
- ^ а б Хоффман Э., Алимохаммади М., Лайонс Дж., Дэвис Э., Уокер Т.Р., Лейк-CB (август 2019 г.). «Характеристика и пространственное распределение отложений, загрязненных органическими веществами, образовавшихся из исторических промышленных стоков». Экологический мониторинг и оценка. 191 (9): 590. Дои:10.1007 / s10661-019-7763-у. PMID 31444645.
- ^ Допико, М; Гомес, А. (сентябрь 2015 г.). «Обзор текущего состояния и основных источников диоксинов в мире». Журнал Ассоциации управления воздухом и отходами (1995 г.). 65 (9): 1033–49. Дои:10.1080/10962247.2015.1058869. PMID 26068294.
- ^ «Предельное значение ЕС». europa.eu.
- ^ РЕШЕНИЕ КОМИССИИ ПО ВЫПОЛНЕНИЮ (ЕС) 2019/2010 от 12 ноября 2019 г., устанавливающее выводы о наилучших доступных технологиях (НДТ), в соответствии с Директивой 2010/75 / ЕС Европейского парламента и Совета по сжиганию отходов (2019 г.) Официальный вестник Европы Союз L 312/55 https://eur-lex.europa.eu/legal-content/EN/TXT/PDF/?uri=CELEX:32019D2010&from=EN%7CEU Лучшие доступные методы
- ^ Quass U, Fermann M, Bröker G (март 2004 г.). «Европейский проект инвентаризации выбросов диоксинов в атмосферу - окончательные результаты». Атмосфера. 54 (9): 1319–27. Bibcode:2004Чмсп..54.1319Q. Дои:10.1016 / S0045-6535 (03) 00251-0. PMID 14659425.
- ^ а б «Перечень источников и выбросов в окружающую среду диоксиноподобных соединений в США за 1987, 1995 и 2000 годы (финал, ноябрь 2006 г.)». epa.gov.
- ^ «Лесные пожары: основной источник диоксинов». DioxinFacts.org. Получено 3 сентября 2017.
- ^ «Инвентаризация источников диоксинов и выбросов в окружающую среду». EPA. 24 ноября 2014 г.. Получено 3 сентября 2017.
- ^ Мартин, Д., Томида, М., Мичем, Б. (2016) «Воздействие пожара на окружающую среду». Fire Sci Rev 5, 5. Дата обращения 14 сентября 2020.
- ^ Schmitz M, Scheeder G, Bernau S, Dohrmann R, Germann K и др. (Январь 2011 г.). «Диоксины в первичном каолине и вторичных каолинитовых глинах». Экологические науки и технологии. 45 (2): 461–7. Bibcode:2011EnST ... 45..461S. Дои:10.1021 / es103000v. PMID 21126071.
- ^ а б Чунг Квет Йив Н.С., Тироумалешетти М. (июнь 2008 г.). «Уровни диоксина в летучей золе от сжигания жома». Журнал опасных материалов. 155 (1–2): 179–82. Дои:10.1016 / j.jhazmat.2007.11.045. PMID 18166264.
- ^ а б Ли В.С., Чан-Чиен Г.П., Чен С.Дж., Ван Л.С., Ли В.Дж., Ван Ю.Х. (2004). «Удаление полихлорированных дибензо-п-диоксинов и дибензофуранов из дымовых газов скруббером Вентури и рукавным фильтром». Исследование аэрозолей и качества воздуха. 4: 27–37. Дои:10.4209 / aaqr.2004.07.0003.
- ^ Kim SC, Jeon SH, Jung IR, Kim KH, Kwon MH, Kim JH и др. (2001). «Эффективность удаления ПХДД / ПХДФ с помощью устройств контроля загрязнения воздуха в установках для сжигания твердых бытовых отходов». Атмосфера. 43 (4–7): 773–6. Bibcode:2001Чмсп..43..773С. Дои:10.1016 / S0045-6535 (00) 00432-X. PMID 11372864.
- ^ а б Клаас Бернес: Стойкие органические загрязнители. Шведское агентство по охране окружающей среды, Стокгольм, 1998 г. ISBN 91-620-1189-8.
- ^ «Ученые обнаружили бактерии, поедающие диоксины».
- ^ Бунге М., Адриан Л., Краус А., Опель М., Лоренц В. Г., Андрисен Дж. Р. и др. (Январь 2003 г.). «Восстановительное дегалогенирование хлорированных диоксинов анаэробной бактерией». Природа. 421 (6921): 357–60. Bibcode:2003Натура.421..357Б. Дои:10.1038 / природа01237. PMID 12540897.
- ^ а б c Койстинен Дж., Койвусаари Дж., Нууджа И., Паасивирта Дж. (1995). «ПХДЭ, ПХД, ПХДД И ПХДФ в черных кайрах и орланах-белохвостах из Балтийского моря». Атмосфера. 30 (9): 1671–1684. Bibcode:1995Чмсп..30.1671К. Дои:10.1016 / 0045-6535 (95) 00053-Б. ISSN 0045-6535.
- ^ Бык Дж, Фарранд младший (1987). Полевой справочник Общества Одюбона по птицам Северной Америки: Восточный регион. Нью-Йорк: Альфред А. Кнопф. С. 468–9. ISBN 0-394-41405-5
- ^ "Воздействие диоксинов в ЕС и данные о состоянии здоровья за 1999 г." (PDF). europa.eu.
- ^ а б c Лорбер М., Филлипс Л. (июнь 2002 г.). «Воздействие диоксиноподобных соединений в грудном молоке на младенцев». Перспективы гигиены окружающей среды. 110 (6): А325-32. Дои:10.1289 / ehp.021100325. ЧВК 1240886. PMID 12055063. Архивировано из оригинал 27 мая 2010 г.
- ^ Вартиайнен Т., Лампи П., Толонен К., Туомисто Дж. (1995). «Концентрация полихлордибензо-п-диоксина и полихлордибензофурана в донных отложениях и рыбе после загрязнения грунтовых вод хлорфенолами». Атмосфера. 30 (8): 1439–1451. Bibcode:1995Чмсп..30.1439В. Дои:10.1016/0045-6535(95)00037-9. ISSN 0045-6535.
- ^ Эйлуорд Л.Л., Брюнет Р.С., Старр Т.Б., Кэрриер Г, Делзелл Э., Ченг Х., Билл С. (август 2005 г.). «Реконструкция экспозиции для когорты NIOSH, подвергшейся воздействию TCDD, с использованием модели исключения, зависящей от концентрации и возраста». Анализ риска. 25 (4): 945–56. Дои:10.1111 / j.1539-6924.2005.00645.x. PMID 16268942.
- ^ Кимбро Р. Д., Картер С. Д., Лиддл Дж. А., Клайн Р. Р. (1977). «Эпидемиология и патология эпизода отравления тетрахлордибензодиоксином». Архивы гигиены окружающей среды. 32 (2): 77–86. Дои:10.1080/00039896.1977.10667259. PMID 557961.
- ^ «Загрязнение ПХД обнаружено на оборудовании компании по переработке отходов в северной части штата». штат.
- ^ «ПОТЕНЦИАЛ ДЛЯ ОБЛУЧЕНИЯ ЧЕЛОВЕКА» (PDF). Получено 2018-11-14.
- ^ «РЕЧНЫЕ КОНСУЛЬТАЦИИ ПО ПОТРЕБЛЕНИЮ РЫБЫ КАТАВБА резко расширены». catawbariverkeeper.org.
- ^ Ким М., Ким Д.Г., Чой С.В., Герреро П., Норамбуэна Дж., Чанг Г.С. (февраль 2011 г.). «Образование полихлорированных дибензо-п-диоксинов / дибензофуранов (ПХДД / Ф) в процессе переработки оксида цинка, используемого в кормовых добавках: источник загрязнения диоксинами чилийской свинины». Атмосфера. 82 (9): 1225–9. Bibcode:2011Чмсп..82.1225К. Дои:10.1016 / j.chemosphere.2010.12.040. PMID 21216436.
- ^ Туомисто, Йоуко (2011). «Принцип токсической эквивалентности и его применение в оценке риска диоксинов». Рецептор AH в биологии и токсикологии. John Wiley & Sons, Ltd., стр. 317–330. Дои:10.1002 / 9781118140574.ch23. ISBN 9781118140574.