Неосакситоксин - Википедия - Neosaxitoxin
Эта статья слишком полагается на Рекомендации к основные источники. (Июль 2019) (Узнайте, как и когда удалить этот шаблон сообщения) |
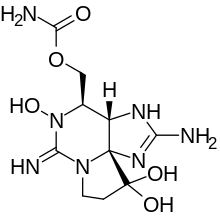 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК | |
| Другие имена 1H, 10H-пирроло (1,2-c) пурин-10,10-диол, 2-амино-4 - (((аминокарбонил) окси) метил) -3a, 4,5,6,8,9-гексагидро- 5-гидрокси-6-имино-, (3aS, 4R, 10aS) -; 1H, 10H-пирроло (1,2-c) пурин-10,10-диол, 2-амино-4 - ((аминокарбонил) окси) метил-3a, 4,5,6,8,9-гексагидро-5- гидрокси-6-имино -, (3aS, 4R, 10aS) -; 1H, 10H-пирроло (1,2-c) пурин-10,10-диол, 2-амино-4 - ((аминокарбонил) окси) метил-3a, 4,5,6,8,9-гексагидро-5- гидрокси-6-имино -, (3aS- (3aalpha, 4alpha, 10aR *)) - | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.237.662 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C10ЧАС17N7О5 | |
| Молярная масса | 315.286 |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
| H300 | |
| P264, P270, P301 + 310, P321, P330, P405, P501 | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Неосакситоксин (NSTX) включен, как и другие сакситоксин - аналоги в широкой группе природных нейротоксических алкалоидов, широко известных как паралитические токсины моллюсков (PST). Исходное соединение PST, сакситоксин (STX), представляет собой трициклический пергидропуриновый алкалоид, который может быть замещен в различных положениях, что дает более 30 встречающихся в природе аналогов STX. Все они являются родственными производными имидазолингуанидиния.[3]
Источники
NSTX и другие PST продуцируются несколькими видами морских динофлагеллят (эукариотами) и пресноводными цианобактериями, сине-зелеными водорослями (прокариотами), которые могут образовывать обширные цветения по всему миру.[4] В особых условиях во время вредоносное цветение водорослей (HAB) или Красная волна, все эти токсины могут накапливаться в моллюсках, питающихся фильтром, таких как мидии, моллюски и устрицы, и могут вызвать вспышку Паралитическое отравление моллюсками (PSP).[5]
Аналоги сакситоксина, ассоциированные с PSP, можно разделить на три категории:[6]
- Карбамат соединения, включая сакситоксин, неосакситоксин и гониаутоксины 1–4.
- N-сульфокарбамоил соединения, включая токсины C и B.
- Декарбамойл соединения в отношении наличия или отсутствия 1-N-гидроксильных, 11-гидроксисульфатных и 21-N-сульфокарбамоильных замещений, а также эпимеризации в положении C-11.
Структура и свойства
NSTX очень похож на сакситоксин, как и все нейротоксины, связанные с PSP, с той лишь разницей, что NSTX показывает одну гидроксильную группу, связанную с азотом «1», где сакситоксин содержит один водород.[7]
Этот пурин очень гидрофильный[8] и термостойкий, он не разрушается при варке.[9] Кроме того, он очень стабилен при обычном хранении, особенно в кислой среде.[10]
Механизм действия
NSTX блокирует внеклеточную часть,[11] внешний вестибюль,[12] некоторых потенциал-управляемых натриевых каналов очень мощным и обратимым образом, без воздействия на другие ионные каналы.
«Стробированные по напряжению», также называемые «чувствительные к напряжению» и «зависимые от напряжения» натриевой канал также известные как «VGSC» или «Nav-канал», являются ключевыми элементами нормальной физиологии у различных животных, включая мух, пиявок, кальмаров и медуз, а также у млекопитающих и позвоночных, не являющихся млекопитающими. Этот большой интегральный мембранный белок играет важную роль в инициировании и распространении потенциалов действия в нейронах, миоцитах и других возбудимых клетках.[13]
Навигационные каналы составляют основу электрическая возбудимость у животных. Навигационные каналы произошли от Ca2+ каналов и присутствовали у общего предка хоанофлагеллят и животных, хотя этот канал, вероятно, был проницаем как для Na+ и Ca2+. Таким образом, как и многие другие нейрональные каналы и рецепторы, Nav-каналы появились раньше нейронов. У беспозвоночных есть два Nav-канала (Nav1 и Nav2), тогда как Nav-каналы позвоночных относятся к семейству Nav1.[14]
Белки натриевых каналов в головном мозге млекопитающих состоят из ассоциации, которая включает одну альфа-субъединицу и одну или несколько вспомогательных бета-субъединиц. Описано девять типов альфа-субъединиц (Nav1,1 к Nav1.9) и десятая родственная изоформа (NaИкс) также может играть некоторую роль в качестве навигационного канала. Основываясь на этой информации, можно описать десять классов Nav: Nav1,1 к Nav1.9, а NaИкс.[15]
Бывшая пятерка,[16] но совсем недавно шесть[17] рецепторы нейротоксина были распознаны между семью рецепторными сайтами[18] расположена в альфа-субъединице рецептора натриевого канала позвоночных:
- Сайт 1 связывает блокаторы натриевых каналов тетродотоксин и сакситоксин.
- Сайт 2 связывает жирорастворимые активаторы натриевых каналов, такие как вератридин.
- Сайт 3 связывает токсины альфа-скорпиона и морского анемона, которые замедляют инактивацию натриевых каналов.
- Сайт 4 связывает токсины бета-скорпиона, которые влияют на активацию натриевых каналов.
- Сайт 5 связывает бреветоксины полиэфирной лестницы и сигуатоксин.
- Сайт 6 связывает дельта-конотоксин.
- Рецептор местного анестетика связывает местные анестетики, антиаритмические и противоэпилептические препараты.
NSTX и другие блокаторы сайта 1 обладают высокой аффинностью (очень низкой константой диссоциации) и высокой специфичностью в отношении каналов Nav. Действие NSTX оказывает минимальное влияние на сердечный Nav, где он проявляет примерно в 20-60 раз меньшее сродство, чем Nav-каналы из скелетных мышц и мозга крысы.[19] Большинство данных подчеркивает роль «устойчивого к STX» Na.v канал 1,5 в сердце человека.[20][21]
Токсины, такие как неосакситоксин и тетродотоксин, имеют меньшее сродство к большинству сердечных Nav-каналов, чем к большинству Nav-каналов в нервной ткани. Более того, NSTX настолько активен в нервном канале, что примерно в миллион раз более эффективен, чем лидокаин.[22]
Воздействие на человека
Этот механизм действия может вызывать у человека два хорошо известных эффекта:
Токсический эффект, связанный с плазматическими уровнями NSTX
Его можно приблизительно описать с помощью одной из классических моделей нейротоксического заболевания, известного с древних времен как красный прилив, наиболее вредоносное цветение водорослей (ВЦВ). Эта хорошо известная клиническая модель - «паралитическое отравление моллюсками».[23]
Конечно, цветение разных водорослей сильно различается,[24][25][26][27] из-за смешения видов, включенных в каждую ВЦВ, обычно связанных с условиями окружающей среды;[28] из-за уровней и качества PST, продуцируемых в каждом HAB, это может модулироваться сопутствующим микроорганизмом;[29][30][31][32] и, наконец, что не менее важно, из-за специфических свойств каждого типа PST, например:
- Бреветоксины - это жирорастворимые (гидрофобные) морские токсины на основе простых полиэфиров; их преобладающее действие является возбуждающим (блокируется тетродотоксином), опосредованным увеличением клеточного Na+ приток; и связываются с сайтом 5 на Nav (как сигуатоксин).[33]
- Токсичность тетродотоксина (ТТХ) связана с выраженными и неожиданными сердечно-сосудистыми эффектами (например, гипотензией и брадикардией).[34] Эти эффекты являются неожиданными из-за печально известной устойчивости к ТТХ, наблюдаемой в сердечном канале позвоночных. Более того, эта характеристика сердечного Nav-канала млекопитающих объясняется преобладанием в сердце изоформы ТТХ-резистентного Nav-канала (Nav1.5).[35] Напротив, как предполагается на физиологической основе, NSTX вызывает лишь легкие и преходящие сердечно-сосудистые нарушения во время экспериментальной интоксикации (нет данных о клинической токсичности чистого NSTX).
- STX имеет два положительных заряда, в отличие от одиночного заряда TTX и GTX2 / 3, естественного конгенера STX с чистым зарядом +1. Ввиду их довольно различных структур неудивительно, что STX и TTX по-разному связываются с VGSC. Фактически, когда Phe 385 рядом с фильтром селективности Nav1.2 мутирован в Cys, сродство канала к TTX снижается в 3000 раз, тогда как для STX снижается (только) в 340 раз.[36]
- Имеются очень ограниченные данные об относительной эффективности различных PST, и разработка методов, альтернативных биотестам животных, для обнаружения морских токсинов является насущной необходимостью.[37]
Несмотря на неоднородную и плохо изученную эпидемиологию, клиническая картина PSP может быть полезна для прогнозирования клинических эффектов системного NSTX.
- В наиболее частой и доброкачественной ситуации пациент страдает легкой кратковременной парестезией рта или конечностей.
- В умеренных случаях может наблюдаться периоральное покалывание, переходящее в онемение, распространяющееся на лицо и шею.[38]
- В тяжелых случаях у пациента может развиться апноэ вследствие моторного блока, требующего искусственной вентиляции легких.[39]
Обычно у пострадавших от легкой и тяжелой острой интоксикации токсин выводится с мочой в течение первых 24 часов после приема внутрь и улучшается до полного выздоровления в первый день внутрибольничной помощи (когда жизненно важная поддержка оказывается своевременно).[40]
Когда вспышки PSP происходят в отдаленных районах, где медицинская помощь ограничена, зарегистрированная летальность составляет менее 10% у взрослых, но может достигать 50% у детей младше шести лет. Это различие могло быть вторичным по отношению к разным дозам и составу задействованных смесей PST; задержка в оказании медицинской помощи; или какая-то восприимчивость детей.[41] Более свежая информация предполагает, что летальность может составлять около 1% пациентов с симптомами.[42] включая случаи, когда требовалась воздушная транспортировка из отдаленных мест Аляски.[43]
Электрофизиологические наблюдения продемонстрировали субклинические нарушения, сохраняющиеся в течение нескольких дней.[44] или недели[45] после клинического выздоровления.
Некоторые данные свидетельствуют о наличии метаболических путей последовательного окисления и глюкуронизации PST in vitro, которые являются начальными реакциями детоксикации для выведения этих токсинов у людей.[46]
Судебно-медицинский анализ смертельных случаев после тяжелых случаев пришел к выводу, что токсины PSP метаболически трансформируются человеком и выводятся из организма путем выделения с мочой и фекалиями, как и любые другие ксенобиотические соединения.[47]
Учитывая гетерогенный характер смесей токсинов, содержащихся в зараженных двустворчатых моллюсках, безопасный предел содержания токсина в моллюсках, пригодный для употребления в пищу человеком, выражается в «эквивалентах сакситоксина». По данным Продовольственной и сельскохозяйственной организации Объединенных Наций (ФАО) и Европейского парламента, этот предел составляет 80 микрограммов эквивалента сакситоксина на 100 граммов мяса мидий (каждая мидия весит около 23 г).[48][49] Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США применяет то же определение к качеству «рыбы», но термин «рыба» относится к пресноводным или морским плавниковым рыбам, ракообразным, другим формам водных животных, кроме птиц или млекопитающих, и всем моллюскам; и включить использование «ppm» в качестве другой меры для эквивалентной концентрации сакситоксина в упомянутых пищевых продуктах.[50]
Как это ни парадоксально, хроническое и / или повторяющееся воздействие токсинов морских морепродуктов, что является гораздо более реалистичным явлением, полностью не изучено.[51][52] Одно исследование на крысах, подвергавшихся хроническому (12 недель) введению NSTX, продемонстрировало некоторое снижение потребления воды и пищи и умеренную степень преходящего холестаза, вероятно, связанного с голоданием, без других аномалий.[53]
Анестезирующий эффект, вызванный местной инфильтрацией NSTX
Это действие было продемонстрировано на животных.[54] и люди.[55][56][57][58]
Медицинское применение обезболивающего эффекта NSTX подтверждается тремя причинами:
- Продолжительность анестезии NSTX:
- Любой доступный в настоящее время местный анестетик практически не дает клинических эффектов через 12 часов после однократной инъекции.[59] Затем, в случае сильной или продолжительной боли, некоторым пациентам необходимы повторные инъекции, катетеры, помпы и опиоиды.[60][61] чувствовать себя комфортно, с различными побочными эффектами, затратами и рисками.[62]
- С другой стороны, местная инфильтрация NSTX обеспечивает длительную анестезию, намного превосходящую все доступные местные анестетики. Некоторые исследования продемонстрировали анестезирующее действие, продолжающееся более одной недели после однократной инъекции у грызунов при использовании состава с пролонгированным высвобождением, без гистологических или функциональных последствий.[63]
- Кроме того, два отчета о людях продемонстрировали сильное усиление анестезирующего эффекта NSTX, бупивакаин и адреналин.[64][65]
- Местная безопасность NSTX:
- Все доступные местные анестетики связаны с местным повреждением в разных моделях.[66][67][68][69][70] Этот нежелательный эффект может быть усилен составами с замедленным высвобождением.[71]
- Напротив, несколько исследований показывают местную безопасность нейротоксинов, связанных с сакситоксином, включая очень чувствительные модели, и нет никаких оснований предполагать иное для NSTX.[72][73][74][75]
- Системная безопасность NSTX:
- Несмотря на успехи инъекций под ультразвуковым контролем, острая системная токсичность местных анестетиков все еще остается нерешенной клинической проблемой и может иметь разрушительные последствия, связанные с неврологическими и сердечно-сосудистыми эффектами всех доступных местных анестетиков.[76][77]
- В остальном клинический опыт и модели на животных показывают относительную безопасность случайной и экспериментальной интоксикации NSTX (когда своевременно предоставляется соответствующая поддерживающая терапия).[78]
- Недавние исследования у овец показали безопасный предел, связанный с моторным блоком, более 1 мкг / кг для внутривенной инъекции NSTX, с полным восстановлением после короткого курса механической вентиляции.[79]
- Что касается системной безопасности, сакситоксины проникают через гематоэнцефалический барьер,[80] но из-за специфичности Nav-каналов острая токсичность связана с очень низким риском судорог. Это устанавливает важное отличие от текущей токсичности местных анестетиков.[81]
- Как можно было предположить по его селективности ионного канала,[82] Клиническая картина интоксикации NSTX практически лишена аритмий, что свидетельствует о другом различии с многочисленными сердечными эффектами доступных местных анестетиков.[83]
- И, наконец, что не менее важно, можно наблюдать некоторое улучшение терапевтического индекса NSTX при смешивании с бупивакаином и / или адреналином.[84]
В заключение, NSTX - это четко определенная молекула, имеющая длительные и иногда опасные отношения с людьми. Недавние исследования предполагают клиническое применение в качестве нового местного анестетика, что звучит «слишком хорошо, чтобы быть правдой», но требуются дополнительные исследования.[85]
Смотрите также
Рекомендации
- ^ Национальная медицинская библиотека США (NLM). ChemoIDplus Advanced. Регистрационный номер: 64296-20-4 (дата обращения: 12 мая 2012 г.) [1]
- ^ Национальный центр биотехнологической информации (NCBI). PubChem Compound (дата обращения: 12 мая 2012 г.) [2]
- ^ Михали Т.К., Келлманн Р., Нейлан Б.А. (март 2009 г.). "Характеристика кластеров генов биосинтеза паралитического токсина моллюсков в Анабаена циркиналис AWQC131C и Aphanizomenon sp. NH-5 ". BMC Биохимия. 10: 8. Дои:10.1186/1471-2091-10-8. ЧВК 2679770. PMID 19331657.
- ^ Визе М., Д'Агостино П.М., Михали Т.К., Моффитт М.С., Нейлан Б.А. (июль 2010 г.). «Нейротоксические алкалоиды: сакситоксин и его аналоги». Морские препараты. 8 (7): 2185–2211. Дои:10.3390 / md8072185. ЧВК 2920551. PMID 20714432.
- ^ Центры по контролю и профилактике заболеваний (CDC). Лабораторный ответ CDC на токсины (дата обращения: 8 мая 2012 г.) [3]
- ^ Ван Д.З. (март 2008 г.). «Нейротоксины морских динофлагеллят: краткий обзор». Морские препараты. 6 (3): 349–71. Дои:10.3390 / md6020349. ЧВК 2525493. PMID 18728731.
- ^ Ху SL, Као CY (март 1991 г.). «Взаимодействие неосакситоксина с натриевым каналом волокна скелетных мышц лягушки». Журнал общей физиологии. 97 (3): 561–78. Дои:10.1085 / jgp.97.3.561. ЧВК 2216488. PMID 1645395.
- ^ Этеридж С.М. (август 2010 г.). «Паралитическое отравление моллюсками: безопасность морепродуктов и перспективы здоровья человека». Токсикон. 56 (2): 108–22. Дои:10.1016 / j.toxicon.2009.12.013. PMID 20035780.
- ^ Лоуренс Дж. Ф., Махер М., Уотсон-Райт В. (январь 1994 г.). «Влияние приготовления пищи на концентрацию токсинов, связанных с паралитическим ядом моллюсков в гепатопанкреасе омаров». Токсикон. 32 (1): 57–64. Дои:10.1016/0041-0101(94)90021-3. PMID 9237337.
- ^ Альфонсо А., Louzao MC, Vieytes MR, Botana LM (декабрь 1994 г.). «Сравнительное исследование стабильности сакситоксина и неосакситоксина в кислых растворах и лиофилизированных образцах». Токсикон. 32 (12): 1593–8. Дои:10.1016/0041-0101(94)90318-2. PMID 7725328.
- ^ Tarnawa I, Bölcskei H, Kocsis P (январь 2007 г.). «Блокаторы потенциал-управляемых натриевых каналов для лечения заболеваний центральной нервной системы». Последние патенты на открытие лекарств для ЦНС. 2 (1): 57–78. Дои:10.2174/157488907779561754. PMID 18221218.
- ^ Penzotti JL, Lipkind G, Fozzard HA, Dudley SC Jr (февраль 2001 г.). "Специфические взаимодействия неосакситоксина с Na+ наружный вестибюль канала определяется анализом мутантного цикла ". Биофизический журнал. 80 (2): 698–706. Bibcode:2001BpJ .... 80..698P. Дои:10.1016 / S0006-3495 (01) 76049-3. ЧВК 1301268. PMID 11159437.
- ^ Catterall WA. (Апрель 2012 г.). "Натриевые каналы, управляемые напряжением в 60 лет: структура, функции и патофизиология". Журнал физиологии. 590 (Pt 11): 2577–89. Дои:10.1113 / jphysiol.2011.224204. ЧВК 3424717. PMID 22473783.
- ^ Закон Х. (июнь 2012 г.). «Адаптивная эволюция потенциалозависимых натриевых каналов: первые 800 миллионов лет». Труды Национальной академии наук Соединенных Штатов Америки. 109 (Приложение 1): 10619–25. Дои:10.1073 / pnas.1201884109. ЧВК 3386883. PMID 22723361.
- ^ Ю. Ф. Х., Каттералл В. А. (июль 2003 г.). «Обзор семейства натриевых каналов с регулируемым напряжением». Геномная биология. 4 (3): 207. Дои:10.1186 / gb-2003-4-3-207. ЧВК 153452. PMID 12620097.
- ^ Файнзильбер М., Кофман О., Злоткин Е., Гордон Д. (январь 1994 г.). «Новый участок рецептора нейротоксина на натриевых каналах идентифицируется конотоксином, который влияет на инактивацию натриевых каналов у моллюсков и действует как антагонист в мозге крысы» (PDF). Последние патенты на открытие лекарств для ЦНС. 269 (4): 2574–80. PMID 8300586. Получено 9 мая, 2012.
- ^ Ван Дж., Яров-Яровой В., Кан Р., Гордон Д., Гуревиц М., Шойер Т., Каттералл В. А. (сентябрь 2011 г.). «Картирование рецепторного сайта для токсинов альфа-скорпиона на Na+ датчик напряжения канала ". PNAS. 108 (37): 15426–31. Bibcode:2011PNAS..10815426W. Дои:10.1073 / pnas.1112320108. ЧВК 3174582. PMID 21876146.
- ^ Каттералл, В. А., Голдин А. Л., Ваксман С. Г. (декабрь 2005 г.). "Международный союз фармакологии. XLVII. Номенклатура и взаимосвязь между структурой и функцией потенциалзависимых натриевых каналов". Фармакологические обзоры. 57 (4): 397–409. Дои:10.1124 / пр.57.4.4. PMID 16382098. S2CID 7332624.
- ^ Guo XT, Uehara A, Ravindran A, Bryant SH, Hall S, Moczydlowski E (декабрь 1987 г.). «Кинетическая основа нечувствительности к тетродотоксину и сакситоксину в натриевых каналах сердца собак и денервированных скелетных мышцах крыс». Биохимия. 26 (24): 7546–56. Дои:10.1021 / bi00398a003. PMID 2447944.
- ^ Лоу Дж. С., Палыгин О., Бхасин Н., Хунд Т. Дж., Бойден П. А., Шибата Е., Андерсон М. Е., Молер П. Дж. (Январь 2008 г.). «Для нацеливания управляемых напряжением каналов навигации в сердце требуется анкирин-G-зависимый клеточный путь». Журнал клеточной биологии. 180 (1): 173–86. Дои:10.1083 / jcb.200710107. ЧВК 2213608. PMID 18180363.
- ^ Абриэль Х (7 мая 2012 г.). "Сердечный натриевый канал Nav1.5 Ранолазин подавляет механочувствительность ». Тираж. 125 (22): 2681–3. Дои:10.1161 / CIRCULATIONAHA.112.110908. PMID 22565937.
- ^ Баттерворт Дж. Ф. 4-е место (март – апрель 2011 г.). «Скоро ли традиционные местные анестетики заменят нейротоксины?». Регионарная анестезия и обезболивающее. 36 (2): 101–2. Дои:10.1097 / AAP.0b013e31820db23e. PMID 21326065. S2CID 33189422.
- ^ ДОКУМЕНТ ФАО ПО ПРОДУКТАМ И ПИТАНИЮ 80. Продовольственная и сельскохозяйственная организация Объединенных Наций. Глава 2. Паралитическое отравление моллюсками (PSP). Рим, 2004 г. (дата обращения: 6 мая 2012 г.)[4][постоянная мертвая ссылка ]
- ^ Салфате О, Васкес Дж., Гальван Дж., Санчес А., Назар А. (май – июнь 1991 г.). "Intoxicaciones por toxina paralizante de molusco en Oaxaca" (PDF). Salud Pública de México (на испанском). 33 (3): 240–7. Получено 10 мая, 2012.
- ^ Андерсон Д.М. (август 1994 г.). «Красные приливы». Scientific American. 271 (2): 62–8. Bibcode:1994SciAm.271b..62A. Дои:10.1038 / scientificamerican0894-62. PMID 8066432. (дата обращения: 9 мая 2012 г.) [5]
- ^ Сивонен К., Джонс Г. (1999). «3. Цианобактериальные токсины» (PDF). В Припеве I, Бартрам Дж. (Ред.). Токсичные цианобактерии в воде: руководство по их последствиям для здоровья населения, мониторингу и управлению. Всемирная организация здоровья. ISBN 0-419-23930-8. Архивировано из оригинал в 1999 году. Получено 10 мая 2012. [6]
- ^ Глиберт PM, Андерсон DM, Gentien P, Granéli E, Sellner KG (июнь 2005 г.). «Глобальные сложные явления вредоносного цветения водорослей». Океанография. 18 (2): 136–47. Дои:10.5670 / oceanog.2005.49.(дата обращения: 11 мая 2012 г.) [7] В архиве 2006-05-10 на Wayback Machine
- ^ Хаяси М., Янаги Т. (2008). «Анализ изменения видов красных приливов в устье реки Йодо с помощью численной модели экосистемы» (PDF). Бюллетень загрязнения морской среды. 57 (1–5): 103–7. Дои:10.1016 / j.marpolbul.2008.04.015. PMID 18513758.
- ^ Галлахер С., Флинн К.Дж., Франко Дж. М., Брюггеман Э. Э., Хайнс Х. Б. (январь 1997 г.). «Доказательства продукции паралитических токсинов моллюсков бактериями, связанными с Alexandrium spp. (Dinophyta) в культуре». Прикладная и экологическая микробиология. 63 (1): 239–45. Дои:10.1128 / AEM.63.1.239-245.1997. ЧВК 168316. PMID 9065273.
- ^ Grzebyk D, Denardou A, Berland B, Pouchus YF (август 1997 г.). «Свидетельства наличия нового токсина в минимуме динофлагеллат Prorocentrum красного прилива» (PDF). Журнал исследований планктона. 19 (8): 1111–24. Дои:10.1093 / планкт / 19.8.1111. Получено 9 мая, 2012.
- ^ Чжэн Т.Л., Су Дж.К., Маскауи К., Ю З.М., Ху З., Сюй Дж.С., Хун Х.С. (2005). «Микробная модуляция в биомассе и производстве токсинов водорослями, вызывающими красный прилив». Бюллетень загрязнения морской среды. 51 (8–12): 1018–25. Дои:10.1016 / j.marpolbul.2005.02.039. PMID 16291201.
- ^ Алонсо Родригес Р., Очоа Дж. Л., Урибе Алкосер М. (январь – июнь 2005 г.). «Выпас гетеротрофной динофлагелляты. Noctiluca scintillans (Макартни) Кофоид на Gymnodinium catenatum Graham ". Revista Latinoamericana de Microbiología. 47 (1–2): 6–10. PMID 17061541.
- ^ Баден Д.Г. (май 1989 г.). «Бреветоксины: уникальные токсины полиэфирных динофлагеллят». Журнал FASEB. 3 (7): 1807–17. Дои:10.1096 / fasebj.3.7.2565840. PMID 2565840. S2CID 44847897.
- ^ Как СК, Черн СН, Хуанг Ю.К., Ван Л.М., Ли СН (январь 2003 г.). «Отравление тетродотоксином». Американский журнал неотложной медицины. 21 (1): 51–4. Дои:10.1053 / ajem.2003.50008. PMID 12563582.
- ^ Ворнанен М, Хассинен М, Хаверинен Дж (2011). «Тетродотоксиновая чувствительность сердца позвоночных Na+ Текущий". Морские препараты. 9 (11): 2409–22. Дои:10.3390 / md9112409. ЧВК 3229242. PMID 22163193.
- ^ Zhang MM, Gruszczynski P, Walewska A, Bulaj G, Olivera BM, Yoshikami D (июль 2010 г.). «Захват внешнего преддверия потенциалзависимых натриевых каналов микроконотоксином KIIIA и сакситоксином или тетродотоксином». Журнал нейрофизиологии. 104 (1): 88–97. Дои:10.1152 / ян.00145.2010. ЧВК 2904204. PMID 20410356.
- ^ Перес С., Вале С., Ботана А.М., Алонсо Э., Вейтес М.Р., Ботана Л.М. (июль 2011 г.). «Определение факторов эквивалента токсичности паралитических токсинов моллюсков электрофизиологическими измерениями в культивируемых нейронах». Химические исследования в токсикологии. 24 (7): 1153–7. Дои:10.1021 / tx200173d. PMID 21619049.
- ^ Океанографическое учреждение Вудс-Хоул. Паралитическое отравление моллюсками. Флеминг Л.Е. Последнее обновление: 7 мая 2008 г. (дата обращения: 8 мая 2012 г.)[8]
- ^ Yuen CW, Ng MH (апрель 2002 г.). «Респираторная недостаточность после употребления в пищу морских улиток» (PDF). Гонконгский журнал экстренной медицины. 9 (3): 159–61. Дои:10.1177/102490790200900308. S2CID 115428542. Получено 6 мая, 2012.
- ^ Центры по контролю и профилактике заболеваний (CDC) (декабрь 2011 г.). «Паралитическое отравление моллюсками на юго-востоке Аляски, май – июнь 2011 г.». Еженедельный отчет о заболеваемости и смертности. 60 (45): 1554–56. PMID 22089968.(дата обращения: 8 мая 2012 г.)[9]
- ^ Родриг, округ Колумбия, Эцель Р.А., Холл S, де Поррас Е., Веласкес О.Н., Токс Р.В., Килбурн Е.М., Блейк, Пенсильвания (март 1990 г.). «Смертельное паралитическое отравление моллюсками в Гватемале». Американский журнал тропической медицины и гигиены. 42 (3): 267–71. Дои:10.4269 / ajtmh.1990.42.267. PMID 2316796.
- ^ Cheng HS, Chua SO, Hung JS, Yip KK (апрель 1991 г.). «Повышение уровня креатинкиназы MB при паралитическом отравлении моллюсками» (PDF). Грудь. 99 (4): 1032–3. Дои:10.1378 / сундук.99.4.1032. PMID 2009759. Получено 9 мая, 2012.[постоянная мертвая ссылка ]
- ^ Gessner BD, Middaugh JP (апрель 1995 г.). «Паралитическое отравление моллюсками на Аляске: ретроспективный анализ за 20 лет». Американский журнал эпидемиологии. 141 (8): 766–70. Дои:10.1093 / oxfordjournals.aje.a117499. PMID 7709919.
- ^ Лонг Р.Р., Сарджент Дж. К., Хаммер К. (август 1990 г.). «Паралитическое отравление моллюсками. История болезни и серийные электрофизиологические наблюдения». Неврология. 40 (8): 1310–2. Дои:10.1212 / wnl.40.8.1310. PMID 2381544. S2CID 33896985.
- ^ де Карвалью М., Хасинто Дж., Рамос Н., де Оливейра В., Пинхо и Мело Т., де Са Дж. (август 1998 г.). «Паралитическое паралитическое отравление моллюсками: клинические и электрофизиологические наблюдения». Журнал неврологии. 245 (8): 551–4. Дои:10.1007 / s004150050241. PMID 9747920. S2CID 29180723.
- ^ Гарсия К., Баррига А., Диас Дж. К., Лагос М., Лагос Н. (январь 2010 г.). «Паралитический путь метаболизма и детоксикации паралитических токсинов моллюсков у человека». Токсикон. 55 (1): 135–44. Дои:10.1016 / j.toxicon.2009.07.018. HDL:10533/141436. PMID 19632259.
- ^ Гарсия К., дель Кармен Браво М., Лагос М., Лагос Н. (февраль 2004 г.). «Паралитическое отравление моллюсками: посмертный анализ образцов тканей и биологических жидкостей человеческих жертв во фьордах Патагонии». Токсикон. 43 (2): 149–58. Дои:10.1016 / j.toxicon.2003.11.018. PMID 15019474.
- ^ Документ ФАО по продовольствию и питанию 80. Продовольственная и сельскохозяйственная организация Объединенных Наций. Глава 8. Оценка рисков. Rome, 2004. (дата обращения: 6 мая 2012 г.). [10][постоянная мертвая ссылка ]
- ^ Европейский парламент и Совет Европейского Союза (апрель 2004 г.). «Регламент (ЕС) № 853/2004 Европейского парламента и Совета от 29 апреля 2004 г., устанавливающий особые правила гигиены для пищевых продуктов животного происхождения». Off J Eur Comm. 139: 61. (дата обращения: 6 мая 2012 г.)[11]
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Руководство по опасностям и мерам контроля в отношении рыбы и рыбных продуктов, четвертое издание, ноябрь 2011 г. Глава 6: Природные токсины (стр. 99–112). (дата обращения: 6 мая 2012 г.) [12] [13]
- ^ Океанографическое учреждение Вудс-Хоул. Морские биотоксины и вредные водоросли: национальный план. Глава II. ТОКСИНЫ. Оценка рисков. (дата обращения: 8 мая 2012 г.)[14]
- ^ Batoréu MC, Dias E, Pereira P, Franca S (май 2005 г.). «Риск воздействия паралитических токсинов водорослевого происхождения на человека». Экологическая токсикология и фармакология. 19 (3): 401–6. Дои:10.1016 / j.etap.2004.12.002. PMID 21783504.
- ^ Зепеда Р.Дж., Кандираччи М., Лобос Н., Люкс С., Миранда Х.Ф. (сентябрь 2014 г.). «Исследование хронической токсичности неосакситоксина у крыс». Морские препараты. 12 (9): 5055–71. Дои:10.3390 / md12095055. ЧВК 4178483. PMID 25257789.
- ^ Кохан Д.С., Лу Н.Т., Гекгёль-Клайн А.С., Шубина М., Куанг Ю., Холл С., Стрихарц Г.Р., Берде CB (январь – февраль 2000 г.). «Местные анестезирующие свойства и токсичность гомологов сакситонина для блокады седалищного нерва крысы in vivo». Регионарная анестезия и обезболивающее. 25 (1): 52–9. Дои:10.1097/00115550-200001000-00010. PMID 10660241.
- ^ Родригес-Наварро А.Дж., Лагос Н., Лагос М., Брагетто I, Чендес А., Гамильтон Дж., Бергер З., Видмайер Г., Энрикес А. (ноябрь 2006 г.). «Внутрисфинктерная инъекция неосакситоксина: свидетельство расслабления нижнего сфинктера пищевода при ахалазии». Американский журнал гастроэнтерологии. 101 (11): 2667–8. PMID 17090291.
- ^ Родригес-Наварро А.Дж., Лагос Н., Лагос М., Брагетто I, Чендес А., Гамильтон Дж., Фигероа С., Труан Д., Гарсия С., Рохас А., Иглесиас В., Брюнет Л., Альварес Ф. (февраль 2007 г.). «Неосакситоксин как местный анестетик: предварительные наблюдения первого испытания на людях». Анестезиология. 106 (2): 339–45. Дои:10.1097/00000542-200702000-00023. PMID 17264729. S2CID 19507764.
- ^ Родригес-Наварро AJ, Berde CB, Wiedmaier G, Mercado A, Garcia C, Iglesias V, Zurakowski D (март – апрель 2011 г.). «Сравнение неосакситоксина и бупивакаина через инфильтрацию порта для послеоперационной анальгезии после лапароскопической холецистэктомии: рандомизированное двойное слепое исследование». Регионарная анестезия и обезболивающее. 36 (2): 103–9. Дои:10.1097 / aap.0b013e3182030662. PMID 21425506. S2CID 37539195.
- ^ Манрикес В., Кастро Каперан Д., Гусман Р., Насер М., Иглесиа В., Лагос Н. (2015). «Первое свидетельство неосакситоксина как блокатора боли длительного действия при болевом синдроме мочевого пузыря». Int Urogynecol J. 26 (6): 853–8. Дои:10.1007 / s00192-014-2608-2. PMID 25571865. S2CID 22432232.
- ^ Леоне С., Ди Чианни С., Касати А., Фанелли Дж. (Август 2008 г.).«Фармакология, токсикология и клиническое использование новых местных анестетиков длительного действия, ропивакаина и левобупивакаина». Acta Biomedica. 79 (2): 92–105. PMID 18788503. (дата обращения: 10 мая 2012 г.) [15] В архиве 2011-12-16 на Wayback Machine
- ^ Обрун Ф., Мазойт Дж. Х., Риу Б. (февраль 2012 г.). «Послеоперационное внутривенное титрование морфина». Британский журнал анестезии. 108 (2): 193–201. Дои:10.1093 / bja / aer458. PMID 22250276.
- ^ Бейлин Ю., Хальперн С. (август 2012 г.). «Целенаправленный обзор: ропивакаин по сравнению с бупивакаином для эпидуральной анальгезии родов». Анестезия и анальгезия. 111 (2): 482–7. Дои:10.1213 / ANE.0b013e3181e3a08e. PMID 20529986.
- ^ Ву К.Л., Раджа С.Н. (июнь 2011 г.). «Лечение острой послеоперационной боли». Ланцет. 377 (9784): 2215–25. Дои:10.1016 / S0140-6736 (11) 60245-6. PMID 21704871. S2CID 13140529.
- ^ Эпштейн-Бараш Х., Шичор И., Квон А.Х., Холл С., Лоулор М.В., Лангер Р., Кохан Д.С. (апрель 2009 г.). «Местная анестезия длительного действия с минимальной токсичностью». Труды Национальной академии наук Соединенных Штатов Америки. 106 (17): 7125–30. Bibcode:2009PNAS..106.7125E. Дои:10.1073 / pnas.0900598106. ЧВК 2678453. PMID 19365067.
- ^ Родригес-Наварро А.Дж., Лагос М., Фигероа С., Гарсия С., Рекабаль П., Сильва П., Иглесиас В., Лагос Н. (ноябрь 2009 г.). «Усиление местной анестезирующей активности неосакситоксина с помощью бупивакаина или адреналина: разработка блокатора боли длительного действия». Исследования нейротоксичности. 16 (4): 408–15. Дои:10.1007 / s12640-009-9092-3. PMID 19636660. S2CID 23287251.
- ^ Лобо К., Донадо С., Корнелиссен Л., Ким Дж., Ортис Р., Пик Р. В., Келлог М., Александр М. Е., Зураковский Д., Курганский К. Э., Пейтон Дж., Бильге А., Борецкий К., Макканн М. Е., Берде CB, Краверо Дж. (Октябрь 2015 г. ). «Фаза 1, повышение дозы, двойное слепое, блочно-рандомизированное, контролируемое испытание безопасности и эффективности неосакситоксина в отдельности и в комбинации с 0,2% бупивакаином, с эпинефрином и без него для кожной анестезии». Анестезиология. 123 (4): 873–85. Дои:10.1097 / ALN.0000000000000831. PMID 26275090. S2CID 22740054.
- ^ Цинк В., Граф Б. (июль – август 2004 г.). «Обзорные статьи: Миотоксичность местного анестетика». Регионарная анестезия и обезболивающее. 29 (4): 333–40. Дои:10.1016 / j.rapm.2004.02.008. PMID 15305253. S2CID 26185858.
- ^ Bogatch MT, Ferachi DG, Kyle B, Popinchalk S, Howell MH, Ge D, You Z, Savoie FH (июнь 2006 г.). «Цитотоксичность лидокаина или бупивакаина на эндотелиальных клетках роговицы на модели кролика». Роговица. 25 (5): 590–6. Дои:10.1097 / 01.ico.0000220775.93852.02. PMID 16783149. S2CID 21454799.
- ^ Перес-Кастро Р., Патель С., Гаравито-Агилар З. В., Розенберг А., Ресио-Пинто Е., Чжан Дж., Бланк Т. Дж., Сюй Ф. (март 2009 г.). «Цитотоксичность местных анестетиков в нейрональных клетках человека». Анестезия и обезболивание. 108 (3): 997–1007. Дои:10.1213 / ane.0b013e31819385e1. PMID 19224816. S2CID 41982515.
- ^ Nouette-Gaulain K, Dadure C, Morau D, Pertuiset C, Galbes O, Hayot M, Mercier J, Sztark F, Rossignol R, Capdevila X (ноябрь 2009 г.). «Возрастозависимая мышечная токсичность, вызванная бупивакаином во время непрерывной блокады периферических нервов у крыс». Анестезиология. 111 (5): 1120–7. Дои:10.1097 / ALN.0b013e3181bbc949. PMID 19809284.
- ^ Bogatch MT, Ferachi DG, Kyle B, Popinchalk S, Howell MH, Ge D, You Z, Savoie FH (март 2010 г.). «Является ли химическая несовместимость причиной гибели хондроцитов, вызванной местными анестетиками?». Американский журнал спортивной медицины. 38 (3): 520–6. Дои:10.1177/0363546509349799. PMID 20194957. S2CID 8766478.
- ^ Падера Р., Беллас Э., Цзе Дж.Й., Хао Д., Кохане Д.С. (май 2008 г.). «Местная миотоксичность от длительного высвобождения бупивакаина из микрочастиц». Анестезиология. 108 (5): 921–8. Дои:10.1097 / ALN.0b013e31816c8a48. ЧВК 3939710. PMID 18431129.
- ^ Габликс Дж., Бартер С. (апрель – сентябрь 1987 г.). «Сравнительная цитотоксичность афлатоксина B1 и сакситоксина в культурах клеток». Молекулярная токсикология. 1 (2–3): 209–16. PMID 3130568.
- ^ Шварц Д.М., Дункан К.Г., Филдс Х.Л., Джонс М.Р. (октябрь 1998 г.). «Тетродотоксин: анестезирующая активность в деэпителизированной роговице». Архив клинической и экспериментальной офтальмологии Грефе. 236 (10): 790–4. Дои:10.1007 / s004170050160. PMID 9801896. S2CID 25050842.
- ^ Дункан К.Г., Дункан Дж. Л., Шварц Д.М. (август 2001 г.). «Сакситоксин: анестетик дипителизированной роговицы кролика». Роговица. 20 (6): 639–42. Дои:10.1097/00003226-200108000-00016. PMID 11473167. S2CID 24304236.
- ^ Падера РФ, Це Дж.Й., Беллас Э., Кохане Д.С. (декабрь 2006 г.). «Тетродотоксин для пролонгированной местной анестезии с минимальной миотоксичностью». Мышечный нерв. 34 (6): 747–53. Дои:10.1002 / mus.20618. PMID 16897761.
- ^ Диллан Д., Finucane BT (апрель 2010 г.). «Системная токсичность местных анестетиков». Канадский журнал анестезии. 57 (4): 368–80. Дои:10.1007 / s12630-010-9275-7. PMID 20151342.
- ^ Нил Дж. М., Бернардс С. М., Баттерворт Дж. Ф., Ди Грегорио Дж., Драснер К., Хейтманк М. Р., Малрой М. Ф., Розенквист Р. У., Вайнберг Г. Л. (март – апрель 2010 г.). «Практические рекомендации ASRA по поводу системной токсичности местных анестетиков». Регионарная анестезия и обезболивающее. 35 (2): 152–61. Дои:10.1097 / AAP.0b013e3181d22fcd. PMID 20216033. S2CID 8548084.
- ^ Popkiss ME, Horstman DA, Harpur D (июнь 1979 г.). «Паралитическое отравление моллюсками. Отчет о 17 случаях в Кейптауне». Южноафриканский медицинский журнал. 55 (25): 1017–23. PMID 573505. (дата обращения: 8 мая 2012 г.)[16]
- ^ Wylie MC, Johnson VM, Carpino E, Mullen K, Hauser K, Nedder A, Kheir JN, Rodriguez-Navarro AJ, Zurakowski D, Berde CB (март 2012 г.). «Дыхательные, нервно-мышечные и сердечно-сосудистые эффекты неосакситоксина у овец, анестезированных изофлураном». Регионарная анестезия и обезболивающее. 37 (2): 152–8. Дои:10.1097 / AAP.0b013e3182424566. PMID 22330260. S2CID 205432781.
- ^ Фунари Э., Тестай Э. (февраль 2008 г.). «Оценка риска для здоровья человека, связанного с воздействием цианотоксинов». Критические обзоры в токсикологии. 38 (2): 97–125. Дои:10.1080/10408440701749454. PMID 18259982. S2CID 19506251.
- ^ Гуай Дж (декабрь 2009 г.). «Неблагоприятные события, связанные с внутривенной регионарной анестезией (блок Биера): систематический обзор осложнений». Журнал клинической анестезии. 21 (8): 585–94. Дои:10.1016 / j.jclinane.2009.01.015. PMID 20122591.
- ^ Guo XT, Uehara A, Ravindran A, Bryant SH, Hall S, Moczydlowski E (декабрь 1987 г.). «Кинетическая основа нечувствительности к тетродотоксину и сакситоксину в натриевых каналах сердца собак и денервированных скелетных мышцах крыс». Биохимия. 26 (24): 7546–56. Дои:10.1021 / bi00398a003. PMID 2447944.
- ^ Sheets MF, Fozzard HA, Lipkind GM, Hanck DA (январь 2010 г.). «Молекулярные конформации натриевых каналов и сродство к антиаритмическим препаратам». Тенденции в сердечно-сосудистой медицине. 20 (1): 16–21. Дои:10.1016 / j.tcm.2010.03.002. ЧВК 2917343. PMID 20685573.
- ^ Templin JS, Wylie MC, Kim JD, Kurgansky KE, Gorski G, Kheir J, Zurakowski D, Corfas G, Berde C (октябрь 2015 г.). «Неосакситоксин при седалищном блоке у крыс: улучшение терапевтического индекса с использованием комбинаций с бупивакаином, с адреналином и без него». Анестезиология. 123 (4): 886–98. Дои:10.1097 / ALN.0000000000000832. PMID 26280473. S2CID 39363279.
- ^ Ip VH, Tsui BC (январь 2011 г.). «Новинка без токсичности: поиски более безопасного местного анестетика». Канадский журнал анестезии. 58 (1): 8–13. Дои:10.1007 / s12630-010-9409-у. PMID 21042902.
