Метаболизм фенилпропаноидов - Phenylpropanoids metabolism
В биосинтез из фенилпропаноиды задействует ряд ферментов.
От аминокислот до корицы
В растениях все фенилпропаноиды получают из аминокислот фенилаланин и тирозин.
Фенилаланин аммиак-лиаза (PAL, также известный как фенилаланин / тирозинаммиаклиаза) представляет собой фермент, который превращает L-фенилаланин и тирозин в транс-коричная кислота и п-куаровая кислота соответственно.
Транс-циннамат-4-монооксигеназа (циннамат-4-гидроксилаза) - это фермент, который превращает транс-циннамат в 4-гидроксициннамат (п-куаровая кислота). 4-кумарат-КоА лигаза это фермент, который превращает 4-кумарат (п-куаровая кислота) в 4-кумароил-КоА.[1]
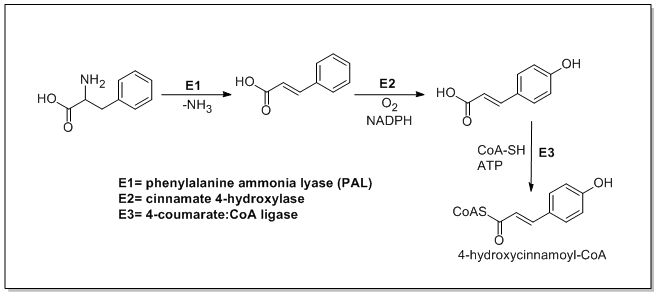
Ферменты, связанные с биосинтезом гидроксикоричных кислот
- Циннамиловый спиртдегидрогеназа (CAD), фермент, преобразующий циннамиловый спирт в коричный альдегид
- Синапинэстераза, фермент, который превращает синапоилхолин в синапате (синапиновая кислота ) и холин
- Транс-циннамат-2-монооксигеназа, фермент, преобразующий трансциннамат (коричная кислота ) в 2-гидроксициннамат
- Кофеат О-метилтрансфераза, фермент, который превращает кофейная кислота в феруловая кислота
- Caffeoyl-CoA O-метилтрансфераза, фермент, который превращает кофеил-КоА в ферулоил-КоА
- 5-O- (4-кумароил) -D-хинат 3'-монооксигеназа, фермент, который превращает транс-5-O- (4-кумароил) -D-хинат в транс-5-O-кофеил-D-хинат
- Синапоилглюкоза — холин-O-синапоилтрансфераза, фермент, который превращает 1-O-синапоил-бета-D-глюкоза в синапоилхолин (синапин )
- Синапоилглюкоза — малат-O-синапоилтрансфераза, фермент, который превращает 1-O-синапоил-бета-D-глюкоза в синапоил- (S) -малат
- Циннамоил-КоА редуктаза, фермент, который превращает циннамоил-КоА от коричный альдегид
Ферменты конъюгации
Эти ферменты сопрягать фенилпропаноидов к другим молекулам.
- 2-кумарат O-бета-глюкозилтрансфераза, фермент, который превращает транс-2-гидроксициннамат в транс-бета-D-глюкозил-2-гидроксициннамат
- Гидроксициннамат 4-бета-глюкозилтрансфераза, фермент, который превращает п-кумаровая кислота в 4-O-бета-D-глюкозил-4-гидроксициннамат
- Шикимат O-гидроксициннамоилтрансфераза, фермент, который превращает 4-кумароил-КоА в 4-кумароилшикимат
- Хинат-O-гидроксициннамоилтрансфераза, фермент, который превращает ферулоил-КоА в О-ферулоилхинат
- Синапат-1-глюкозилтрансфераза, фермент, который превращает синапат (синапиновая кислота ) в 1-синапоил-D-глюкоза
- Конифериловый спирт глюкозилтрансфераза, фермент, который превращает конифериловый спирт в хвойный
Глюкозидазы
- Кониферин бета-глюкозидаза, фермент, который превращает хвойный в кониферол
Биосинтез стильбеноидов
- Пиносилвинсинтаза, фермент, который превращает пиносильвин от циннамоил-КоА
- Тригидроксистильбенсинтаза, фермент, который превращает 4-кумароил-КоА к ресвератрол.
Альтернативный бактериальный кетосинтаза -направленный стильбеноиды путь биосинтеза существует в Photorhabdus бактериальные симбионты Гетерорабдит нематоды, продуцирующие 3,5-дигидрокси-4-изопропил-транс-стильбен в антибиотических целях.[2]
Кумарины биосинтез
- Скополетин глюкозилтрансфераза, фермент, который превращает скополетин в Скополин
Биосинтез халконов
4-кумароил-КоА может сочетаться с малонил-КоА чтобы получить истинную основу флавоноидов, группу соединений, называемых халконоиды, которые содержат два фенил кольца. Нарингенин-халкон-синтаза это фермент, катализирующий следующее превращение:
- 3-малонил-КоА + 4-кумароил-КоА → 4 CoA + нарингенин халкон + 3 СО2
Биосинтез флавоноидов
Сопряженное замыкание цикла халконов приводит к знакомой форме флавоноиды, трехкольцевая структура флавон.
Биоразложение
Разложение гидроксикоричной кислоты
- Кофеат-3,4-диоксигеназа это фермент, который использует 3,4-дигидрокси-транс-циннамат (кофейная кислота ) и кислород для производства 3- (2-карбоксиэтенил) -цис, цис-муконат.
использованная литература
- ^ Ververidis Filippos, F; Трантас Эммануил; Дуглас Карл; Фоллмер Гюнтер; Крецшмар Георг; Панопулос Николас (октябрь 2007 г.). «Биотехнология флавоноидов и других природных продуктов на основе фенилпропаноидов. Часть I: Химическое разнообразие, воздействие на биологию растений и здоровье человека». Биотехнологический журнал. 2 (10): 1214–34. Дои:10.1002 / biot.200700084. PMID 17935117.
- ^ Джойс С.А., Брахманн А.О., Глейзер I, Ланго Л., Швар Г., Кларк Д.Д., Боде Х.В. (2008). «Бактериальный биосинтез мультипотентного стильбена». Angew Chem Int Ed Engl. 47 (10): 1942–5. CiteSeerX 10.1.1.603.247. Дои:10.1002 / anie.200705148. PMID 18236486.
