Humulone - Humulone
 | |
 | |
| Имена | |
|---|---|
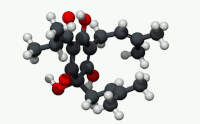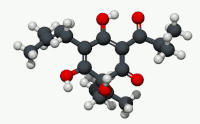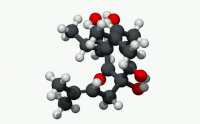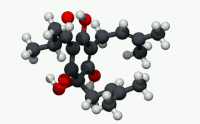
| Название ИЮПАК (6S) -3,5,6-Тригидрокси-2- (3-метилбутаноил) -4,6-бис (3-метилбут-2-ен-1-ил) циклогекса-2,4-диен-1-он[1] | |
| Другие имена α-лупуловая кислота; α-горькая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.043.371 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C21ЧАС30О5 | |
| Молярная масса | 362.466 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Humulone (α-лупуловая кислота), а винилогичный тип органической кислоты, представляет собой Горький -дегустация химическое соединение содержится в смоле зрелого хмель (Humulus lupulus ).[2] Гумулон является преобладающим членом класса соединений, известных как альфа-кислоты, которые в совокупности придают охмеленному пиву характерный горький вкус.
Химия
По структуре гумулон является флороглюцин производная с тремя изопреноид боковые цепи. Две боковые цепи являются пренильными группами, а одна - изовалерильной группой. Кислотность кольца энол фрагменты, которые привели к его обозначению как кислота, лежат в своих винилогичный взаимосвязь с карбонильными функциональными группами кольца и боковой цепи.[нужна цитата ]
Изогумулон
В процессе заваривания гумулон разлагается до цис- и транс-изогумулон.[1] Эти «альфа-кислоты» выдерживают процесс кипячения, хотя образуются многочисленные окисленные производные.[3] Изо-альфа-кислоты значительно более растворимы, чем гумулон, при уровнях pH, обычно присутствующих в процессе пивоварения.[4]
Лабораторный синтез
Хумулон может быть синтезирован ацилирование из бензол-1,2,3,5-тетрол с изовалерилхлоридом с получением 2,3,4,6-тетрагидроксиизовалерофенона. За этой стадией следует пренилирование 1-бром-3-метил-2-бутеном с получением гумулона.[5]
 Синтез гумулона из бензол-1,2,3,5-тетрола
Синтез гумулона из бензол-1,2,3,5-тетрола
Биосинтез
Как определено НЕАДЕКВАТ 2D ЯМР, биосинтез гумулона в Humulus lupulus начинается с изовалерил-КоА единица и 3 малонил-КоА установки, катализируемые флоровалерофенонсинтаза. Это превращение дает бензоид 3-метил-1- (2,4,6-тригидроксифенил) бутан-1-он. Диметилаллил пирофосфат затем получают по пути дезоксиксилулозы, где происходит пренилирование бензоида с образованием гумулона.[6]
- изовалерил-КоА + 3 малонил-КоА → 4 CoASH + 3 CO2 + 3-метил-1- (2,4,6-тригидроксифенил) бутан-1-он
- 3-метил-1- (2,4,6-тригидроксифенил) бутан-1-он + 2 DMAPP → C21ЧАС30О5
Исследование
Хумулон находится под фундаментальные исследования с in vitro исследования, чтобы определить, есть ли у него биологические свойства, например, ГАМКА рецептор Мероприятия[7][8] или же антибактериальный последствия.[9]
Рекомендации
- ^ а б Городской, Янв; Дальберг, Клинтон; Кэрролл, Брайан; Каминский, Вернер (2013). «Абсолютная конфигурация горьких соединений пива». Энгью. Chem. Int. Эд. 52 (5): 1553–1555. Дои:10.1002 / anie.201208450. ЧВК 3563212. PMID 23239507.
- ^ De Keukeleire, J; Ooms, G; Хейерик, А; Ролдан-Руис, I; Van Bockstaele, E; Де Кёкелейре, Д. (2003). «Образование и накопление альфа-кислот, бета-кислот, десметилксантогумола и ксантогумола во время цветения хмеля (Humulus lupulus L.)». Журнал сельскохозяйственной и пищевой химии. 51 (15): 4436–41. Дои:10.1021 / jf034263z. PMID 12848522.
- ^ Blanco, C.A .; Рохас, А; Caballero, P.A .; Ронда, Ф; Гомес, М; Кабальеро, И., «Лучший контроль свойств пива путем прогнозирования кислотности изо-α-кислот хмеля», Тенденции в пищевой науке и технологиях, том 17, выпуск 7, июль 2006 г., страницы 373-377, ISSN 0924-2244, Дои:10.1016 / j.tifs.2005.11.012.
- ^ Эсслингер, Х. М. и Нарцисс, Л. 2003. «Пиво». в Энциклопедии промышленной химии Ульмана. Wiley-VCH Verlag GmbH & Co. KGaA, 2009 г. Дои:10.1002 / 14356007.a03_421
- ^ Обара; и другие. (1989). «Синтетический путь к (±) -гумулону». Бык. Chem. Soc. JPN. 62 (9): 3034–3035. Дои:10.1246 / bcsj.62.3034.
- ^ М. Гёзе; К. Каммхубер; А. Бахер; М. Х. Зенк; В. Эйзенрайх (1999). «Биосинтез горьких кислот в хмеле. A (13) C-ЯМР и (2) H-ЯМР исследование строительных блоков гумулона». Журнал FEBS. 263 (2): 447–454. Дои:10.1046 / j.1432-1327.1999.00518.x. PMID 10406953.
- ^ Benkherouf, Ali Y .; Эерола, Ким; Soini, Sanna L .; Ууси-Оукари, Микко (2020). «Модуляция гумулоном рецепторов GABAA и его роль в сонной активности хмеля». Границы неврологии. 14. Дои:10.3389 / fnins.2020.594708. ISSN 1662-453X.
- ^ Benkherouf, Ali Y .; Логрен, Нора; Сомборак, Тамара; Кортесниеми, Маария; Soini, Sanna L .; Ян, Баору; Salo-Ahen, Outi M.H .; Лааксонен, Оскар; Ууси-Оукари, Микко (01.04.2020). «Модулирующие эффекты соединений хмеля и двойной механизм действия 6-пренилнарингенина на рецепторы ГАМК». Европейский журнал фармакологии. 873: 172962. Дои:10.1016 / j.ejphar.2020.172962. PMID 32001220.
- ^ Ямагути, N; Сато-Ямагути, К. Оно, М (2009). «Оценка in vitro антибактериальной, антиколлагеназной и антиоксидантной активности компонентов хмеля (Humulus lupulus) от вульгарных угрей ». Фитомедицина. 16 (4): 369–76. Дои:10.1016 / j.phymed.2008.12.021. PMID 19201179.


