Ячейка Купфера - Kupffer cell
| Ячейка Купфера | |
|---|---|
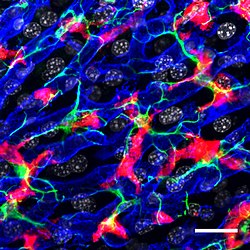 Конфокальная микроскопия изображение, показывающее устойчивое положение и взаимодействие между Клетки Купфера (Красный), звездчатые клетки печени (зеленый) и синусоидальные эндотелиальные клетки печени (синий). Ядра клеток выделены серым цветом.[1] | |
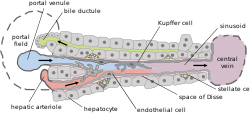 Основное строение печени | |
| Подробности | |
| Место расположения | Печень |
| Функция | Макрофаги |
| Идентификаторы | |
| латинский | звездчатый макрофагоцит |
| MeSH | D007728 |
| TH | H3.04.05.0.00016 |
| FMA | 14656 |
| Анатомические термины микроанатомии | |
Клетки Купфера, также известный как звездчатые макрофаги и Клетки Купфера-Бровича, являются специализированными клетками, локализованными в печень в просвете синусоидов печени и прикрепляются к своим эндотелиальным клеткам, которые составляют стенки кровеносных сосудов. Клетки Купфера содержат наибольшее количество резидентных тканей макрофаги в организме. Кишечные бактерии, бактериальные эндотоксины и остатки микробов, транспортируемые в печень из желудочно-кишечный тракт через воротная вена сначала вступит в контакт с клетками Купфера, первыми иммунными клетками печени. Именно из-за этого любое изменение функций клеток Купфера может быть связано с различными заболеваниями печени, такими как алкогольная болезнь печени, вирусный гепатит, внутрипеченочный холестаз, стеатогепатит, активация или отторжение печени во время трансплантации печени и фиброз печени.[2][3] Они составляют часть система мононуклеарных фагоцитов.
Структура
Клетки Купфера амебовидной формы прикреплены к синусоидальным эндотелиальным клеткам. Поверхность клеток Купфера содержит микроворсинки, псевдоподии и ламеллиподии, которые выступают во всех направлениях. Микроворсинки и псевдоподии играют роль в эндоцитозе частиц. В их цитоплазме можно найти рибосомы, аппарат Гольджи, центриоли, микротрубочки и микрофиламенты. Ядро имеет выемку, яйцевидную форму и может быть дольчатым. Они также содержат грубую эндоплазматическую сеть, ядерную оболочку и кольцевидные ламеллы, которые все содержат пероксидазную активность. Как в центрилобулярной, так и в перипортальной областях печени находятся клетки Купфера, но их функции и структуры меняются в зависимости от их расположения. Перипортальные клетки Купфера имеют тенденцию быть больше и обладают большей лизосомальной ферментативной и фагоцитарной активностью, тогда как центрилобулярные клетки Купфера создают больше супероксидных радикалов. Рецептор скавенджера SR-AI / II находится внутри клеток Купфера. Этот рецептор участвует в распознавании и связывании домена липида А липополисахарида (ЛПС) и липотейхоевой кислоты. Липополисахарид (ЛПС) представляет собой бактериальный эндотоксин, который содержится в грамотрицательных бактериях клеточной стенки, тогда как липотейхоевая кислота присутствует в грамположительных бактериях.[4]
Разработка
Их развитие начинается в желточный мешок где они дифференцируются на макрофаги плода. Попадая в кровоток, они мигрируют в печень плода где они остаются. Там они завершают свою дифференцировку в клетки Купфера.[5]
В основном есть два типа печеночных макрофаги: Клетки Купфера, которые находятся в печень и происходит из красного желточного мешка Костный мозг клетки-предшественники, а также макрофаги, происходящие из моноцитов, полученные из гемопоэтические стволовые клетки из костного мозга и по кровообращению транспортируется в печень. Макрофаги, происходящие из моноцитов, представляют собой иммуногенные макрофаги, которые дифференцируются под влиянием микроокружения. Клетки Купфера самоподдерживаются. Они локально пролиферируют, обычно представляют собой восприимчивую популяцию фагоцитарных клеток. Моноциты которые находятся в периферическом кровообращении и происходят из клеток-предшественников в костном мозге, считаются незрелыми предшественниками тканевых макрофагов у взрослых животных. В печень могут попасть моноциты периферической крови, затем моноциты созревают и приобретают фенотип, характерный для тканевых макрофагов. Различные факторы роста регулируют дифференцировку макрофагов. Однако роль стимуляции колонии макрофагов, по-видимому, является наиболее важной в развитии зрелых клеток Купфера.[6][3]
Функция
Средняя продолжительность жизни ячейки Купфера составляет около 3,8 дня. Основная функция клетки Купфера - удалять инородный мусор и частицы, которые попадают из портальной системы при прохождении через печень. Ячейки Купфера могут поглощать крупные частицы за счет фагоцитоз и более мелкие частицы через пиноцитоз.[4] Клетки Купфера являются неотъемлемой частью врожденных реакций иммунной системы. Они также важны для защиты хозяина и играют роль в метаболизме многих различных соединений, включая липиды, белковые комплексы и мелкие частицы. Они также полезны для удаления апоптотических клеток из кровотока.[2][3] Количество купферовских клеток в печени постоянно. Они регулируются апоптозом, а также фагоцитируются соседними клетками Купфера. Клетки Купфера обладают пролиферативной способностью, это позволяет им самовосстанавливаться, что полностью контрастирует с макрофагами, происходящими из моноцитов, которые не имеют пролиферативного потенциала. Было показано, что клетки Купфера неоднородны по своим функциям, в зависимости от их расположения в организме. Например, в зоне 1 долек печени они гораздо более активны, чем их аналоги в зоне 3. Повышенная активность может быть связана с тем, что в зоне 1 гораздо больше воздействия опасных веществ, чем в зоне 3. Клетки Купфера могут производить воспалительные цитокины, TNF-альфа, кислородные радикалы и протеазы, а также выполняющие фагоцитоз. Считается, что создание этих медиаторов приводит к развитию повреждения печени.[4]
Помимо очистка любые бактерии, красные кровяные тельца также разрушаются фагоцитарным действием, где гемоглобин молекула расщепляется. Цепи глобина используются повторно, а железосодержащая часть гем, далее распадается на железо, которое используется повторно, и билирубин, который сопряжен с глюкуроновая кислота в гепатоциты и спрятан в желчь.
Helmy et al. идентифицировали рецептор, присутствующий в клетках Купфера, рецептор комплемента семейства иммуноглобулинов (CRIg). Мыши без CRIg не могли очистить система комплемента покрытые оболочкой патогены. CRIg сохраняется у мышей и людей и является критическим компонентом врожденной иммунной системы.[7]
Клиническое значение
Активация клеток Купфера ответственна за раннее повреждение печени, вызванное этанолом, которое часто встречается у хронических алкоголиков. Хронический алкоголизм и повреждение печени справляются с системой двойного удара. Второй удар характеризуется активацией Toll-подобного рецептора 4 (TLR4 ) и CD14, рецепторы на клетке Купфера, которые усваивают эндотоксин (липополисахарид или LPS). Это активирует транскрипцию провоспалительных цитокины (Фактор некроза опухоли альфа или TNFα) и производство супероксиды (прооксидант). TNFα затем войдет в звездчатая клетка в печени, что приводит к коллаген синтез и фиброз. В конечном итоге фиброз приводит к циррозу или потере функции печени.[8]
В ответ на сепсис клетки Купфера играют роль в патогенезе поврежденной печени. Макрофаги в печени активируют и высвобождают как IL-1, так и TNF-альфа. В свою очередь, это активирует лейкоциты и синусоидальные эндотелиальные клетки для экспрессии ICAM-1. Это приводит к повреждению ткани эндотелия из-за протеаз, кислородных радикалов, простаноидов и других веществ из лейкоцитов. Алкогольная болезнь печени, или, как его известно, ALD, это термин, который включает широкий спектр повреждений печени от стеатоза до стеатогепатита, фиброз и цирроз печени. Фактические данные показали, что клетки Купфера играют важную роль в патогенезе как хронической, так и острой ALD. Воздействие алкоголя может привести к увеличению печеночной транслокации эндотоксина / липополисахарида, поступающего из кишечника, что является сильной поляризацией M1 клеток Купфера. Активированные клетки Купфера вырабатывают большое количество активных форм кислорода, провоспалительных цитокинов и хемокинов, что приводит к повреждению печени. Клетки Купфера - невероятно пластичные клетки, которые обладают способностью поляризовать определенные состояния активации и могут выполнять разные функции в разных микросредах. M1 (классическая активация) и M2 (альтернативная активация) - два обозначения двух крайних значений поляризации макрофагов. Поляризованный M1 Купфер продуцирует большое количество провоспалительных цитокинов, таких как TNF-альфа. С другой стороны, M2-поляризованные клетки Купфера демонстрируют большое количество противовоспалительных медиаторов, например IL-10.[9][4]
История
Впервые клетки наблюдали Карл Вильгельм фон Купфер в 1876 г.[10] Ученый назвал их «Sternzellen» (звездные клетки или звездчатая клетка печени ), но ошибочно полагал, что они являются неотъемлемой частью эндотелий кровеносных сосудов печени и что они исходили от нее. В 1898 году, после нескольких лет исследований, Тадеуш Брович правильно идентифицировал их как макрофаги.[11][12]
Рекомендации
- ^ Боннардель Дж., Т'Джонк В., Гобломм Д., Брауэйс Р., Скотт К.Л., Мартенс Л. и др. (Октябрь 2019 г.). «Звездчатые клетки, гепатоциты и эндотелиальные клетки отпечатывают идентичность клеток Купфера на моноцитах, колонизирующих нишу макрофагов печени». Иммунитет. 51 (4): 638–654.e9. Дои:10.1016 / j.immuni.2019.08.017. ЧВК 6876284. PMID 31561945.
- ^ а б Нгуен-Лефевр, Ань Тху; Хоружско, Анатолий (2015). «Метаболизм и функция клеток Купфера». Журнал энзимологии и метаболизма. 1 (1). ЧВК 4771376. PMID 26937490.
- ^ а б c Диксон, Лаура Дж .; Барнс, Марк; Тан, Хуэй; Pritchard, Michele T .; Надь, Лаура Э. (апрель 2013 г.). «Клетки Купфера в печени». Комплексная физиология. 3 (2): 785–797. Дои:10.1002 / cphy.c120026. ISSN 2040-4603. ЧВК 4748178. PMID 23720329.
- ^ а б c d Басит, Хаджира; Tan, Michael L .; Вебстер, Дэниел Р. (2020), «Гистология, ячейка Купфера», StatPearls, Остров сокровищ (Флорида): StatPearls Publishing, PMID 29630278, получено 2020-08-25
- ^ Наито М., Хасэгава Г., Такахаши К. (ноябрь 1997 г.). «Развитие, дифференциация и созревание клеток Купфера». Микроскопические исследования и техника. 39 (4): 350–64. Дои:10.1002 / (SICI) 1097-0029 (19971115) 39: 4 <350 :: AID-JEMT5> 3.0.CO; 2-L. PMID 9407545.
- ^ "Клетки Купфера при безалкогольной жировой болезни печени: друг или враг?". www.ijbs.com. Получено 2020-08-31.
- ^ Хельми К.Ю., Качке К.Дж., Горгани Н.Н., Клявин Н.М., Эллиотт Дж.М., Диль Л. и др. (Март 2006 г.). «CRIg: рецептор комплемента макрофагов, необходимый для фагоцитоза циркулирующих патогенов». Клетка. 124 (5): 915–27. Дои:10.1016 / j.cell.2005.12.039. PMID 16530040.
- ^ Уиллер, доктор медицины (2003). «Эндотоксин и активация клеток Купфера при алкогольной болезни печени». Исследования алкоголя и здоровье: Журнал Национального института злоупотребления алкоголем и алкоголизма. 27 (4): 300–6. ЧВК 6668869. PMID 15540801.
- ^ Цзэн, Дао; Чжан, Цуй-Ли; Сяо, Мо; Ян, Руи; Се, Кэ-Цинь (2016). «Критические роли клеток Купфера в патогенезе алкогольной болезни печени: от фундаментальной науки до клинических испытаний». Границы иммунологии. 7. Дои:10.3389 / fimmu.2016.00538. ISSN 1664-3224.
- ^ Хаубрих WS (июль 2004 г.). «Купфер ячеек Купфера». Гастроэнтерология. 127 (1): 16. Дои:10.1053 / j.gastro.2004.05.041. PMID 15236167.
- ^ Szymańska R, Schmidt-Pospuła M (1979). «[Исследования ретикулоэндотелиальных клеток печени Тадеушем Бровичем и Карлом Купфером. Исторический очерк]». Archiwum Historii Medycyny. 42 (3): 331–6. PMID 386989.
- ^ Stachura J, Gałazka K (декабрь 2003 г.). «История и современное состояние польской гастроэнтерологической патологии». Журнал физиологии и фармакологии. 54 Дополнение 3: 183–92. PMID 15075472.
внешняя ссылка
- Анатомическое фото: пищеварительная система / млекопитающее / печень5 / печень4 - Сравнительная органология в Калифорнийском университете в Дэвисе - «Млекопитающие, печень (EM, низкий)»
- Гистологическое изображение: 15508 лоа - Система обучения гистологии в Бостонском университете
- Kupffer Cell Foundation - Миссия Фонда клеток Купфера состоит в том, чтобы стимулировать и поддерживать исследования и образование для улучшения знаний о роли клетки Купфера и синусоидального барьера в здоровой и больной печени.
