Микроглия - Microglia
| Микроглия | |
|---|---|
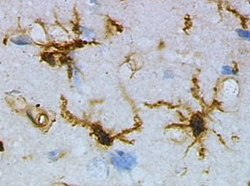 Микроглия в состоянии покоя из коры головного мозга крысы перед черепно-мозговой травмой (окрашивание лектина HRP ) | |
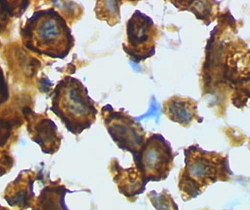 Микроглия / макрофаг - активированная форма коры головного мозга крысы после черепно-мозговой травмы (окрашивание лектина с помощью HRP) | |
| Подробности | |
| Предшественник | Примитивные макрофаги, полученные из желточного мешка |
| Система | Центральная нервная система |
| Идентификаторы | |
| MeSH | D017628 |
| TH | H2.00.06.2.00004, H2.00.06.2.01025 |
| FMA | 54539 |
| Анатомические термины микроанатомии | |
Микроглия являются разновидностью нейроглия (глиальная клетка), расположенная по всей мозг и спинной мозг.[1] Микроглия составляет 10–15% всех клеток головного мозга.[2] Как резидент макрофаг клетки, они действуют как первая и основная форма активной иммунной защиты в Центральная нервная система (ЦНС).[3] Микроглия (и другие нейроглии, включая астроциты ) распределены в больших неперекрывающихся областях по всей ЦНС.[4][5] Микроглия - ключевые клетки в общем функционировании мозга - они постоянно очищают ЦНС от бляшки, повреждены или ненужны нейроны и синапсы, и инфекционные агенты.[6] Поскольку эти процессы должны быть эффективными, чтобы предотвратить потенциально смертельное повреждение, микроглия чрезвычайно чувствительна даже к небольшим патологическим изменениям в ЦНС.[7] Эта чувствительность частично достигается наличием уникальных калиевые каналы которые реагируют даже на небольшие изменения в внеклеточный калий.[6] Последние данные показывают, что микроглия также играет ключевую роль в поддержании нормальных функций мозга в здоровых условиях.[8] Микроглия также постоянно контролирует нейрональные функции посредством прямых соматических контактов и при необходимости оказывает нейропротекторное действие.[9]
Головной и спинной мозг, составляющие ЦНС, обычно не подвергаются прямому доступу патогенным факторам кровообращения в организме из-за ряда эндотелиальные клетки известный как гематоэнцефалический барьер, или BBB. BBB предотвращает попадание большинства инфекций в уязвимую нервную ткань. В случае, когда инфекционные агенты попадают непосредственно в мозг или пересекают гематоэнцефалический барьер, клетки микроглии должны быстро реагировать на уменьшение воспаление и уничтожить инфекционные агенты до того, как они повредят чувствительную нервную ткань. Из-за отсутствия антитела от остального тела (некоторые антитела достаточно малы, чтобы пересечь гематоэнцефалический барьер), микроглия должна распознавать инородные тела, проглатывать их и действовать как антигенпрезентирующие клетки активация Т-клетки.
Формы
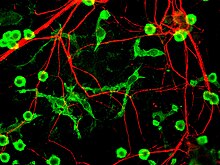
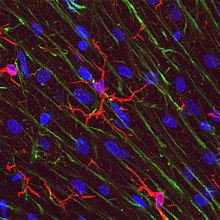
Клетки микроглии чрезвычайно пластик, и претерпевают различные структурные изменения в зависимости от местоположения и потребностей системы. Такой уровень пластичности необходим для выполнения огромного количества функций, которые выполняет микроглия. Способность к трансформации отличает микроглию от макрофаги, которые необходимо заменять на регулярной основе, и дает им возможность защищать ЦНС в очень короткие сроки, не вызывая иммунологических нарушений.[6] Микроглия принимает определенную форму, или фенотип в ответ на местные условия и обнаруженные химические сигналы.[10]
Чувствительная генетика
Сенсом микроглии - это относительно новая биологическая концепция, которая, по-видимому, играет большую роль в развитие нервной системы и нейродегенерация. Сенсом относится к уникальной группе белков. стенограммы используется для зондирования лиганды и микробы. Другими словами, сенсома представляет собой гены, необходимые для белков, используемых для восприятия молекул в организме. Сенсом можно анализировать с помощью различных методов, включая КПЦР, РНК-последовательность, микроматричный анализ и прямое секвенирование РНК. Гены, включенные в сенсомный код рецепторов и трансмембранные белки на плазматическая мембрана которые более высоко экспрессируются в микроглии по сравнению с нейронами. Он не включает секретируемые белки или трансмембранные белки, специфичные для мембраносвязанных органелл, таких как ядро, митохондрии, и эндоплазматический ретикулум.[11] Множество идентифицированных сенсомных генов кодируют рецепторы распознавания образов, однако имеется большое разнообразие включенных генов. Микроглии имеют схожий сенсом с другими макрофагами, однако они содержат 22 уникальных гена, 16 из которых используются для взаимодействия с эндогенными лигандами. Эти различия создают уникальный микроглиальный биомаркер, который включает более 40 генов, в том числе: P2ry12 и HEXB. DAP12, по-видимому, играет важную роль во взаимодействии с сенсомными белками, действуя как адаптер передачи сигналов и регуляторный белок.[11]
Регуляция генов в сенсоме должна изменяться, чтобы реагировать на потенциальный вред. Микроглия может взять на себя роль нейрозащита или же нейротоксичность чтобы противостоять этим опасностям.[12] По этим причинам предполагается, что сенсома может играть роль в нейродегенерации. Сенсомные гены, которые активируются с возрастом, в основном участвуют в распознавании инфекционных микробных лигандов, в то время как гены с пониженной регуляцией в основном участвуют в распознавании эндогенных лигандов.[11] Этот анализ предполагает специфическую глиальную регуляцию, благоприятствующую нейропротекции при естественной нейродегенерации. Это контрастирует со сдвигом в сторону нейротоксичности, наблюдаемым при нейродегенеративных заболеваниях.
Сенсома также может играть роль в развитии нервной системы. Инфекция мозга в раннем возрасте приводит к образованию микроглии, которая становится сверхчувствительной к более поздним иммунным стимулам. При контакте с инфекцией происходит активация сенсомных генов, участвующих в нейровоспаление и подавление генов, участвующих в нейропластичности.[13] Однако способность сенсомы влиять на развитие нервной системы может бороться с болезнью. Удаление CX3CL1, высокоэкспрессируемый сенсомный ген, в моделях грызунов Синдром Ретта привел к улучшению здоровья и увеличению продолжительности жизни.[14] Подавление Cx3cr1 у людей без синдрома Ретта ассоциируется с симптомами, похожими на шизофрения.[15] Это говорит о том, что сенсома не только играет роль в различных нарушениях развития, но также требует строгой регуляции для поддержания безболезненного состояния.
Разветвленный
Эта форма микроглиальных клеток обычно обнаруживается в определенных местах по всему головному и спинному мозгу в отсутствие инородного материала или умирающих клеток. Эта «покоящаяся» форма микроглии состоит из длинных ветвящихся отростков и небольшого клеточного тела. В отличие от амебоидных форм микроглии, тело клетки разветвленной формы остается на месте, в то время как ее ветви постоянно перемещаются и осматривают окружающую территорию. Ветви очень чувствительны к небольшим изменениям физиологического состояния и требуют очень специфических условий культивирования для наблюдения. in vitro.[10]
В отличие от активирован или же амебовидный микроглия, разветвленная микроглия не фагоцитируют клетки и секретируют меньше иммуномолекул (включая MHC класс I /II белки). Микроглия в этом состоянии может искать и идентифицировать иммунные угрозы, сохраняя при этом гомеостаз в ЦНС.[16][17][18] Хотя это считается состоянием покоя, микроглия в этой форме по-прежнему чрезвычайно активна в химическом исследовании окружающей среды. Разветвленная микроглия может быть преобразована в активированную форму в любой момент в ответ на травму или угрозу.[10]
Реактивный (активирован)
Хотя исторически часто используемый термин «активированная» микроглия следует заменить на «реактивную» микроглию.[19] В самом деле, явно покоящаяся микроглия не лишена активных функций, и термин «активация» вводит в заблуждение, поскольку он имеет тенденцию указывать на поляризацию реактивности клеток «все или ничего». Маркер Iba1, который активируется в реактивной микроглии, часто используется для визуализации этих клеток.[20]
Нефагоцитарный
Это состояние на самом деле является частью дифференцированной реакции, когда микроглия переходит из разветвленной формы в полностью активную фагоцитарную форму. Микроглия может быть активирована множеством факторов, включая провоспалительные цитокины, клетка некроз факторы, липополисахариды и изменения внеклеточного калия (что указывает на разрыв клеток). После активации клетки претерпевают несколько ключевых морфологических изменений, включая утолщение и ретракцию ветвей, поглощение белков MHC класса I / II, экспрессию иммуномолекул, секрецию цитотоксический факторы, секреция молекул рекрутирования и секреция провоспалительных сигнальных молекул (что приводит к провоспалительному сигнальному каскаду). Активированная нефагоцитарная микроглия обычно выглядит как «кустистая», «палочка» или маленькие амебоиды, в зависимости от того, насколько далеко они находятся в континууме разветвленной или полной фагоцитарной трансформации. Кроме того, микроглия также быстро разрастается, чтобы увеличить их количество. С чисто морфологической точки зрения изменение формы микроглии вдоль континуума связано с изменяющейся морфологической сложностью и может быть количественно оценено с использованием методов фрактального анализа, которые оказались чувствительными даже к едва заметным, визуально не обнаруживаемым изменениям, связанным с различной морфологией в различных патологических состояниях .[6][16][17][21]
Фагоцитарный
Активированная фагоцитарная микроглия - это форма микроглии с максимальной иммунной реакцией. Эти клетки обычно принимают большую амебовидную форму, хотя наблюдаются некоторые различия. Помимо наличия антигена, цитотоксический и опосредованной воспалением передачи сигналов активированной нефагоцитарной микроглии, они также способны фагоцитировать чужеродные материалы и отображать полученные иммуномолекулы для Т-клетка активация. Фагоцитарная микроглия перемещается к месту повреждения, поглощает материал, вызывающий нарушение, и секретирует провоспалительные факторы, чтобы способствовать размножению большего количества клеток и делать то же самое. Активированная фагоцитарная микроглия также взаимодействует с астроциты и нервные клетки, чтобы как можно быстрее бороться с любой инфекцией или воспалением с минимальным повреждением здоровых клеток мозга.[6][16]
Амебовидный
Эта форма позволяет микроглии свободно перемещаться по нервной ткани, что позволяет ей выполнять свою роль клетки-мусорщика. Амебовидная микроглия способна фагоцитировать дебрис, но не выполняет те же антигенпредставляющие и воспалительные функции, как активированная микроглия. Амебоидная микроглия особенно распространена во время развития и перестройки мозга, когда имеется большое количество внеклеточного мусора и апоптотические клетки удалять. Эта форма микроглиальных клеток встречается в основном в перинатальном периоде. белое вещество области в мозолистое тело известный как «Фонтаны Микроглии».[6][17][22]
Гиттер-клетки
Гиттер-клетки - это конечный результат микроглиальных клеток. фагоцитоз инфекционного материала или клеточного мусора. В конце концов, после поглощения определенного количества материала фагоцитарная микроглиальная клетка становится неспособной фагоцитировать какие-либо другие материалы. Образовавшаяся клеточная масса известна как гранулированное тельце, названное так из-за своего «зернистого» вида. Глядя на окрашенную ткань, чтобы выявить клетки, патологи могут визуализировать зажившие участки после инфицирования.[23]
Периваскулярный
В отличие от других типов микроглии, упомянутых выше, «периваскулярная» микроглия относится к расположению клетки, а не к ее форме / функции. Периваскулярная микроглия в основном находится в стенках базальная пластинка. Они выполняют нормальные функции микроглии, но, в отличие от нормальной микроглии, заменяются Костный мозг -производные клетки-предшественники на регулярной основе и экспрессируют MHC класс II антигены независимо от их окружения. Периваскулярная микроглия также сильно реагирует на антигены дифференцировки макрофагов.[6] Было показано, что эти микроглии необходимы для восстановления сосудистый стены, как показали эксперименты Риттера и наблюдения ишемический ретинопатия. Периваскулярная микроглия способствует эндотелиальная клетка пролиферация, позволяющая формировать новые сосуды и восстанавливать поврежденные сосуды. Во время этих процессов миелоидный рекрутирование и дифференцировка в клетки микроглии значительно ускоряется для выполнения этих задач.[24]
Юкставаскулярный
Подобно периваскулярной микроглии, юкставаскулярную микроглию можно отличить в основном по их расположению. Юкставаскулярная микроглия находится в прямом контакте с базальная пластинка стенки кровеносных сосудов, но не находятся внутри стенок. Как и периваскулярные клетки, они экспрессируют MHC класс II белки даже при низком уровне воспалительного цитокин Мероприятия. В отличие от периваскулярных клеток, но подобно резидентной микроглии, юкставаскулярная микроглия не демонстрирует быстрого обновления или замены миелоидные клетки-предшественники на регулярной основе.[6]
Функции

Клетки микроглии выполняют множество различных задач в ЦНС, в основном связанных как с иммунным ответом, так и с поддержанием гомеостаза. Ниже приведены некоторые из основных известных функций, выполняемых этими ячейками.[нужна цитата ]
Уборка мусора
Помимо того, что каждая микроглиальная клетка очень чувствительна к небольшим изменениям в окружающей среде, она также регулярно физически изучает свой домен. Это действие проводится в амебоидном состоянии и состоянии покоя. Если при движении через установленную область микроглиальная клетка обнаруживает какой-либо инородный материал, поврежденные клетки, апоптотический клетки нейрофибриллярные сплетения, Фрагменты ДНК или бляшки он активирует и фагоцитирует материал или клетку. Таким образом, микроглиальные клетки также действуют как «домработницы», очищая случайный клеточный мусор.[16] Во время развития мозга клетки микроглии играют большую роль, регулируя количество нервных клеток-предшественников и удаляя апоптозные нейроны. Есть также свидетельства того, что микроглия может улучшить синаптическую схему, поглощая и уничтожая синапсы.[25] После развития большинство мертвых или апоптотических клеток обнаруживается в кора головного мозга и подкорковые белое вещество. Это может объяснить, почему большинство амебоидных микроглиальных клеток находится в «фонтанах микроглии» в коре головного мозга.[22]
Фагоцитоз
Основная роль микроглии, фагоцитоз, включает в себя поглощение различных материалов. Поглощенные материалы обычно состоят из клеточного мусора, липиды, и апоптотический клетки в невоспаленном состоянии и вторгаются вирус, бактерии, или другие инородные материалы в воспаленном состоянии. Как только микроглиальная клетка «заполнится», она останавливается. фагоцитарный активности и превращается в относительно нереактивную gitter cell.[нужна цитата ]
Внеклеточная передача сигналов
Большая часть роли микроглиальных клеток в головном мозге поддерживает гомеостаз в незараженных регионах и продвижение воспаление в инфицированной или поврежденной ткани. Микроглия достигает этого с помощью чрезвычайно сложной серии внеклеточных сигнальных молекул, которые позволяют им общаться с другими микроглиями, астроциты, нервы, Т-клетки, и миелоидные клетки-предшественники. Как упоминалось выше, цитокин IFN-γ можно использовать для активации клеток микроглии. Кроме того, после активации IFN-γ микроглия также высвобождает больше IFN-γ во внеклеточное пространство. Это активирует больше микроглии и запускает индуцированный цитокинами каскад активации, быстро активирующий всю близлежащую микроглию. ФНО-α, продуцируемый микроглией, заставляет нервную ткань подвергаться апоптоз и усиливает воспаление. Ил-8 продвигает В-клетка рост и дифференциация, что позволяет микроглии бороться с инфекцией. Другой цитокин, Ил-1, подавляет цитокины Ил-10 и TGF-β, которые подавляют презентация антигена и провоспалительная сигнализация. Дополнительный дендритные клетки и Т-клетки рекрутируются к месту повреждения через микроглиальную продукцию хемотаксический молекулы как MDC, Ил-8 и MIP-3β. Наконец, PGE2 и другие простаноиды не допустить хроническое воспаление путем ингибирования провоспалительного ответа микроглии и подавления Чт1 (Т-хелперная клетка) ответ.[16]
Презентация антигена
Как упоминалось выше, резидентная неактивированная микроглия действует как плохой антигенпрезентирующие клетки из-за отсутствия белков MHC класса I / II. После активации они быстро поглощают белки MHC класса I / II и быстро становятся эффективными презентаторами антигенов. В некоторых случаях микроглия также может быть активирована IFN-γ, чтобы представить антигены, но не действуют так эффективно, как если бы они подверглись поглощению белков MHC класса I / II. В течение воспаление, Т-клетки через гематоэнцефалический барьер благодаря специальным поверхностным маркерам, а затем напрямую связываются с микроглией, чтобы получить антигены. После того, как им были представлены антигены, Т-клетки продолжают выполнять множество функций, включая провоспалительный набор, формирование иммуно-воспоминаний, секрецию цитотоксический материалы и прямые атаки на плазматические мембраны чужеродных клеток.[6][16]
Цитотоксичность
В дополнение к способности уничтожать инфекционные организмы через контакт клетки с клеткой через фагоцитоз, микроглия также может выделять различные цитотоксический вещества. Микроглия в культуре выделяет большое количество перекиси водорода и оксида азота в процессе, известном как «респираторный взрыв '. Оба этих химиката могут напрямую повреждать клетки и приводить к гибели нервных клеток. Протеазы секретируется микроглией катаболизировать специфические белки, вызывающие прямое повреждение клеток, в то время как цитокины подобно Ил-1 продвигать демиелинизация аксонов нейронов. Наконец, микроглия может поражать нейроны посредством процессов, опосредованных рецептором NMDA, путем секреции глутамат, аспартат и хинолиновая кислота. Цитотоксическая секреция направлена на уничтожение инфицированных нейронов, вирусов и бактерий, но также может вызывать большое количество сопутствующих нервных повреждений. В результате хроническая воспалительная реакция может привести к крупномасштабному повреждению нервной системы, поскольку микроглия разрушает мозг, пытаясь уничтожить вторгающуюся инфекцию.[6] Эдаравоне, поглотитель радикалов, предотвращает окислительную нейротоксичность, вызываемую активированной микроглией.[26]
Синаптическое удаление
Это явление, впервые обнаруженное Блинцингером и Крейцбергом в 1968 году при поражении позвоночника, состоит в том, что поствоспалительная микроглия удаляет ветви нервов рядом с поврежденной тканью. Это способствует возобновлению роста и восстановлению поврежденных участков. нейронная схема.[6]
Продвижение ремонта
Поствоспалительная микроглия проходит несколько этапов, способствующих возобновлению роста нервной ткани. К ним относятся синаптическое удаление, секреция противовоспалительных цитокины, набор нейроны и астроциты к поврежденному участку и образование gitter клетки. Без микроглиальных клеток отрастание и повторное картирование было бы значительно медленнее в резидентных областях ЦНС и почти невозможно во многих сосудистых системах, окружающих мозг и глаза.[6][24] Недавние исследования подтвердили, что процессы микроглии постоянно контролируют нейронные функции через специализированные соматические соединения и определяют «благополучие» нервных клеток. Посредством этого межклеточного пути коммуникации микроглия способна оказывать сильные нейропротекторные эффекты, внося значительный вклад в восстановление после травмы головного мозга.[27]
Разработка
Долгое время считалось, что клетки микроглии дифференцируются в Костный мозг из гемопоэтические стволовые клетки, то прародители всех клеток крови. Однако недавние исследования показывают, что микроглия возникает в желточном мешке в течение чрезвычайно ограниченного эмбрионального периода и заселяет мозг. мезенхима. Кроме того, они непрерывно обновляются и сохраняются на протяжении всей жизни без пополнения периферическими моноцитарными предшественниками.[28]
Моноциты также могут дифференцироваться на миелоидные дендритные клетки и макрофаги в периферических системах. Как и макрофаги в остальном теле, микроглия использует фагоцитарный и цитотоксический механизмы для уничтожения посторонних материалов. Микроглия и макрофаги вносят свой вклад в иммунный ответ, действуя как антигенпрезентирующие клетки, а также способствует развитию воспаления и гомеостатических механизмов в организме, выделяя цитокины и другие сигнальные молекулы.[29]
В подавленной форме микроглии не хватает MHC класс I /MHC класс II белки, IFN-γ цитокины, CD45 антигены и многие другие поверхностные рецепторы, необходимые для действия в антигенпредставляющей, фагоцитарный, и цитотоксический роли, которые различают нормальные макрофаги. Микроглия также отличается от макрофагов тем, что они гораздо более жестко регулируются в пространстве и во времени, чтобы поддерживать точный иммунный ответ.[16]
Еще одно различие между микроглией и другими клетками, которые дифференцируются от миелоидных клеток-предшественников, заключается в скорости обновления. Макрофаги и дендритные клетки постоянно расходуются и заменяются миелоидные клетки-предшественники которые дифференцируются в нужный тип. Из-за гематоэнцефалический барьер, организму будет довольно сложно постоянно заменять микроглию. Поэтому вместо постоянной замены на миелоидные клетки-предшественники, микроглия сохраняет свой статус-кво, пока находится в состоянии покоя, а затем, когда они активируются, они быстро размножаются, чтобы поддерживать свою численность. Однако исследования костных химер показали, что в случаях крайней инфекционное заболевание то гематоэнцефалический барьер ослабнет, и микроглия будет заменена гематогенными клетками костного мозга, а именно миелоидные клетки-предшественники и макрофаги. Как только инфекция уменьшилась, разрыв между периферической и центральной системами восстанавливается, и только микроглия присутствует в период восстановления и отрастания.[30]
Старение
Микроглия подвергается вспышке митотический активность при травме; за этим распространением следует апоптоз чтобы уменьшить количество ячеек до исходного уровня.[31] Активация микроглии создает нагрузку на анаболический и катаболический механизмы клеток, вызывающие гибель активированной микроглии раньше, чем неактивированные клетки.[31] Чтобы компенсировать потерю микроглии с течением времени, микроглия подвергается митозу и происходит из костного мозга. клетки-предшественники мигрируют в мозг через мозговые оболочки и сосудистая сеть.[31]
Накопление незначительных повреждений нейронов, возникающих при нормальном старении, может трансформировать микроглию в увеличенные и активированные клетки.[32] Это хроническое возрастное повышение активации микроглии и экспрессии IL-1 может способствовать увеличению риска болезни Альцгеймера с возрастом, способствуя образованию нейритных бляшек у восприимчивых пациентов.[32] Повреждение ДНК может способствовать возрастной активации микроглии. Еще одним фактором может быть накопление конечные продукты с улучшенным гликированием, которые накапливаются с возрастом.[32] Эти белки очень устойчивы к протеолитическим процессам и способствуют развитию белка. сшивание.[32]
Исследования обнаружили дистрофическую (дефектную) микроглию человека. «Эти клетки характеризуются аномалиями в их цитоплазматической структуре, такими как дерамифицированные, атрофические, фрагментированные или необычно извилистые отростки, часто имеющие сфероидальные или луковичные вздутия».[31] Частота возникновения дистрофической микроглии увеличивается с возрастом.[31] О дегенерации и смерти микроглии сообщалось в исследованиях Прионная болезнь, Шизофрения и болезнь Альцгеймера, что указывает на то, что ухудшение микроглии может быть связано с нейродегенеративными заболеваниями.[31] Сложность этой теории состоит в том, что в человеческом мозге трудно различить «активированную» и «дистрофическую» микроглию.[31]
На мышах было показано, что блокада CD22 восстанавливает гомеостатический микроглиальный фагоцитоз в стареющем мозге.[33]

Клиническое значение
Микроглия - это первичные иммунные клетки центральной нервной системы, похожие на периферические макрофаги. Они реагируют на патогены и травмы, изменяя морфологию и мигрируя к месту инфекции / травмы, где они уничтожают патогены и удаляют поврежденные клетки. В рамках своего ответа они секретируют цитокины, хемокины, простагландины и активные формы кислорода, которые помогают направлять иммунный ответ. Кроме того, они играют важную роль в разрешении воспалительной реакции за счет производства противовоспалительных цитокинов. Микроглия также была тщательно изучена на предмет ее вредной роли при нейродегенеративных заболеваниях, таких как болезнь Альцгеймера, болезнь Паркинсона, рассеянный склероз, а также сердечных заболеваниях, глаукоме, вирусных и бактериальных инфекциях. Накапливаются доказательства того, что иммунная дисрегуляция вносит свой вклад в патофизиологию обсессивно-компульсивного расстройства (ОКР), синдрома Туретта и аутоиммунных нейропсихиатрических расстройств у детей, связанных со стрептококковыми инфекциями (PANDAS).[34]
История
Способность просматривать и характеризовать различные нервные клетки, включая микроглию, появилась в 1880 году, когда красители по Нисслю были разработаны Франц Ниссль. Франц Ниссль и Ф. Робертсон впервые описали микроглиальные клетки во время их гистология эксперименты. Методы окрашивания клеток в 1880-х годах показали, что микроглия связана с макрофаги. Активация микроглии и образование разветвленных кластеров микроглии были впервые отмечены Виктор Бабеш во время изучения бешенство дела в 1897 году. Бабеш отметил, что клетки были обнаружены во множестве популярный инфекции головного мозга, но не знал, какие скопления микроглии он видел.[35] Пио-дель-Рио-Ортега, студент Сантьяго Рамон-и-Кахаль, впервые назвал клетки «микроглией» примерно в 1920 году. В 1927 году он охарактеризовал реакцию микроглии на поражения мозга и отметил «фонтаны микроглии», присутствующие в мозолистом теле и других перинатальных тканях. белое вещество области в 1932 году. После многих лет исследований Рио Хортега стал общепризнанным «отцом микроглии».[36][37] В течение долгого времени наши знания о микроглии не улучшались. Затем, в 1988 году, Хики и Кимура показали, что периваскулярные микроглиальные клетки происходят из костного мозга и экспрессируют высокие уровни MHC класс II белки, используемые для презентации антигена. Это подтвердило постулат Пио Дель Рио-Хортеги о том, что клетки микроглии функционируют аналогично макрофаги выполняя фагоцитоз и презентация антигена.[нужна цитата ]
Смотрите также
Рекомендации
- ^ Ginhoux F, Lim S, Hoeffel G, Low D, Huber T (2013). «Происхождение и дифференциация микроглии». Границы клеточной неврологии. 7: 45. Дои:10.3389 / fncel.2013.00045. ЧВК 3627983. PMID 23616747.
- ^ Лоусон LJ, Перри VH, Гордон S (1992). «Оборот резидентной микроглии в нормальном мозге взрослой мыши». Неврология. 48 (2): 405–15. Дои:10.1016/0306-4522(92)90500-2. PMID 1603325.
- ^ Филиано А.Дж., Гадани С.П., Кипнис Дж. (Август 2015 г.). «Взаимодействие врожденного и адаптивного иммунитета в развитии и функционировании мозга». Исследование мозга. 1617: 18–27. Дои:10.1016 / j.brainres.2014.07.050. ЧВК 4320678. PMID 25110235.
- ^ Кройцберг Г.В. (март 1995 г.). «Микроглия - первая линия защиты при патологиях головного мозга». Arzneimittel-Forschung. 45 (3A): 357–60. PMID 7763326.
- ^ Бушонг Э.А., Мартон М.Э., Джонс Ю.З., Эллисман М.Х. (январь 2002 г.). «Протоплазматические астроциты в лучевом слое CA1 занимают отдельные анатомические домены». Журнал неврологии. 22 (1): 183–92. Дои:10.1523 / JNEUROSCI.22-01-00183.2002. PMID 11756501.
- ^ а б c d е ж грамм час я j k л Германн Дж., Мацумото Ю., Кройцберг Г.В. (март 1995 г.). «Микроглия: внутренняя иммуноэффекторная клетка головного мозга». Исследование мозга. Обзоры исследований мозга. 20 (3): 269–87. Дои:10.1016 / 0165-0173 (94) 00015-H. PMID 7550361.
- ^ Диссинг-Олесен Л., Ладеби Р., Нильсен Х. Х., Тофт-Хансен Х., Далмау И., Финсен Б. (октябрь 2007 г.). «Аксональное поражение, вызванное пролиферацией микроглии и образование кластеров микроглии у мышей». Неврология. 149 (1): 112–22. Дои:10.1016 / j.neuroscience.2007.06.037. PMID 17870248.
- ^ Кирдорф и Принц, J Clin Invest. 2017; 127 (9): 3201–3209. https://doi.org/10.1172/JCI90602.
- ^ Cserép C, Pósfai B, Lénárt N, Fekete R, László ZI, Lele Z, et al. (Январь 2020 г.). «Микроглия контролирует и защищает функцию нейронов с помощью специализированных соматических пуринергических соединений». Наука. 367 (6477): 528–537. Bibcode:2020Sci ... 367..528C. Дои:10.1126 / science.aax6752. PMID 31831638. S2CID 209343260.
- ^ а б c Верхратский А, Приклад А (2013). Глиальная физиология и патофизиология. Честер: Джон Уайли и сыновья. ISBN 978-1118402054.[страница нужна ]
- ^ а б c Hickman SE, Kingery ND, Ohsumi TK, Borowsky ML, Wang LC, Means TK, El Khoury J (2013). «Сенсома микроглии, выявленная прямым секвенированием РНК». Природа Неврология. 16 (12): 1896–905. Дои:10.1038 / № 3554. ЧВК 3840123. PMID 24162652.
- ^ Блок, М.Л., Зекка, Л., Хонг, Дж. Нейротоксичность, опосредованная микроглией: раскрытие молекулярных механизмов. Nat. Rev. Neurosci. 2007. Т. 8. С. 57–69.
- ^ Джи П., Шахтшнайдер К.М., Шук Л.Б., Уокер Ф.Р., Джонсон Р.В. (2016). «Периферическая вирусная инфекция индуцировала гены сенсомных микроглии и повышала активность микроглиальных клеток в гиппокампе новорожденных поросят». Мозг, поведение и иммунитет. 54: 243–251. Дои:10.1016 / j.bbi.2016.02.010. ЧВК 4828316. PMID 26872419.
- ^ Хориучи М., Смит Л., Маэдзава И., Джин Л. В. (2017). «Абляция CX3CR1 улучшает моторные и респираторные дисфункции и улучшает выживаемость мышей с синдромом Ретта». Мозг, поведение и иммунитет. 60: 106–116. Дои:10.1016 / j.bbi.2016.02.014. ЧВК 5531048. PMID 26883520.
- ^ Бергон А., Белзо Р., Конт М., Пеллетье Ф., Эрве М., Гардинер Э. Дж. И др. (2015). «CX3CR1 не регулируется в крови и головном мозге больных шизофренией» (PDF). Исследование шизофрении. 168 (1–2): 434–43. Дои:10.1016 / j.schres.2015.08.010. PMID 26285829.
- ^ а б c d е ж грамм Алоизи Ф (ноябрь 2001 г.). «Иммунная функция микроглии». Глия. 36 (2): 165–79. Дои:10.1002 / glia.1106. PMID 11596125.
- ^ а б c Кристенсен Р.Н., Ха Б.К., Сан Ф., Бреснахан Дж.С., Битти М.С. (июль 2006 г.). «Каинат вызывает быстрое перераспределение актинового цитоскелета в амебоидной микроглии». Журнал неврологических исследований. 84 (1): 170–81. Дои:10.1002 / jnr.20865. PMID 16625662.
- ^ Дэвис Э.Дж., Фостер Т.Д., Томас В.Е. (1994). «Клеточные формы и функции микроглии головного мозга». Бюллетень исследований мозга. 34 (1): 73–8. Дои:10.1016/0361-9230(94)90189-9. PMID 8193937.
- ^ Эгген Б.Дж., Радж Д., Ханиш Великобритания, Боддеке Х.В. (сентябрь 2013 г.). «Микроглиальный фенотип и адаптация». Журнал нейроиммунной фармакологии. 8 (4): 807–23. Дои:10.1007 / s11481-013-9490-4. PMID 23881706.
- ^ Лан X, Хан X, Ли Q, Ян QW, Ван Дж (июль 2017 г.). «Модуляторы активации и поляризации микроглии после внутримозгового кровоизлияния». Нат Рев Нейрол. 13 (7): 420–433. Дои:10.1038 / nrneurol.2017.69. ЧВК 5575938. PMID 28524175.
- ^ Елинек Х.Ф., Карпериен А., Босомайер Т., Бьюкен А. (1975). «Дифференциация степеней активации микроглии с помощью фрактального анализа» (PDF). Complexity International. 12 (18): 1713–7. Архивировано из оригинал (PDF) 17 декабря 2008 г.
- ^ а б Феррер I, Бернет Э, Сориано Э, дель Рио Т, Фонсека М. (1990). «Естественная смерть клеток в коре головного мозга крысы и удаление мертвых клеток временными фагоцитами». Неврология. 39 (2): 451–8. Дои:10.1016/0306-4522(90)90281-8. PMID 2087266.
- ^ Rissi DR, Oliveira FN, Rech RR, Pierezan F, Lemos RA, Barros CS (2006). "Epidemiologia, sinais clínicos e distribuição das lesões encefálicas em bovinos afetados por meningoencefalite por herpesvírus bovino-5" [Эпидемиология, клинические признаки и распространение энцефалических поражений у крупного рогатого скота, пораженных менингоэнцефалитом, вызванным вирусом герпеса-5 крупного рогатого скота]. Pesquisa Veterinária Brasileira (на португальском). 26 (2): 123–32. Дои:10.1590 / S0100-736X2006000200010.
- ^ а б Риттер М.Р., Банин Е., Морено С.К., Агилар Е., Доррелл М.И., Фридлендер М. (декабрь 2006 г.). «Миелоидные предшественники дифференцируются в микроглию и способствуют восстановлению сосудов в модели ишемической ретинопатии». Журнал клинических исследований. 116 (12): 3266–76. Дои:10.1172 / JCI29683. ЧВК 1636693. PMID 17111048.
- ^ Чунг В.С., Уэльс, Калифорния, Баррес Б.А., Стивенс Б. (ноябрь 2015 г.). «Управляет ли глия синаптическими и когнитивными нарушениями при болезни?». Природа Неврология. 18 (11): 1539–1545. Дои:10.1038 / № 4142. ЧВК 4739631. PMID 26505565.
- ^ Банно М., Мизуно Т., Като Х. и др. (2005). «Поглотитель радикалов эдаравон предотвращает окислительную нейротоксичность, вызванную пероксинитритом и активированной микроглией». Нейрофармакология. 48 (2): 283–90. Дои:10.1016 / j.neuropharm.2004.10.002. PMID 15695167.
- ^ Cserép C, Pósfai B, Lénárt N, Fekete R, László ZI, Lele Z, et al. (Январь 2020 г.). «Микроглия контролирует и защищает функцию нейронов с помощью специализированных соматических пуринергических соединений». Наука. 367 (6477): 528–537. Bibcode:2020Sci ... 367..528C. Дои:10.1126 / science.aax6752. PMID 31831638. S2CID 209343260.
- ^ Ginhoux F, Prinz M (июль 2015 г.). «Происхождение микроглии: современные концепции и прошлые споры». Перспективы Колд-Спринг-Харбор в биологии. 7 (8): a020537. Дои:10.1101 / cshperspect.a020537. ЧВК 4526747. PMID 26134003.
- ^ Zhu H, Wang Z, Yu J, Yang X, He F, Liu Z, Che F, Chen X, Ren H, Hong M, Wang J (март 2019). «Роль и механизмы цитокинов при вторичном повреждении головного мозга после внутримозгового кровоизлияния». Прог. Нейробиол. 178: 101610. Дои:10.1016 / j.pneurobio.2019.03.003. PMID 30923023.
- ^ Германн Дж (1996). «Микроглия: датчик угроз для нервной системы?». Исследования в вирусологии. 147 (2–3): 79–88. Дои:10.1016/0923-2516(96)80220-2. PMID 8901425.
- ^ а б c d е ж грамм Streit WJ (сентябрь 2006 г.). «Старение микроглии: есть ли у иммунной системы мозга срок годности?». Тенденции в неврологии. 29 (9): 506–10. Дои:10.1016 / j.tins.2006.07.001. PMID 16859761.
- ^ а б c d Мрак Р.Э., Гриффин В.С. (март 2005 г.). «Глии и их цитокины в прогрессировании нейродегенерации». Нейробиология старения. 26 (3): 349–54. Дои:10.1016 / j.neurobiolaging.2004.05.010. PMID 15639313.
- ^ Pluvinage JV, Wyss-Coray T, et al. (11 апреля 2019 г.). «Блокада CD22 восстанавливает гомеостатический фагоцитоз микроглии в стареющем мозге». Природа. 568 (7751): 187–192. Дои:10.1038 / s41586-019-1088-4. ЧВК 6574119.
- ^ Фрик, Лучиана; Питтенгер, Кристофер (2016). «Нарушение регуляции микроглии при ОКР, синдроме Туретта и PANDAS». Журнал иммунологических исследований. Дои:10.1155/2016/8606057.
- ^ Бабеш, В.М. (1892). "Определенные характеристики гистологических поражений бешенства" [Некоторые характеристики гистологических поражений бешенства]. Annales de l'Institut Pasteur (На французском). 6: 209–23.
- ^ дель Рио Ортега П., Пенфилд В. (1892 г.). «Церебральный рубец: реакция нейроглии и микроглии на раны головного мозга». Бюллетень больницы Джонса Хопкинса. 41: 278–303.
- ^ дель Рио-Хортега F (1937). «Микроглия». Цитология и клеточная патология нервной системы: 481–534.
дальнейшее чтение
- Rock RB, Gekker G, Hu S, Sheng WS, Cheeran M, Lokensgard JR, Peterson PK (октябрь 2004 г.). «Роль микроглии в инфекциях центральной нервной системы». Обзоры клинической микробиологии. 17 (4): 942–64, содержание. Дои:10.1128 / CMR.17.4.942-964.2004. ЧВК 523558. PMID 15489356.
- Хан X, Li Q, Lan X и др. (Февраль 2019). «Истощение микроглии липосомами клодроната увеличивает уровни провоспалительных цитокинов, вызывает активацию астроцитов и повреждает целостность кровеносных сосудов». Мол Нейробиол. Дои:10.1007 / s12035-019-1502-9. ЧВК 6684378. PMID 30734229.
внешняя ссылка
- Домашняя страница Microglia на microglia.net
- Закрадывается в вашу голову - краткое введение в микроглию - Обзор журнала Science Creative Quarterly
- "Поглотители иммунитета нацелены на бляшки Альцгеймера". 6 апреля 2007 г.
- В Кафедра неврологии в Викиверситет
- Поиск NIF - микроглиальная клетка через Информационная структура по неврологии
