Нейтральная сеть (эволюция) - Neutral network (evolution)
А нейтральная сеть это набор гены все связаны точечные мутации которые имеют эквивалентную функцию или фитнес.[1] Каждый узел представляет последовательность гена, а каждая линия представляет мутацию, соединяющую две последовательности. Нейтральные сети можно рассматривать как высокие плоские плато в фитнес-ландшафт. В течение нейтральная эволюция, гены могут случайным образом перемещаться через нейтральные сети и пересекать области пространство последовательности что может иметь последствия для надежность и эволюционируемость.
Генетические и молекулярные причины
Нейтральные сети существуют в фитнес-пейзажи поскольку белки крепкий мутациям. Это приводит к расширенным сетям генов эквивалентной функции, связанных между собой нейтральные мутации.[2][3] Белки устойчивы к мутациям, потому что многие последовательности могут складываться в очень похожие структурные складки.[4] Белок принимает ограниченный набор нативных конформаций, потому что эти конформеры имеют более низкую энергию, чем развернутые и неправильно свернутые состояния (ΔΔG сворачивания).[5][6] Это достигается за счет распределенной внутренней сети кооперативных взаимодействий (гидрофобный, полярный и ковалентный ).[7] Структурная устойчивость белка является результатом того, что несколько одиночных мутаций достаточно разрушительны, чтобы нарушить функцию. Белки также эволюционировали, чтобы избежать агрегирование[8] поскольку частично свернутые белки могут объединяться в большие повторяющиеся нерастворимые белковые фибриллы и массы.[9] Есть свидетельства того, что белки обладают отрицательными конструктивными особенностями, снижающими воздействие склонных к агрегации. бета-лист мотивы в их структурах.[10]Кроме того, есть некоторые свидетельства того, что генетический код сам по себе может быть оптимизирован так, чтобы большинство точечных мутаций приводили к аналогичным аминокислотам (консервативный ).[11][12] Вместе эти факторы создают распределение фитнес-эффектов мутаций, которые содержат высокую долю нейтральных и почти нейтральных мутаций.[13]
Эволюция
Нейтральные сети - это подмножество последовательностей в пространство последовательности которые имеют эквивалентную функцию и образуют широкую плоскую плато в фитнес-ландшафт. Нейтральная эволюция Таким образом, можно представить себе популяцию, распространяющуюся от одного набора узлов последовательности через нейтральную сеть к другому кластеру узлов последовательности. Поскольку большая часть эволюции считается нейтральной,[14][15] большая часть изменений генов - это движение через обширные нейтральные сети.
Надежность
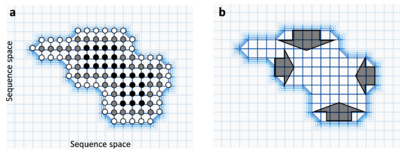
Чем больше нейтральных соседей имеет последовательность, тем больше устойчив к мутациям это потому, что мутации с большей вероятностью просто нейтрально превратят его в равно функциональную последовательность.[1] В самом деле, если есть большие различия между числом нейтральных соседей разных последовательностей в нейтральной сети, прогнозируется, что популяция будет развиваться в сторону этих устойчивых последовательностей. Иногда это называется циркум-нейтральностью и представляет собой перемещение населения от скал в фитнес-ландшафт.[16]
Помимо моделей in silico,[17] эти процессы начинают подтверждаться экспериментальная эволюция из цитохром P450s[18] и В-лактамаза.[19]
Эволюционируемость
Интерес к взаимодействию между генетический дрейф а отбор существует с 1930-х годов, когда теория смещения баланса предположила, что в некоторых ситуациях генетический дрейф может способствовать более поздней адаптивной эволюции.[20] Хотя специфика теории была в значительной степени дискредитирована,[21] он обратил внимание на возможность того, что дрейф может вызвать загадочные изменения, которые, хотя и нейтральны по отношению к текущей функции, могут повлиять на выбор для новых функций (эволюционируемость ).[22]
По определению, все гены в нейтральной сети имеют эквивалентную функцию, однако некоторые могут демонстрировать беспорядочная деятельность которые могут служить отправной точкой для адаптивной эволюции к новым функциям.[23][24] С точки зрения пространство последовательности Современные теории предсказывают, что если нейтральные сети для двух разных видов деятельности перекрываются, нейтрально развивающаяся популяция может распространиться в регионы нейтральной сети первой активности, которые позволят ей получить доступ ко второй.[25] Это будет только в том случае, если расстояние между видами деятельности меньше, чем расстояние, которое может преодолеть нейтрально развивающаяся популяция. Степень взаимопроникновения двух сетей будет определять, насколько распространены загадочные вариации беспорядочной активности в пространстве последовательностей.[26]
Математическая основа
Тот факт, что нейтральные мутации, вероятно, были широко распространены, был предложен Фризом и Йошидой в 1965 году.[27] Мотоо Кимура позже выкристаллизовал теорию нейтральной эволюции в 1968 г.[28] Кинг и Джакс независимо друг от друга предложили аналогичную теорию (1969).[29] Кимура вычислил скорость нуклеотидных замен в популяции (то есть среднее время замены одной пары оснований в геноме) и обнаружил, что она составляет ~ 1,8 года. Такой высокий показатель не будет терпеть ни одна популяция млекопитающих, согласно Холдейн формула. Таким образом, он пришел к выводу, что у млекопитающих нейтральные (или почти нейтральные) мутации нуклеотидных замен ДНК должен доминировать. Он подсчитал, что такие мутации происходят примерно со скоростью 0-5 в год на гамету.

В последующие годы появилась новая парадигма, РНК как молекула-предшественник ДНК. Принцип первичной молекулы был выдвинут еще в 1968 г. Крик,[30] и привести к тому, что сейчас известно как Гипотеза мира РНК.[31] ДНК обнаруживается, преимущественно, полностью базовая пара двойные спирали, а биологические РНК является одноцепочечным и часто демонстрирует сложные взаимодействия спаривания оснований. Это связано с его повышенной способностью формировать водородные связи, факт, который проистекает из существования дополнительных гидроксил группа в рибоза сахар.
В 1970-х годах Штейн и М. Уотерман заложил основу комбинаторики РНК второстепенные конструкции.[32] Waterman дал первое теоретико-графическое описание РНК вторичные структуры и связанные с ними свойства, и использовали их для создания эффективных минимум свободной энергии (MFE) алгоритм сворачивания.[33] An РНК вторичную структуру можно рассматривать как диаграмму над N помеченными вершинами с ее Watson-Crick пар оснований представлены в виде непересекающихся дуг в верхней полуплоскости. Следовательно, вторичная структура представляет собой каркас, имеющий множество последовательностей, совместимых с предполагаемыми ограничениями спаривания оснований. Потом, Смит и Уотерман разработали алгоритм, выполняющий локальное выравнивание последовательностей.[34] Другой алгоритм прогнозирования для РНК вторичная структура была дана Нусинов[35] Алгоритм Нусинова описал проблему сворачивания двухбуквенного алфавита как задачу оптимизации плоского графа, где величина, которая должна быть максимизирована, - это количество совпадений в строке последовательности.
Придет 1980 год, Хауэлл и др. вычислил производящую функцию всех сверток последовательности[36] пока Д. Санкофф (1985) описали алгоритмы выравнивания конечных последовательностей, предсказания вторичных структур РНК (сворачивание) и реконструкции протопоследовательностей на филогенетическом дереве.[37] Потом, Waterman и храм (1986) произвел полиномиальное время динамическое программирование (DP) алгоритм для прогнозирования общих РНК вторичная структура.[38] в то время как в 1990 году Джон Маккаскилл представил алгоритм DP с полиномиальным временем для вычисления полной равновесной статистической суммы вторичной структуры РНК.[39]
М. Цукер, реализованные алгоритмы вычисления MFE РНК второстепенные конструкции[40] на основе работы Нусинов и другие.,[35] Смит и Уотерман[34] и Studnicka, et al.[41] Позже Л. Хофакер (и др., 1994),[42] представил Венский пакет РНК, программный пакет, который интегрировал сворачивание MFE и вычисление статистической суммы, а также вероятностей образования пары оснований.
Питер Шустер и W. Fontana (1994) сместили акцент с последовательностей на структурные карты (генотип-фенотип ). Они использовали алгоритм обратного сворачивания, чтобы получить вычислительные доказательства того, что РНК последовательности, имеющие одинаковую структуру, распределяются случайным образом в пространство последовательности. Они заметили, что общие структуры могут быть получены из случайной последовательности всего за несколько мутаций. Эти два факта приводят их к выводу, что пространство последовательностей казалось просачивающийся нейтральными сетями ближайших соседних мутантов, которые складываются в одну и ту же структуру.[43]
В 1997 г. К. Рейдис Стадлер и Шустер заложены математические основы исследования и моделирования нейтральных сетей РНК второстепенные конструкции. Используя модель случайного графа они доказали существование порогового значения для связности случайных подграфов в конфигурационном пространстве, параметризованного λ, долей нейтральных соседей. Они показали, что сети связаны и просачиваться пространство последовательности, если доля нейтральных ближайших соседей превышает λ *, пороговое значение. Ниже этого порога сети делятся на самые большие гигантский компонент и несколько более мелких. Ключевые результаты этого анализа касались пороговых функций для плотности и связности для нейтральных сетей, а также Шустер Космическая гипотеза.[43][44][45]
Смотрите также
Рекомендации
- ^ а б ван Нимвеген, Э; Кратчфилд, JP; Хуйнен, М. (17 августа 1999 г.). «Нейтральная эволюция мутационной устойчивости». Труды Национальной академии наук Соединенных Штатов Америки. 96 (17): 9716–20. arXiv:adap-org / 9903006. Bibcode:1999PNAS ... 96.9716V. Дои:10.1073 / пнас.96.17.9716. ЧВК 22276. PMID 10449760.
- ^ Таверна, DM; Гольдштейн, РА (18 января 2002 г.). «Почему белки так устойчивы к сайт-мутациям?». Журнал молекулярной биологии. 315 (3): 479–84. Дои:10.1006 / jmbi.2001.5226. PMID 11786027.
- ^ Токурики, N; Тауфик, Д.С. (октябрь 2009 г.). «Эффекты стабильности мутаций и эволюционируемости белков». Текущее мнение в структурной биологии. 19 (5): 596–604. Дои:10.1016 / j.sbi.2009.08.003. PMID 19765975.
- ^ Мейергуз, Л; Клейнберг, Дж; Эльбер, Р. (10 июля 2007 г.). «Сеть потока последовательностей между белковыми структурами». Труды Национальной академии наук Соединенных Штатов Америки. 104 (28): 11627–32. Bibcode:2007ПНАС..10411627М. Дои:10.1073 / pnas.0701393104. ЧВК 1913895. PMID 17596339.
- ^ Карплюс, М. (17 июня 2011 г.). «За схемой складной воронки». Природа Химическая Биология. 7 (7): 401–4. Дои:10.1038 / nchembio.565. PMID 21685880.
- ^ Токурики, N; Stricher, F; Schymkowitz, J; Серрано, L; Тауфик, Д.С. (22 июня 2007 г.). «Эффекты стабильности протеиновых мутаций, по-видимому, универсальны». Журнал молекулярной биологии. 369 (5): 1318–32. Дои:10.1016 / j.jmb.2007.03.069. PMID 17482644.
- ^ Шахнович Б.Е .; Дела, E; Делиси, С; Шахнович, E (март 2005 г.). «Структура белка и история эволюции определяют топологию пространства последовательностей». Геномные исследования. 15 (3): 385–92. arXiv:q-bio / 0404040. Дои:10.1101 / гр.3133605. ЧВК 551565. PMID 15741509.
- ^ Monsellier, E; Chiti, F (август 2007 г.). «Предотвращение амилоидоподобной агрегации как движущей силы эволюции белка». Отчеты EMBO. 8 (8): 737–42. Дои:10.1038 / sj.embor.7401034. ЧВК 1978086. PMID 17668004.
- ^ Финк А.Л. (1998). «Агрегация белков: сворачивающиеся агрегаты, тельца включения и амилоид». Складывание и дизайн. 3 (1): R9-23. Дои:10.1016 / с 1359-0278 (98) 00002-9. PMID 9502314.
- ^ Ричардсон, Дж. С.; Ричардсон, округ Колумбия (5 марта 2002 г.). «Природные белки с бета-слоями используют негативный дизайн, чтобы избежать агрегации от края до края». Труды Национальной академии наук Соединенных Штатов Америки. 99 (5): 2754–9. Bibcode:2002PNAS ... 99.2754R. Дои:10.1073 / pnas.052706099. ЧВК 122420. PMID 11880627.
- ^ Мюллер, ММ; Эллисон, младший; Hongdilokkul, N; Гайон, L; Каст, П; ван Гунстерен, ВФ; Marlière, P; Хилверт, Д. (2013). «Направленная эволюция модельного первичного фермента дает представление о развитии генетического кода». PLOS Genetics. 9 (1): e1003187. Дои:10.1371 / journal.pgen.1003187. ЧВК 3536711. PMID 23300488.
- ^ Фирнберг, Э; Остермайер, М. (август 2013 г.). «Генетический код сдерживает, но способствует дарвиновской эволюции». Исследования нуклеиновых кислот. 41 (15): 7420–8. Дои:10.1093 / nar / gkt536. ЧВК 3753648. PMID 23754851.
- ^ Хиетпас, RT; Дженсен, JD; Болонь Д.Н. (10 мая 2011 г.). «Экспериментальное освещение фитнес-ландшафта». Труды Национальной академии наук Соединенных Штатов Америки. 108 (19): 7896–901. Bibcode:2011PNAS..108.7896H. Дои:10.1073 / pnas.1016024108. ЧВК 3093508. PMID 21464309.
- ^ Кимура, Мотоо. (1983). Нейтральная теория молекулярной эволюции. Кембридж
- ^ Кимура, М. (1968). «Скорость эволюции на молекулярном уровне». Природа. 217 (5129): 624–6. Bibcode:1968Натура.217..624К. Дои:10.1038 / 217624a0. PMID 5637732. S2CID 4161261.
- ^ Proulx, SR; Адлер, Франция (июль 2010 г.). «Эталон нейтралитета: все еще развевается на ветру?». Журнал эволюционной биологии. 23 (7): 1339–50. Дои:10.1111 / j.1420-9101.2010.02006.x. PMID 20492093. S2CID 7774510.
- ^ van Nimwegen E .; Кратчфилд Дж. П .; Хуйнен М. (1999). «Нейтральная эволюция мутационной устойчивости». PNAS. 96 (17): 9716–9720. Bibcode:1999PNAS ... 96.9716V. Дои:10.1073 / пнас.96.17.9716. ЧВК 22276. PMID 10449760.
- ^ Блум, JD; Lu, Z; Чен, Д; Раваль, А; Вентурелли, ОС; Арнольд, FH (17 июля 2007 г.). «Эволюция способствует устойчивости белков к мутации в достаточно больших популяциях». BMC Биология. 5: 29. arXiv:0704.1885. Дои:10.1186/1741-7007-5-29. ЧВК 1995189. PMID 17640347.
- ^ Берштейн, Шимон; Гольдин, Корина; Тауфик, Дэн С. (июнь 2008 г.). «Интенсивные нейтральные дрейфы дают надежные и эволюционирующие консенсусные белки». Журнал молекулярной биологии. 379 (5): 1029–1044. Дои:10.1016 / j.jmb.2008.04.024. PMID 18495157.
- ^ Райт, Сьюэл (1932). «Роли мутации, инбридинга, скрещивания и отбора в эволюции». Материалы Шестого Международного конгресса генетиков: 356–366.
- ^ Coyne, JA; Barton NH; Турелли М (1997). «Перспектива: критика теории эволюции сдвига баланса Сьюэла Райта». Эволюция. 51 (3): 643–671. Дои:10.2307/2411143. JSTOR 2411143. PMID 28568586.
- ^ Дэвис, Э. К. (10 сентября 1999 г.). «Высокая частота скрытых вредных мутаций у Caenorhabditis elegans». Наука. 285 (5434): 1748–1751. Дои:10.1126 / наука.285.5434.1748. PMID 10481013.
- ^ Masel, J (март 2006 г.). «Скрытые генетические вариации обогащены для потенциальных адаптаций». Генетика. 172 (3): 1985–91. Дои:10.1534 / генетика.105.051649. ЧВК 1456269. PMID 16387877.
- ^ Hayden, EJ; Феррада, Э; Вагнер, А (2 июня 2011 г.). «Скрытая генетическая изменчивость способствует быстрой эволюционной адаптации фермента РНК» (PDF). Природа. 474 (7349): 92–5. Дои:10.1038 / природа10083. PMID 21637259. S2CID 4390213.
- ^ Борнберг-Бауэр, Э; Huylmans, AK; Сикосек, Т. (июнь 2010 г.). «Как возникают новые белки?». Текущее мнение в структурной биологии. 20 (3): 390–6. Дои:10.1016 / j.sbi.2010.02.005. PMID 20347587.
- ^ Вагнер, Андреас (14.07.2011). Истоки эволюционных инноваций: теория трансформационных изменений в живых системах. Оксфорд [и др.]: Издательство Оксфордского университета. ISBN 978-0199692590.
- ^ Фриз, Э. и Йошида, А. (1965). Роль мутаций в эволюции. В V Bryson и HJ Vogel, ред. Развивающиеся гены и белки, стр. 341-55. Академический, Нью-Йорк.
- ^ Кимура, М. (1968). «Скорость эволюции на молекулярном уровне». Природа. 217 (5129): 624–6. Bibcode:1968Натура.217..624К. Дои:10.1038 / 217624a0. PMID 5637732. S2CID 4161261.
- ^ King, JL; Джукс, TH (1969). «Недарвиновская эволюция». Наука. 164 (3881): 788–97. Bibcode:1969Sci ... 164..788L. Дои:10.1126 / science.164.3881.788. PMID 5767777.
- ^ Крик, FH (1968). «Происхождение генетического кода». Журнал молекулярной биологии. 38 (3): 367–79. Дои:10.1016/0022-2836(68)90392-6. PMID 4887876.
- ^ Робертсон, член парламента; Джойс, GF (2012). «Истоки мира РНК». Перспективы Колд-Спринг-Харбор в биологии. 4 (5): а003608. Дои:10.1101 / cshperspect.a003608. ЧВК 3331698. PMID 20739415.
- ^ Stein, P.R .; Уотерман, М. (1978). «О некоторых новых последовательностях, обобщающих числа Каталонии и Моцкина». Дискретная математика. 26 (3): 261–272. Дои:10.1016 / 0012-365x (79) 90033-5.
- ^ РС. Уотерман. Вторичная структура одноцепочечных нуклеиновых кислот. Adv. Математика. I (доп.), 1: 167–212, 1978.
- ^ а б Smith, Temple F .; Уотерман, Майкл С. (1981). «Идентификация общих молекулярных подпоследовательностей». Журнал молекулярной биологии. 147 (1): 195–197. Дои:10.1016/0022-2836(81)90087-5. PMID 7265238.
- ^ а б Нусинив; и другие. (1978). «Алгоритмы сопоставления петель». СИАМ. 35: 68–82.
- ^ Howell, J.A .; Smith, T.F .; Уотерман, М. (1980). «Вычисление производящих функций для биологических молекул». SIAM J. Appl. Математика. 39: 119133. Дои:10.1137/0139010.
- ^ Дэвид Санкофф. Одновременное решение проблем сворачивания, выравнивания и протопоследовательности РНК. 1985/10 SIAM Journal on Applied Mathematics Volume 45 Issue 5 Pages 810-825
- ^ Waterman, M.S .; Смит, Т.Ф. (1986). «Алгоритмы быстрого динамического программирования вторичной структуры РНК». Adv. Appl. Математика. 7 (4): 455–464. Дои:10.1016/0196-8858(86)90025-4.
- ^ Маккаскилл, Джон (1990). «Равновесная функция распределения и вероятности связывания пар оснований для вторичной структуры РНК». Биополимеры. 29 (6–7): 1105–19. Дои:10.1002 / bip.360290621. HDL:11858 / 00-001M-0000-0013-0DE3-9. PMID 1695107. S2CID 12629688.
- ^ Цукер, Майкл; Стиглер, Патрик (1981). «Оптимальное компьютерное сворачивание больших последовательностей РНК с использованием термодинамики». Исследования нуклеиновых кислот. 9 (1): 133–148. Дои:10.1093 / nar / 9.1.133. ЧВК 326673. PMID 6163133.
- ^ Studnicka, Gary M .; Ран, Джорджия М .; Каммингс, Ян У .; Зальсер, Уинстон А. (1978-09-01). «Компьютерный метод предсказания вторичной структуры одноцепочечной РНК». Исследования нуклеиновых кислот. 5 (9): 3365–3388. Дои:10.1093 / nar / 5.9.3365. ISSN 0305-1048. ЧВК 342256. PMID 100768.
- ^ Hofacker, I.L .; Fontana, W .; Stadler, P.F .; и другие. (1994). «Быстрое сворачивание и сравнение вторичных структур РНК». Monatsh Chem. 125 (2): 167. Дои:10.1007 / BF00818163. S2CID 19344304.
- ^ а б Шустер, Питер; Фонтана, Уолтер; Стадлер, Питер Ф .; Хофакер, Иво Л. (22 марта 1994 г.). «От последовательностей к формам и обратно: пример вторичных структур РНК». Труды Лондонского королевского общества B: биологические науки. 255 (1344): 279–284. Bibcode:1994RSPSB.255..279S. Дои:10.1098 / rspb.1994.0040. ISSN 0962-8452. PMID 7517565. S2CID 12021473.
- ^ «Нейтральные сети вторичных структур РНК» (PDF).
- ^ Hofacker, Ivo L .; Шустер, Питер; Стадлер, Питер Ф. (1998). «Комбинаторика вторичных структур РНК». Дискретная прикладная математика. 88 (1–3): 207–237. Дои:10.1016 / s0166-218x (98) 00073-0.
