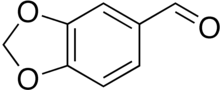
Пиперональ - Piperonal
 | |
| Имена | |
|---|---|
| Название ИЮПАК 1,3-бензодиоксол-5-карбальдегид | |
| Другие имена Гелиотропин; Гелиотропин; Пиперонилальдегид; Метиленовый эфир протокатехинового альдегида; 3,4-метилендиоксибензальдегид; | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.004.009 |
| UNII | |
| |
| |
| Характеристики | |
| C8ЧАС6О3 | |
| Молярная масса | 150.133 г · моль−1 |
| Внешность | Бесцветные кристаллы[1] |
| Плотность | 1,337 г / см3 |
| Температура плавления | 37 ° С (99 ° F, 310 К)[1] |
| Точка кипения | 263 ° С (505 ° F, 536 К)[1] |
| Растворим в 500 частях[1] | |
| Опасности | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 2700 мг / кг (перорально крысам)[1] |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Пиперональ, также известный как гелиотропин, является органическое соединение который обычно содержится в ароматизаторах и ароматизаторах.[2] Молекула структурно связана с другими ароматный альдегиды Такие как бензальдегид и ванилин.
Естественное явление
Пиперональ в природе встречается в различных растениях. Примеры включают укроп, ваниль, фиолетовые цветы, и черный перец.
Подготовка
Пиперонал можно получить окислительным расщеплением изосафрол или используя многоступенчатую последовательность из катехол или же 1,2-метилендиоксибензол. Синтез последнего химического вещества осуществляется через реакция конденсации с глиоксиловая кислота с последующим раскалывание результирующий α-гидроксикислота с окислитель.[2][3][4] Синтез катехола требует дополнительной стадии, Синтез эфира Вильямсона с помощью дихлорметан.[5]
Реакции
Пиперональ, как и все альдегиды, возможно уменьшенный к его алкоголь (пиперониловый спирт) или окисленный, чтобы дать его кислота (пиперониловая кислота).
Пиперонал может быть использован в синтезе некоторых фармацевтических препаратов, в том числе тадалафил,[6] L-ДОПА,[7] и Атрасентан.[8]
Аромат
Пиперональ имеет цветочный запах, который обычно описывают как похожий на запах ванилина или вишня. По этой причине он обычно используется в ароматах и искусственные ароматизаторы.[2] Соединение было названо гелиотропином в честь нот вишневого пирога, обнаруженных в цветок гелиотропа аромат (даже если химического вещества нет в истинном аромате цветка).[9] Парфюмеры впервые начали использовать аромат к началу 1880-х годов.[10] Он обычно используется для добавления нюансов ванили или миндаля, обычно придавая бальзамический, пудровый и цветочный характер аромату.[11]
Пиперонилацетат синтетический ароматизатор вишни.[12]
Рекомендации
- ^ а б c d е Budavari, Susan, ed. (1996), Индекс Merck: энциклопедия химикатов, лекарств и биологических препаратов (12-е изд.), Merck, ISBN 0911910123
- ^ а б c Карл-Георг Фальбуш, Франц-Йозеф Хаммершмидт, Йоханнес Пантен, Вильгельм Пикенхаген, Дитмар Шатковски, Курт Бауэр, Доротея Гарбе и Хорст Зурбург «Вкус и ароматизаторы» в Энциклопедии промышленной химии Ульмана, Вайли-VCH, 2003. Дои:10.1002 / 14356007.a11_141
- ^ Фатиади, Александр и Шаффер, Роберт (1974). «Улучшенная процедура синтеза DL-4-гидрокси-3-метоксимандальной кислоты (DL-« ваниллил »-миндальная кислота, VMA)». Журнал исследований Национального бюро стандартов Раздел A. 78A (3): 411–412. Дои:10.6028 / jres.078A.024.
- ^ Нвауква, Стивен; Кин, Филипп (1982). «Окислительное расщепление α-диолов, α-дионов, α-гидроксикетонов и α-гидрокси- и α-кетокислот с гипохлоритом кальция [Ca (OCl)2]". Буквы Тетраэдра. 23 (31): 3135–3138. Дои:10.1016 / S0040-4039 (00) 88578-0.
- ^ Бонтрон, В. и Корнфорт, Дж. (1969). «Метиленирование катехинов». Журнал химического общества (9): 1202–1204. Дои:10.1039 / J39690001202.
- ^ Gilla, G .; Anumula, R.R .; Aalla, S .; Вуримиди, Х. и Ганта, М.Р. (2013). «Синтез и характеристика родственных веществ и метаболита тадалафила, ингибитора ФДЭ-5» (PDF). Органические коммуникации. 6 (1): 12–22.
- ^ Ямада, Шун-Ичи; Fujii, Tozo; Шиоири, Такаюки (1962). «Исследования оптически активных аминокислот. I. Получение 3- (3,4-метилендиоксифенил) -D- и -L-аланина». Химико-фармацевтический бюллетень. 10 (8): 680. Дои:10.1248 / cpb.10.680.
- ^ Винн, Мартин; фон Гельдерн, Томас В .; Opgenorth, Терри Дж .; Джэ, Хван-Су; Таскер, Эндрю С .; Бойд, Стивен А .; Кестер, Джеффри А .; Mantei, Robert A .; Бал, Радхика; Соренсен, Брайан К .; Wu-Wong, Jinshyun R .; Chiou, William J .; Диксон, Дуглас Б.; Новосад, Евгений И .; Эрнандес, Лиза; Марш, Кеннан С. (1996). «2,4-диарилпирролидин-3-карбоновые кислоты, обладающие активными ETAS-селективными антагонистами рецепторов эндотелина. 1. Открытие A-127722». Журнал медицинской химии. 39 (5): 1039–1048. Дои:10.1021 / jm9505369. ISSN 0022-2623.
- ^ http://www.bojensen.net/EssentialOilsEng/EssentialOils13A/EssentialOils13A.htm
- ^ Сила моды в политике и обществе: Глобальные перспективы от раннего Нового времени до наших дней Беверли Лемир ISBN 9781409404927
- ^ Запись в базе данных компании Good Scents для Гелиотропин
- ^ Справочник ароматических ингредиентов Фенароли.
