Жан-Пьер Шенжу - Jean-Pierre Changeux
Жан-Пьер Шенжу | |
|---|---|
 | |
| Родившийся | 6 апреля 1936 г. Domont, Франция |
| Национальность | Франция |
| Альма-матер | École Normale Supérieure Институт Пастера |
| Известен | Модель MWC, изоляция нАЧР |
| Супруг (а) | Энни Дюпон (м. 1962) |
| Дети | 1 сын |
| Награды | Премия Вольфа в области медицины (1982) Премия Луи-Жанте в области медицины (1993)[1] Медаль сэра Ганса Кребса (1994) Приз Бальзана (2001) Мировая премия имени Альберта Эйнштейна в области науки (2018) |
| Научная карьера | |
| Поля | Неврология |
| Учреждения | Коллеж де Франс Институт Пастера |
| Докторант | Жак Моно, Франсуа Жакоб |
Жан-Пьер Шенжу (Французский:[ʃɑ̃ʒø]; родился 6 апреля 1936 г.) - француз нейробиолог известен своими исследованиями в нескольких областях биология, из структуры и функции белки (с акцентом на аллостерический белков), к раннему развитию нервная система вплоть до когнитивных функций. Хотя он известен в биологических науках благодаря Модель MWC, идентификация и очистка никотиновый рецептор ацетилхолина и теория эпигенеза путем отбора синапсов также являются заметными научными достижениями. Чангуз известен ненаучной публике своими идеями о связи между разумом и физическим мозгом. Как сказано в его книге, Беседы о разуме, материи и математикеChangeux решительно поддерживает точку зрения о том, что нервная система функционирует скорее в проективном, чем в реактивном стиле, и что взаимодействие с окружающей средой, а не поучительное, приводит к выбору среди множества ранее существовавших внутренних репрезентаций.
биография
Changeux родился в Domont, Франция - Марселю Шенгу и Жанне Бенуа.[2] Он вошел в École Normale Supérieure в 1955 году, где он получил Степень бакалавра (Лицензия) в 1957 г. и Степень магистра (Diplome d'Études Supérieure) в 1958 году. агрегация по естествознанию в том же году. Он начал свою научную карьеру во время учебы в ENS во время летней стажировки в Баньюльс-сюр-Мер где он выделил новый род паразитарныхКопепода. Он преследовал кандидат наук учится в Институт Пастера под руководством Жак Моно и Франсуа Жакоб и получил докторскую степень в 1964 году. После этого Чанжо покинул Францию для обучения в докторантуре. Калифорнийский университет в Беркли (1965–1966), затем в Колледж врачей и хирургов Колумбийского университета, Нью-Йорк (1967). Он вернулся во Францию в качестве атташе на кафедру молекулярной биологии, которую возглавляет Жак Моно. В 1972 году он стал директором отделения молекулярной нейробиологии в Институт Пастера, где он получил звание профессора в 1975 году. В 1975 году Чанже был избран профессором Коллеж де Франс, председатель Cell Communications, должность, которую он занимал до 2006 года. Changeux является автором более 600 научных статей и нескольких книг, технических или для широкой аудитории.
Научные достижения
На протяжении всей своей научной карьеры Ченжакс был верен горстке научных вопросов на молекулярном, клеточном и мозговом уровнях. Если кому-то нужно искать объединяющую тему для всех, это убеждение, что в основе жизненных процессов лежит отбор, а не инструкция. Хотя начатые как отдельные направления исследований, все исследовательские нити были связаны в последние десятилетия с изучением аллостерических механизмов как основы для участия никотиновые рецепторы в когнитивные функции.
Аллостерия

Во время его кандидат наук исследования в лаборатории Жак Моно и Франсуа Жакоб, Changeux изучил аллостерические правила из ферменты, то есть модуляция их активности соединениями, отличными от их субстраты.[3][4][5] Эта работа привела к развитию модель согласованных переходов за аллостерический белки.[6][7] Основные идеи, лежащие в основе этой теории: 1) белки может существовать в различных конформациях в тепловое равновесие при отсутствии регуляторов. Аллостерические регуляторы просто сдвигают равновесие между конформациями, стабилизируя те, к которым они проявляют наибольшее сродство, и 2) все субъединицы симметричного мультимерного белка существуют в одной и той же конформации, причем переход происходит в согласованный мода. Полученная модель объясняет наблюдаемые сотрудничество без прогрессирующего изменения биофизических параметров. Эта концептуальная основа до сих пор является основной моделью, используемой для объяснения функции кооперативных белков, таких как гемоглобин.
В своей докторской диссертации Changeux предположил, что распознавание и передача сигналов мембрана, и в частности синапсы, могут использовать те же механизмы, что и аллостерическая регуляция ферментов. Затем последовали более сорока лет исследований, в основном сосредоточенных на никотиновых рецепторах ацетилхолина (см. Ниже). В 1967 году Changeux расширил модель MWC на двумерную решетку рецепторы[8] (идея, которая также была развита три десятилетия спустя Деннис Брей[9]). Затем он применил эту идею к постсинаптической мембране электрические органы (аналог поперечно-полосатые мышцы ).[10][11] Его команда продемонстрировала существование нескольких взаимопревращаемых состояний никотинового рецептора: покоя, открытого и десенсибилизированного, демонстрируя различное сродство к лигандам, таким как эндогенный агонист. ацетилхолин.[12][13][14] Переходы между состояниями следовали разной кинетике, и этой кинетики плюс дифференциальное сродство было достаточно, чтобы объяснить форму постсинаптического потенциала. Полная механистическая модель никотинового рецептора из поперечнополосатой мышцы (или электрического органа) должна была быть предоставлена намного позже, когда Ченжакс сотрудничал со Стюартом Эдельштейном, другим специалистом по аллостерии, который десятилетиями работал над этим. гемоглобин.[15] Помимо аллостерической модуляции стробирования канала агонистами, с тех пор было обнаружено множество других регуляторов активности лиганд-зависимых ионных каналов. Модуляторы связываются с множеством аллостерических сайтов, будь то сайты связывания агонистов, другие сайты связывания на границах раздела субъединиц, в цитоплазматической части белка или в трансмембранном домене.[16]
Концепция аллостерической фармакологии[17] для ионных каналов разрабатывалась годами. В дополнение к хорошо известным Положительные аллостерические модуляторы рецептора ГАМК (Такие как бензодиазепины и барбитурат препараты) можно найти противопаразитарные препараты, такие как ивермектин[18] и модуляторы рецепторов глутамата, используемые против Болезнь Альцгеймера Такие как анирацетам.
Структура никотиновых рецепторов
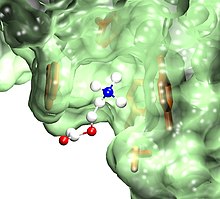
В 1970 году Changeux изолировал никотиновый рецептор ацетилхолина угря электрический орган, первый в истории изолированный мембранный фармакологический рецептор,[20] что он смог идентифицировать благодаря свойствам змеиного токсина, который был очищен тайваньскими исследователями CY Lee и CC Chang.[21] О выделении рецептора позже также сообщили Рикардо Миледи.[22] Совершенствование методов очистки, разработанных в группе[23] позволил предположить, что рецептор был пентамерный белок,[24] находка быстро подтвердилась командой Артура Карлина.[25] Группа Changeux была одной из первых, кто выяснил первичную структуру субъединиц рецептора,[26][27] параллельно с группой Шосаку Нума[28] и Стивен Хайнеманн.[29]
На протяжении 1980-х и 1990-х годов методы молекулярной биологии использовались для расшифровки третичной и четвертичной структуры рецептора. Было идентифицировано расположение ионной поры, состоящей из второго трансмембранного сегмента,[30] как показано позже также группами Шосаку Нума[31] и Фердинанд Хучо.[32] Молекулярные основы ионной селективности также были идентифицированы в трансмембранном домене.[33][34][35] Структура сайта связывания ацетилхолина и никотина была расположена на границе раздела между соседними субъединицами.[36][37][38]
Поиски Changeux для структуры никотинового рецептора завершились опубликованием структуры бактериального гомолога с атомным разрешением в открытом доступе.[39] и отдыхает[40] конформации, поддерживающие концепцию симметричного согласованного отверстия для стробирования канала,[41] в соответствии с расчетами молекулярной динамики.[42][43]
Стабилизация синапсов нейрональной активностью
В 1973 году вместе с Филиппом Куррежем и Антуан Данчен, Changeux предложил модель, описывающую, как во время разработки нервная система, активность сети может вызвать стабилизацию или регресс синапсы участвует[44] и проиллюстрировал это нервно-мышечным соединением. Эта модель, по сути, является предшественником теории «нейронного дарвинизма», которую далее продвигает Джеральд Эдельман. Позже Changeux расширил и проиллюстрировал эту идею.[45] В 1970-х годах он попытался задокументировать этот феномен, изучая животных-мутантов.[46][47] или экспериментальной денервацией.[48][49]
Функция никотиновых рецепторов

В то время как до 1990-х годов группа Changeux изучала структуру никотинового рецептора, присутствующего в электрические органы электрического угря и торпеды, исследования физиологической роли этих рецепторов были в основном сосредоточены на двух модельных системах: никотиновых рецепторах нервномышечное соединение, синапс, связывающий моторнейрон к скелетные мышцы и никотиновые рецепторы мозга, особенно в связи с никотиновой зависимостью.
С середины 1980-х годов группа изучала сопоставление мышечных клеток в процессе развития в качестве модели синаптогенеза и в связи с теоретической работой по эпигенезу. В частности, группа сосредоточилась на накоплении никотиновых рецепторов в постсинаптической области в процессе развития, что сопровождается переключением идентичности рецепторов. Они смогли расшифровать различные сигнальные пути, участвующие в ответе на синаптическую активность, показывая, что накопление происходит в результате ингибирования транскрипции гена вне синаптической области из-за электрической активности, запускающей поглощение кальция и активацию PKC,[50][51][52][53] и стимуляция транскрипции гена в синапсе пептидом, связанным с геном кальцитонина (CGRP), активирующим PKA[54][55][56] и каскады тирозинкиназы, активирующие ARIA (херегулин).[57][58]
В 1990-е годы интерес к Changeux постепенно смещался с нервно-мышечного соединения на никотиновые рецепторы, экспрессируемые в головном мозге. Среди заметных достижений группы - открытие того, что нейронные никотиновые рецепторы очень проницаемы для кальция.[59] - что объясняет положительное влияние никотиновых рецепторов на высвобождение многих нейротрансмиттеров в головном мозге.[60]
Группа также обнаружила, что никотиновый рецептор регулируется множеством «аллостерических модуляторов», таких как: 1. ионы кальция.[61] (Это также было независимо обнаружено группой Джона Дэни[62]), сайты связывания которых были позже идентифицированы[19][63] и локализованы во внеклеточном домене, на границе раздела между субъединицами (Le Novère et al. 2002); 2. ивермектин[18] который ведет себя как мощный положительный аллостерический модулятор, связывающийся с участком трансмембранного домена (где общие анестетики также связываются[64]); 3. фосфорилирование цитоплазматического домена[65] которые регулируют десенсибилизацию.
К середине 1990-х Чанжакс сосредоточил большую часть своего интереса на функции никотиновых рецепторов в базальных ганглиях и, в частности, в мезэнцефальной дофаминергической системе. Используя мышей, удаленных для генов никотиновых рецепторов, группа охарактеризовала типы субъединиц рецептора, присутствующие в дофаминергических клетках.[66][67][68] и идентифицировали рецепторы, в основном ответственные за зависимость от никотина, образованные субъединицами α4, α6 и β2.[69][70]
Моделирование познания
С середины 1990-х годов Changeux разработал деятельность по компьютерному моделированию, чтобы исследовать нейронные основы когнитивных функций. Это исследование в основном проводилось в сотрудничестве с Станислас Дехаене, теперь возглавляет Отделение когнитивной нейровизуализации INSERM-CEA. Они особенно смоделировали приобретение распознавания песен у птиц.[71] и развитие числовых способностей.[72] Совсем недавно Дехаен и Ченжакс разработали нейронную модель доступа к сознанию, основанную на привлечении в масштабе всего мозга сетей нейронов с аксонами дальнего действия, называемую глобальным рабочим пространством нейронов.[73][74] Модель может иметь клиническое применение, например, для понимания механизма комы, действия общих анестетиков.[75] или наркомания[76]
Профессиональная и ненаучная деятельность
Публикация его книги Нейронный человек: биология разума в 1985 году принесла Changeux статус знаменитости среди широкой публики. С тех пор он является автором или соавтором нескольких других книг, вдохновленных его преподаванием в College de France: в частности, Беседы о разуме и математике с математиком Аленом Конном (1998), Что заставляет нас думать с философом Полем Рикером (2002) и Физиология истины (2002), которые, как считается, положили начало поучительному диалогу между двумя часто враждебными дисциплинами нейробиологии и философии. Его также интересовали отношения между эстетическим опытом и мозгом в Raison & Plaisir (1994), Истина - хорошее - прекрасное: нейробиологический подход (2012) и недавно Les Neurones Enchantés. (2014), где он обсуждает вопрос художественного творчества с композиторами Пьером Булезом и Филиппом Манури. Чанжакс получил премию Льюиса Томаса за научные труды Рокфеллерского университета, Нью-Йорк, 2005 г.
Changeux также был куратором трех крупных выставок по искусству и науке: De Nicolo dell'Abate à Nicolas Poussin: aux sources du Classicisme 1550-1650 Musée Bossuet Meaux в 1988, L'Âme au Corps, Arts et Sciences, 1793-1993 (совместно с Жераром Ренье) Национальные галереи Grand Palais Paris в 1993–1994 годах и La lumière au siècle des Lumières et aujourd'hui. Искусство и наука: биология видения à une nouvelle concept du monde Galeries Poirel Nancy в 2005 году. Шенгу также возглавлял межведомственную комиссию по сохранению французского художественного наследия с 1989 года и был членом научного совета Международного агентства музеев с 2007 года.
Наконец, на протяжении всей своей карьеры Чангуза беспокоили этические последствия для города и общества в целом недавнего прогресса в нейробиологии. С 1992 по 1998 год Чанжо возглавлял Национальный консультативный комитет по биоэтике во Франции. Он организовал научную конференцию по этой теме, результатом которой стала книга, которую он редактировал: fondements naturel de l'ethique. В настоящее время он является сопредседателем отдела этики и общества Европейской программы человеческого мозга (с 2013 года).
Он также входит в состав Совета научных управляющих Научно-исследовательский институт Скриппса, независимый некоммерческий институт, специализирующийся на биомедицинских исследованиях.
Общественное признание
Основные научные премии и награды
- 1978: Международная премия Фонда Гейрднера
- 1982: Премия Фонда Вольфа в области медицины
- 1982: премия Ричарда-Лунсбери Академии наук США и Французской академии наук
- 1991: медаль Карла-Густава-Бернхарда Шведская Академия Наук
- 1992: Золотая медаль CNRS.
- 1993: Премия Луи-Жанте в области медицины
- 1994: Премия Гудмана и Гилмана в фармакологии рецепторов лекарств
- 1998: Премия Эмануэля Мерка по химии, Дармштадт
- 2001: Приз Бальзана для когнитивных нейронаук
- 2002: Американское философское общество Премия Карла Спенсера Лэшли в неврологии
- 2005: Приз Льюиса Томаса для статей о науке
- 2005: Золотая Эвридика
- 2007: Премия NAS в области нейробиологии от Национальная Академия Наук[77]
- 2012: Премия Японского общества содействия науке (JSPS) для выдающихся ученых
- 2016: Международная исследовательская премия от Фонд Олафа Тона (Осло)[78]
- 2018: Мировая премия имени Альберта Эйнштейна в области науки предоставленный Всемирный культурный совет[79]
- 2018: Премия Гольдмана-Ракича за выдающиеся достижения в области когнитивной нейробиологии[80]
Академическое членство и почетные степени
Deutsche Akademie der Naturforscher Leopoldina zu Halle (фармакология), 1974; Туринская медицинская академия, 1976 год; Национальная Академия Наук, Вашингтон (США) (иностранный сотрудник), 1983 г .; Королевская академия наук, Стокгольм (Швеция) (иностранный член), 1985 г .; Академия наук, Париж, 1988 год; Королевская медицинская академия Бельгии (Брюссель) (иностранный почетный член), 1988 год; Academia Europaea (член-учредитель), 1988 г .; Американская академия искусств и наук, Бостон (США) (иностранный член), 1994; Румынская академия медицинских наук, Бухарест (иностранный член), 1996 г .; Институт медицины национальных академий, Вашингтон (США) (иностранный сотрудник), 2000 г .; Istituto Veneto di Scienze, Lettere Ed Arti, Венеция (Италия), 2001 г .; Венгерская академия наук, Будапешт (иностранный член-корреспондент), 2004 г .; Европейская академия наук, Брюссель (член), 2004 г .; Международная академия гуманизма; Королевская академия наук Бельгийской литературы и изящных искусств (иностранный член), 2010 г .; Accademia Nazionale dei Lincei, Рим (Италия) (иностранный член), 2010 г.
Почетный доктор: университеты Турина, Италия, 1989 г .; Данди, Шотландия, 1992 год; Женева, Швейцария, 1994 год; Стокгольм, Швеция, 1994 г .; Льеж, Бельгия, 1996 год; Федеральная политехническая школа Лозанны, Швейцария, 1996 год; Университет Южной Калифорнии, Лос-Анджелес, США, 1997 г .; Бат, Великобритания, 1997 год; Монреальский университет, Канада, 2000 год; Еврейский университет Иерусалима, Израиль, 2004 г .; Университет штата Огайо, Колумбус, США, 2007 г .; Университет Буэнос-Айреса, Аргентина, 2010 г.
Почетный член Программы исследований нейронаук Массачусетского технологического института и Рокфеллеровского университета (США) с 1984 г .; Почетный член Японского биохимического общества, Сендай, Япония, 1985; Почетный член Американской ассоциации неврологов, 1988; Почетный член Университетского колледжа Лондона, 1990; Membre d'honneur à titre étranger de la Société Belge de Neurologie, Брюссель, 1991; Член Европейской организации молекулярной биологии.
Ненаучные награды
Grand Croix dans l'Ordre de la Légion d'Honneur, 2010 год; Гран-Круа в Национальном ордене Мерита, 1995 год; Commandeur dans l'Ordre des Arts et des Lettres, 1994.
Научные публикации исторического значения
- Monod, J .; Wyman, J .; Changeux, Дж. П. (1965). «О природе аллостерических переходов: правдоподобная модель». Журнал молекулярной биологии. 12: 88–118. Дои:10.1016 / S0022-2836 (65) 80285-6. PMID 14343300. (в котором Жак Моно, Джеффрис Вайман и Жан-Пьер Шанжо представили согласованная модель аллостерических переходов, что объясняет кооперативность многих аллостерических белков, таких как гемоглобин)
- Changeux J.-P., Kasai M., Huchet M., Meunier J.-C. (1970). Извлечение из электрической ткани гимнастической ткани, представляющей плюс собственников caractéristiques du récepteur Physicologique de l'acétylcholine. C. R. Acad. Sci. 270D: 2864-2867. (первая очистка рецептора нейротрансмиттера. Поскольку статья на французском языке, большинство людей цитируют описание токсина, которое позволило идентифицировать рецептор: Changeux, J .; Kasai, M .; Ли, К. (1970). «Использование токсина змеиного яда для характеристики белка холинергического рецептора». Труды Национальной академии наук Соединенных Штатов Америки. 67 (3): 1241–1247. Bibcode:1970PNAS ... 67.1241C. Дои:10.1073 / pnas.67.3.1241. ЧВК 283343. PMID 5274453.
- Changeux, J .; Courrège, P .; Данчин, А. (1973). «Теория эпигенеза нейронных сетей путем избирательной стабилизации синапсов». Труды Национальной академии наук Соединенных Штатов Америки. 70 (10): 2974–2978. Bibcode:1973PNAS ... 70.2974C. Дои:10.1073 / пнас.70.10.2974. ЧВК 427150. PMID 4517949. (В которой авторы разрабатывают формальную модель отбора синапсов, предшественника «нейронного дарвинизма». Это оригинальная работа, хотя большинство людей цитируют последующий обзор [более подходящий для неспециализированной аудитории и представляющий биологический контекст]: Changeux JP, Danchin A (1976) Nature, 264 (1976) 705-712.)
Книги Жан-Пьера Шенжу
- Changeux, Жан-Пьер. (2008) Du vrai, du beau, du bien: Une Nouvelle Approche Neuronale
- Changeux, Жан-Пьер; Стюарт Эдельштейн. (2004) Никотиновые ацетилхолиновые рецепторы: от молекулярной биологии к познанию
- Changeux, Жан-Пьер. (2002) L'Homme de Verite (2004 Физиология истины)
- Changeux, Жан-Пьер; Поль Рикёр. (1998) Ce qui nous fait penser (2002 Что заставляет нас думать. Нейробиолог и философ спорят об этике, природе человека и мозге[81][82])
- Changeux, Жан-Пьер. (1994) Raison et Plaisir
- Changeux, Жан-Пьер; Ален Конн. (1989) Matière à pensée (1995 Беседы о разуме, материи и математике)
- Changeux, Жан-Пьер. (1983) L'homme нейронный (1985 Нейронный человек: биология разума)
Рекомендации
- ^ Премия Луи-Жанте
- ^ The International Кто есть кто 2004. Психология Press. 2003. с. 299. ISBN 9781857432176.
- ^ Changeux J.-P. (1961). Механизм обратной связи биосинтетической L-треониндезаминазы с помощью L-изолейцина. Колд-Спринг-Харбор. Symp. Quant. Биол. 26: 313-318.
- ^ Changeux J.-P. (1963). Аллостерические взаимодействия на биосинтетической L-теониндезаминазе из E. coli K12. Колд-Спринг-Харб Symp Quant Biol, 28: 497-504
- ^ Monod J., Changeux J.-P., Jacob. Ф. (1963). Аллостерические белки и клеточные системы контроля. J. Mol. Биол. 6: 306-329
- ^ Монод Дж., Вайман Дж. И Ченжакс Ж.-П. (1965). О природе аллостерических переходов: правдоподобная модель. J. Mol. Биол. 12: 88-118.
- ^ Рубин М.М., Ченжакс Ж.-П. (1966). О природе аллостерических переходов; последствия неисключительного связывания лиганда. J. Mol. Биол. 21: 265-274.
- ^ Changeux J.-P., Thiéry J.-P., Tung Y. и Kittel C. (1967). О кооперативности биологических мембран. Proc. Natl. Акад. Sci. USA 57, 335-341.
- ^ Bray D, Levin MD, Morton-Firth CJ (1998) Кластеризация рецепторов как клеточный механизм контроля чувствительности. Природа, 393: 85-88.
- ^ Changeux J.-P., Podleski T.R. (1968). О возбудимости и кооперативности электролактической мембраны. Proc. Natl. Акад. Sci. США 59: 944-950
- ^ Cartaud J., Benedetti E.L., Cohen J.B., Meunier J.C., Changeux J.-P. (1973) Наличие решетчатой структуры в фрагментах мембран, богатых никотиновым рецепторным белком электрического органа Torpedo marmorata. FEBS Lett. 33: 109-113.
- ^ Weber M., David-Pfeuty M.T., Changeux J.-P. (1975). Регуляция связывающих свойств белка никотинового рецептора холинергическими лигандами в мембранных фрагментах Torpedo marmorata. Proc. Natl. Акад. Sci. США 72: 3443-3447.
- ^ Сугияма Х., Чангукс Ж.-П. (1975). Взаимное преобразование между различными состояниями сродства к ацетилхолину холинергического рецепторного белка Torpedo marmorata. Евро. J. Biochem. 55: 505-515.
- ^ Heidmann T., Changeux J.-P. (1979). Быстрые кинетические исследования взаимодействия флуоресцентного агониста с мембраносвязанным рецептором ацетилхолина T. marmorata. Евро. J. Biochem. 94: 255-279.
- ^ Эдельштейн С., Шаад О., Генри Э., Бертран Д. Шанжукс Ж.-П. (1996). Кинетический механизм никотиновых рецепторов ацетилхолина, основанный на множественных аллостерических переходах. Биол. Киберн. 75: 361-379
- ^ Changeux J.-P. (2012). Концепция аллостерической модуляции: обзор. Drug Discov. Сегодня 10: e223-e228
- ^ Christopoulos, A; Changeux, J. P .; Catterall, W. A .; Fabbro, D; Burris, T. P .; Cidlowski, J. A .; Olsen, R.W .; Peters, J. A .; Neubig, R. R .; Pin, J. P .; Секстон, П. М .; Кенакин, Т. П .; Ehlert, F.J .; Спеддинг, М; Лэнгмид, К. Дж. (2014). "Международный союз фундаментальной и клинической фармакологии. XC. Многопозиционная фармакология: Рекомендации по номенклатуре рецепторной аллостеризма и аллостерических лигандов". Фармакологические обзоры. 66 (4): 918–47. Дои:10.1124 / пр.114.008862. PMID 25026896.
- ^ а б Krause, R.M .; Buisson, B; Бертран, S; Коррингер, П. Дж .; Galzi, J. L .; Changeux, J. P .; Бертран, Д. (1998). «Ивермектин: положительный аллостерический эффектор нейронального никотинового ацетилхолинового рецептора альфа7». Молекулярная фармакология. 53 (2): 283–94. Дои:10.1124 / моль 53.2.283. PMID 9463487.
- ^ а б Le Novère N., Grutter T., Changeux J.-P. (2002). Модели внеклеточного домена никотиновых рецепторов и сайтов связывания агонистов и Са ++. Proc. Natl. Акад. Sci. США, 99: 3210-3215.
- ^ Changeux J.-P., Kasai M., Huchet M., Meunier J.-C. (1970). Извлечение из электрической ткани гимнастической ткани, представляющей плюс собственников caractéristiques du récepteur Physicologique de l'acétylcholine. C. R. Acad. Sci. 270D: 2864-2867.
- ^ Changeux J.-P., Kasai M. и Lee C.Y. (1970). Использование токсина змеиного яда для характеристики белка холинергического рецептора. Proc. Natl. Акад. Sci. USA 67: 1241-1247.
- ^ Миледи Р., Молинофф П., Поттер Л.Т. (1971). Выделение холинэргического рецепторного белка электрической ткани Torpedo. Nature 229: 554-557.
- ^ Olsen R., Meunier J.C., Changeux J.-P. (1972). Прогресс в очистке холинергического рецепторного белка из Electrophorus electricus с помощью аффинной хроматографии. FEBS Lett. 28., 96-100.
- ^ Hucho F., Changeux J.-P. (1973). Молекулярный вес и четвертичная структура холинергического рецепторного белка, экстрагированного детергентами из электрической ткани Electrophorus electricus. FEBS Lett. 38: 11-15
- ^ Weill C.L., McNamee M.G., Karlin A. (1974) Аффинное мечение очищенного рецептора ацетилхолина от Torpedo Californica. Biochem Biophys Res Comm 61: 997-1003.
- ^ Devillers-Thiéry A., Changeux J.-P., Paroutaud P. и Strosberg A.D. (1979). Аминоконцевая последовательность субъединицы с молекулярной массой 40 000 белка рецептора ацетилхолина из Torpedo marmorata. FEBS Lett. 104: 99-105.
- ^ Devillers-Thiéry A., Giraudat J., Bentaboulet M., Changeux J.-P. (1983).Полная последовательность мРНК связывающей ацетилхолин альфа-субъединицы ацетилхолинового рецептора Torpedo marmorata: модель трансмембранной организации полипептидной цепи. Proc. Natl. Акад. Sci. США 80: 2067-2071.
- ^ Нода М., Такахаши Х., Танабе Т., Тойосато М., Фурутани Ю., Хиросе Т., Асаи М., Инаяма С., Мията Т., Нума С. (1982) Первичная структура предшественника альфа-субъединицы Ацетилхолиновый рецептор Torpedo californica выведен из последовательности кДНК. Nature 299: 793-797.
- ^ Балливет М., Патрик Дж., Ли Дж., Хайнеманн С. (1982) Молекулярное клонирование кДНК, кодирующей гамма-субъединицу ацетилхолинового рецептора Torpedo. Proc Natl Acad Sci U S. A. 79: 4466-4470.
- ^ Giraudat J., Dennis M., Heidmann T., Chang J.Y., Changeux J.-P. (1986). Структура сайта с высоким сродством для неконкурентных блокаторов рецептора ацетилхолина: серин-262 дельта-субъединицы мечен [3H] -хлорпромазином. Proc. Natl. Акад. Sci. США 83: 2719-2723.
- ^ Имото К., Метфессель К., Сакманн Б., Мишина М., Мори Ю., Конно Т., Фукуда К., Курасаки М., Буджо Х., Фудзита Ю., Шосаку Н. (1986). Расположение области дельта-субъединицы, определяющей транспорт ионов через канал рецептора ацетилхолина. Природа. 1986, 18-31 декабря; 324 (6098): 670-4.
- ^ Hucho F., Oberthür W., Lottspeich F. (1986) Ионный канал никотинового рецептора ацетилхолина образован гомологичными спиралями M II субъединиц рецептора. FEBS Lett.205: 137-142.
- ^ Галци Ж.-Л., Девиллер-Тьери А., Хусси Н., Бертран С., Чанже Ж.-П., Бертран Д. (1992). Мутации в домене ионного канала нейронального никотинового рецептора превращают ионную селективность из катионной в анионную. Nature 359: 500-505.
- ^ Бертран Д., Галци Ж.-Л., Девиллер-Тьери А., Бертран С., Чанжо Ж.-П. (1993). Мутации в двух разных сайтах в домене канала M2 изменяют кальциевую проницаемость нейронального никотинового рецептора альфа7. Proc. Natl. Акад. Sci. США 90: 6971-6975.
- ^ Корринджер П.-Дж., Бертран С., Галци Ж.-Л., Девиллер-Тьери А., Шенжё Ж.-П., Бертран Д. (1999). Мутационный анализ фильтра селективности заряда никотинового ацетилхолинового рецептора α7. Нейрон 22: 831-843.
- ^ Dennis M., Giraudat J., Kotzyba-Hibert F., Goeldner M., Hirth C., Chang J.Y., Lazure C., Chrétien M., Changeux J.-P. (1988). Аминокислоты субъединицы ацетилхолинового рецептора Torpedo marmorata, меченные фотоаффинным лигандом для сайта связывания ацетилхолина. Биохимия 27: 2346-2357.
- ^ Galzi J.-L., Revah F., Black D., Goeldner M., Hirth C., Changeux J.-P. (1990). Идентификация новой аминокислоты a-Tyr 93 в активном сайте рецептора ацетилхолина с помощью фотоаффинного мечения: дополнительные доказательства для трехпетлевой модели сайта связывания ацетилхолина. J. Biol. Chem. 265: 10430-10437.
- ^ Галци Ж.-Л., Бертран Д., Девиллер-Тьери А., Рева Ф., Бертран С., Чанжакс Ж.-П. (1991). Функциональное значение ароматических аминокислот из трех пептидных петель участка нейронального никотинового рецептора альфа 7 исследовано с помощью сайт-направленного мутагенеза. FEBS Lett. 294: 198-202.
- ^ Bocquet N., Nury H., Baaden M., Le Poupon C., Changeux J.-P., Delarue M., Corringer P.-J. (2009) Рентгеновская структура ионного канала, управляемого пентамерным лигандом, в явно открытой конформации. Природа 457 (7225): 111-114
- ^ Sauguet, L; Шахсавар, А; Poitevin, F; Юон, C; Мэнни, А; Nemecz, A .; Хауз, А; Changeux, J. P .; Коррингер, П. Дж .; Деларю, М. (2014). «Кристаллические структуры ионного канала, управляемого пентамерным лигандом, обеспечивают механизм активации». Труды Национальной академии наук. 111 (3): 966–71. Bibcode:2014ПНАС..111..966С. Дои:10.1073 / pnas.1314997111. ЧВК 3903189. PMID 24367074.
- ^ Hilf R.J., Dutzler R. (2009) Структура потенциально открытого состояния активированного протонами ионного канала, управляемого пентамерным лигандом. Природа 457 (7225): 115-118
- ^ Тали А., Деларю М., Грюттер Т., Нильж М., Ле Новер Н., Корринджер П.-Ж., Шенжё Ж.-П. (2005) Анализ нормального режима предлагает модель четвертичного скручивания для механизма стробирования никотиновых рецепторов. Биофиз. J. 88: 3954-3965
- ^ Калимет Н., Симоэс М., Чанжеукс Ж.-П., Карплюс М., Тали А., Чеккини М. (2013) С обложки: механизм стробирования ионных каналов, управляемых пентамерным лигандом. Proc Natl Acad Sci U S A. 110: E3987-3996
- ^ Changeux J.-P., Courrège P., Danchin A. (1973). Теория эпигенеза нейронных сетей путем избирательной стабилизации синапсов. Proc. Natl. Акад. Sci. USA 70: 2974-2978.
- ^ Changeux J.-P., Danchin, A. (1976). Избирательная стабилизация развивающихся синапсов как механизм спецификации нейронных сетей. Природа 264: 705-712.
- ^ Сотело К., Ченжакс Ж.-П. (1974). Транссинаптическая дегенерация «каскадом» в коре мозжечка у мутантных мышей. Brain Res. 67: 519-526.
- ^ Mariani J., Crepel F., Mikoshiba K., Changeux J.-P. (1977). Анатомические, физиологические и биохимические исследования мозжечка мышей-мутантов reeler. Фил. Пер. Royal Soc. В 281: 1-28
- ^ Benoit P, Changeux J.P. (1975) Последствия тенотомии для эволюции мультииннервации в развитии камбаловидной мышцы крысы. Мозг Res.99: 354-8
- ^ Хендерсон CE, Huchet M, Changeux JP. Денервация увеличивает активность нейритов в экстрактах скелетных мышц. Природа. 1983, 14 апреля; 302 (5909): 609-11.
- ^ Бец Х., Ченжакс Ж.-П. (1979). Регуляция синтеза мышечных ацетилхолиновых рецепторов in vitro производными циклических нуклеотидов. Nature 278: 749-752.
- ^ Klarsfeld A., Changeux J.-P. (1985). Активность регулирует уровень мРНК альфа-субъединицы ацетилхолинового рецептора в культивируемых мышечных трубках цыплят. Proc. Natl. Акад. Sci. США 82: 4558-4562.
- ^ Klarsfeld A., Laufer R., Fontaine B., Devillers-Thiéry A., Dubreuil C., Changeux J.-P. (1989). Регулирование экспрессии гена альфа-субъединицы AChR в мышцах с помощью электрической активности: участие протеинкиназы C и Ca ++. Нейрон 2: 1229-1236.
- ^ Piette J., Bessereau J.-L., Huchet M., Changeux J.-P. (1990). Два соседних MyoD1-связывающих сайта регулируют экспрессию гена дельта-субъединицы ацетилхолинового рецептора. Nature 345: 353-355.
- ^ Fontaine B., Klarsfeld A., Hokfelt T., Changeux J.-P. (1986). Связанный с геном кальцитонина пептид, пептид, присутствующий в мотонейронах спинного мозга, увеличивает количество рецепторов ацетилхолина в первичных культурах мышечных трубок куриного эмбриона. Neurosci. Lett. 71: 59-65.
- ^ Fontaine B., Klarsfeld A., Changeux J.-P. (1987). Пептид, родственный гену кальцитонина, и мышечная активность регулируют уровни мРНК альфа-субъединицы ацетилхолинового рецептора различными внутриклеточными путями. J. Cell Biol. 105: 1337-1342.
- ^ Laufer R., Changeux J.-P. (1987). Пептид, связанный с геном кальцитонина, повышает уровни циклического АМФ в скелетных мышцах кур: возможная нейротрофическая роль сосуществующего нейронального мессенджера. EMBO J. 6: 901-906.
- ^ Алтиок Н., Бессеро Ж.-Л., Чанжакс Ж.-П. (1995). ErB3 и ErbB2 / neu опосредуют действие херегулина на экспрессию гена рецептора ацетилхолина в мышцах: дифференциальная экспрессия на замыкательной пластинке. EMBO J. 14: 4258-4266.
- ^ Schaeffer L., Duclert N., Huchet-Dymanus M., Changeux J.-P. (1998). Влияние мультисубъединичного фактора транскрипции Ets в синаптическую экспрессию никотинового ацетилхолинового рецептора. EMBO J., 17: 3078-3090.
- ^ Mulle C., Choquet D., Korn H., Changeux J.-P. (1992). Приток кальция через никотиновый рецептор в центральных нейронах крысы: его значение для клеточной регуляции. Нейрон 8: 135-143.
- ^ Léna C, Changeux, JP (1997). Роль ионов Ca2 + в облегчении никотинового высвобождения ГАМК в таламусе мышей. J Neurosci 17: 576-585.
- ^ Mulle C., Léna C., Changeux J.-P. (1992). Усиление ответа никотиновых рецепторов внешним кальцием в центральных нейронах крысы. Нейрон 8: 937-945.
- ^ Vernino S, Amador M, Leutje CW, Patrick J и Dani JA (1992) Модуляция кальция и высокая кальциевая проницаемость нейронных никотиновых рецепторов ацетилхолина. Нейрон 8: 127-134
- ^ Галци Ж.-Л., Бертран С., Корринджер П.-Ж., Ченжакс Ж.-П., Бертран Д. (1996). Идентификация сайтов связывания кальция, которые регулируют усиление нейронального никотинового рецептора ацетилхолина. EMBO J. 15: 5824-5832.
- ^ Нури Х., Ван Рентергем С., Вен Й., Тран А., Бааден М., Дюфресн В., Чанжук Ж.-П., Соннер Дж. М., Деларю М., Коррингер П.-Дж. (2011) Рентгеновские структуры общих анестетиков, связанные с ионным каналом, управляемым пентамерным лигандом. Природа 469 (7330): 428-431
- ^ Тейхберг В.И., Собель А., Чанжакс Ж.-П. (1977) Фосфорилирование рецептора ацетилхолина in vitro. Природа 267 (5611): 540-542
- ^ Le Novère N., Zoli M., Changeux J.-P. (1996). МРНК субъединицы а6 нейронального никотинового рецептора избирательно концентрируется в катехоламинергических ядрах головного мозга крысы. Eur J Neurosci 8: 2428-2439
- ^ Klink R., de Kerchove d'Exaerde A., Zoli M., Changeux J.-P. (2001). Молекулярное и физиологическое разнообразие никотиновых рецепторов ацетилхолина в дофаминергических ядрах среднего мозга. J. Neurosci. 21: 1452-1463.
- ^ Champtiaux N, Gotti C, Cordero-Erausquin M, David DJ, Przybylski C, Lena C, Clementi F, Moretti M, Rossi FM, Le Novere N, McIntosh JM, Gardier AM, Changeux JP (2003) Состав субъединиц функциональных никотиновых рецепторов в дофаминергических нейронах, исследованных на нокаутированных мышах. J. Neurosci., 27 августа 2003 г .; 23 (21): 7820-9.
- ^ Picciotto M.R., Zoli M., Rimondini R., Léna C., Marubio L., Merlo Pich E., Fuxe K., Changeux J.-P. (1998). Рецепторы ацетилхолина, содержащие b2-субъединицу, участвуют в усиливающих свойствах никотина. Nature 391: 173-177 (1998).
- ^ Маскос У., Моллес Б. Э., Понс С., Бессон М., Гьяр Б. П., Гий Дж. П., Эврард А., Казала П., Кормье А., Мамели-Энгвалл М., Дюфур Н., Клоз-Тайарани И., Бемельманс A.-P., Mallet J., Gardier AM, David V., Faure P., Granon S. и Changeux J.-P. (2005) Никотиновое усиление и познание восстанавливаются за счет целевой экспрессии никотиновых рецепторов. Природа 436: 103-107
- ^ Дехен С., Чанжакс Ж.-П., Надаль Ж.П. (1987). Нейронные сети, которые изучают временные последовательности путем выбора. Proc. Natl. Акад. Sci. США 84: 2727-2731.
- ^ Dehaene S., Changeux J.-P. (1993). Развитие элементарных числовых способностей: нейронная модель. J. Cognitive Neurosci 5: 390-407.
- ^ Dehaene S., Kerszberg M., Changeux J.-P. (1998). Нейронная модель глобального рабочего пространства в сложных когнитивных задачах. Proc Natl Acad Sci USA 95: 14529-14534.
- ^ Дехен С., Сержент К., Чанжакс Ж.-П. (2003) Модель нейронной сети, связывающая субъективные отчеты и объективные физиологические данные во время сознательного восприятия. Proc. Natl. Акад. Sci. США, 100: 8520-8525.
- ^ Changeux J.-P. (2012) Обработка сознания: значение для общей анестезии. Curr. Мнение. Анестезиол. 25: 397–404.
- ^ Changeux J.-P., Lou H.C. (2011) Эмерджентная фармакология сознательного опыта: новые перспективы в наркозависимости. FASEB J. 25 (7): 2098-2108.
- ^ «Премия НАН Украины в области неврологии». Национальная академия наук. Архивировано из оригинал 29 декабря 2010 г.. Получено 16 февраля 2011.
- ^ «Международная исследовательская награда от Фонда Олафа Тона 2016». Получено 28 апреля 2016.
- ^ "Le prix Albert-Einstein World Awards of Science 2018 est remis à Jean-Pierre Changeux" (На французском). Коллеж де Франс. 4 июн 2018. Получено 3 июля 2018.
- ^ "Жан-Пьер Чанжу, доктор философии". 29 октября 2018.
- ^ Обзор Что заставляет нас думать Ховард Гарднер В архиве 16 февраля 2005 г. Wayback Machine
- ^ Обзор Что заставляет нас думать Эллиот Уайт В архиве 22 марта 2006 г. Wayback Machine
внешняя ссылка
- Страница Google Scholar Жан-Пьера Ченджукса
- Лаборатория Жан-Пьера Чанжо в 2005 году
- Жан-Пьер Шенжу Фонд Международной премии Бальзана
