Метилформиат - Википедия - Methyl formate
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Метилформиат | |||
| Систематическое название ИЮПАК Метилметаноат | |||
| Другие имена R-611 | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.166 | ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C2ЧАС4О2 | |||
| Молярная масса | 60.052 г · моль−1 | ||
| Внешность | Бесцветная жидкость | ||
| Запах | приятный[1] | ||
| Плотность | 0,98 г / см3 | ||
| Температура плавления | -100 ° С (-148 ° F, 173 К) | ||
| Точка кипения | 32 ° С (90 ° F, 305 К) | ||
| 30% (20 ° С)[1] | |||
| Давление газа | 634 гПа (476 мм рт. Ст.) (20 ° C)[1] | ||
| -32.0·10−6 см3/ моль | |||
| Опасности | |||
| Паспорт безопасности | Оксфордский паспорт безопасности материалов | ||
Классификация ЕС (DSD) (устарело) | Легковоспламеняющийся (F +); Вредно (Xn) | ||
| точка возгорания | −19 ° С; −2 ° F; 254 К [1] | ||
| Пределы взрываемости | 4.5%-23%[1] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 1622 мг / кг (перорально, кролик)[2] | ||
LCLo (самый низкий опубликованный ) | 50 000 частей на миллион (морская свинка, 20 мин)[2] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 100 частей на миллион (250 мг / м3)[1] | ||
REL (Рекомендуемые) | TWA 100 частей на миллион (250 мг / м3) ST 150 частей на миллион (375 мг / м3)[1] | ||
IDLH (Непосредственная опасность) | 4500 частей на миллион[1] | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
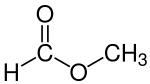
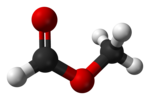
Метилформиат, также называемый метилметаноат, это метил сложный эфир из муравьиная кислота. Самый простой пример сложного эфира, это бесцветная жидкость с эфирным запахом, сильным запахом. давление газа, и низкий поверхностное натяжение. Это предшественник многих других соединений, представляющих коммерческий интерес.[3]
Производство
В лаборатории метилформиат может производиться реакция конденсации из метанол и муравьиная кислота, следующее:
- HCOOH + CH3OH → HCO2CH3 + H2О
Однако промышленный метилформиат обычно получают путем сочетания метанол и монооксид углерода (карбонилирование ) при наличии сильного основания, например метоксид натрия:[3]
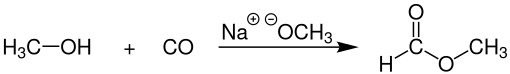
Этот процесс, коммерчески применяемый BASF среди других компаний, дает 96% селективность по метилформиату. В катализатор поскольку этот процесс чувствителен к воде, которая может присутствовать в монооксид углерода сырье, которое обычно получают из синтез-газ. Очень сухой монооксид углерода поэтому очень важно.[4]
Использует
Метилформиат используется в основном для производства формамид, диметилформамид, и муравьиная кислота. Эти соединения являются предшественниками или строительными блоками для многих полезных производных.
Из-за высокого давление газа, используется для быстросохнущего покрытия и как пенообразователь для некоторых применений пенополиуретана и в качестве замены ХФУ, ГХФУ, и ГФУ. Метилформиат не имеет озоноразрушающая способность и ноль потенциал глобального потепления[нужна цитата ]. Он также используется как инсектицид.
Исторически сложившееся использование метилформиата, которое иногда привлекает внимание, было в охлаждении. До появления менее токсичных хладагентов метилформиат использовался в качестве альтернативы диоксиду серы в бытовых холодильниках, например, в некоторых моделях знаменитого GE Monitor Top.
Рекомендации
- ^ а б c d е ж грамм час Карманный справочник NIOSH по химической опасности. "#0417". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Метилформиат». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б Вернер Ройтеманн и Хайнц Кечка «Муравьиная кислота» в Энциклопедия промышленной химии Ульмана 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a12_013
- ^ W. Couteau, J. Ramioulle, Патент США US4216339