Археол - Archaeol
Археол является одним из основных липидов мембран археи, одна из трех сфер жизни. Одна из ключевых особенностей, которая отличает архей от бактерии и эукария это их мембранные липиды, в которых важную роль играют археолы. Из-за этого археол также широко используется в качестве биомаркера древних архей, особенно метаногены, Мероприятия.[1]
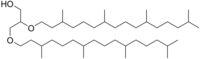
Археол обычно состоит из соединения двух фитаниловых цепей с sn-2 и sn-3 положениями глицерин молекула. Предполагается, что сильно разветвленные боковые цепи объясняют очень низкую проницаемость мембраны на основе археол, которая может быть одной из ключевых адаптаций архей к экстремальным условиям окружающей среды.
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2,3-Бис (3,7,11,15-тетраметилгексадекокси) пропан-1-ол | |
| Другие имена Липид археол; 2,3-Ди-О-фитанил-sn-глицерин; 2,3-Бис [(3,7,11,15-тетраметилгексадецил) окси] -1-пропанол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| MeSH | археол + липид |
PubChem CID | |
| |
| Характеристики | |
| C43ЧАС88О3 | |
| Молярная масса | 653.174 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Химия
Археол - это диэфирный липид, обычно встречающийся в архее. Стандартный археол - это 2,3-ди-O-фитанил-sn-глицерин, с двумя фитаниловые цепи связывание с положением sn-2 и sn-3 глицерина посредством эфир облигации. Структура 2,3-sn-глицерина и эфирная связь - два ключевых отличия липидов архей от липидов бактерии и эукария которые используют 1,2-sn-глицерин и в основном сложноэфирные связи.[2] Природный археол имеет конфигурации 3R, 7R, 11R для трех хиральные центры в изопреноид цепи. Существует четыре структурных варианта, которые усложняют мембранные липиды в функции и свойствах. Две фитанильные цепи могут образовывать 36-членное кольцо, давая макроциклический археол. Гидроксилированный археол имеет фитанильные цепи, гидроксилированные вначале. третичный углерод атом, в то время как сестертерерпаниловый археол имеет боковые цепи фитанила с сестертерерпанильными цепями C25, замещая на C2 глицерина или на обоих атомах углерода. Также обнаружен ненасыщенный археол с таким же углеродным скелетом, что и стандартный археол, но с одной или несколькими двойными связями в боковых цепях фитанила.[3]
Две молекулы археол могут быть связаны друг с другом с образованием кальдархеол (один типичный тетраэфир диалкилглицерина глицерина, GDGT), один из наиболее распространенных тетраэфирных липидов у архей.





Биологическая роль и синтез
Биологическая роль
Археол был обнаружен во всех проанализированных архее, по крайней мере, в следовых количествах. Он представляет собой 100% липидов диэфирного ядра в большинстве нейтрофильныйгалофилы[3] и серозависимые термофилы (хотя их основные липиды - это тетраэфирные липиды). Метаногены содержат гидроксиархеол и макроциклические соединения, отличные от стандартных археол, а археол, содержащий сестертерпаниловую цепь, характерен для алкалифильных крайних галофилов. Примечательно, что тетраэфирные липиды также широко представлены у архей.[2]
Липосомы (сферическая везикула, имеющая по крайней мере один липидный бислой) липидов из архей, как правило, демонстрирует чрезвычайно низкий проницаемость для молекул и ионов, включая протоны. Ионная проницаемость, вызванная ионофоры (переносчиков ионов через мембраны) также довольно низки и сопоставимы только с яичным фосфатидилхолин (очень распространенный компонент биологических мембран) при 37˚C, когда температура поднимается до примерно c.a. 70˚C.[4][5] В сравнении с бактерии и эукария, то изопреноид боковые цепи археола сильно разветвлены. Считается, что это структурное различие снижает проницаемость архей во всем диапазоне температур роста, что позволяет архей адаптироваться к экстремальным условиям окружающей среды.[6]
Процесс синтеза
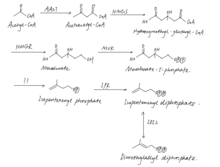
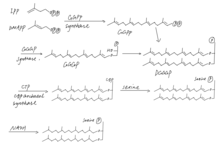
Археол обычно находится в виде фосфолипида в клетках архей. Синтетический путь полностью насыщенного археолфосфолипида протекает следующим образом: синтез изопреноидных боковых цепей за счет связи изопренов голова-хвост, эфирная связь с глицерин-1-фосфатным остовом, образование археола ЦДФ, присоединение полярной головной группы и насыщение двойной облигации. После этого, тетраэфирные липиды могут быть синтезированы впоследствии реакцией димеризации через связь голова к голове.[7]
У архей разные пути биосинтеза изопреноидных цепей по сравнению с бактериями и эукариями. Предшественниками изопреноида являются единицы С5. изопентенилпирофосфат (IPP) и диметилаллил пирофосфат (DMAPP), которые универсальны для всех трех сфер жизни. Как правило, два соединения синтезируются в бактериях через 2-C-метил-D-эритритол 4-фосфат / 1-дезокси-D-ксилулозо-5-фосфатный путь (путь MEP / DOXP) и синтезируются через путь мевалоната (MVA). в большинстве эукарий. Синтез IPP и DMAPP в архее происходит по альтернативному пути MVA, который отличается от классического пути MVA на последних трех этапах и разделяет остальные четыре этапа.[7]
Эфирные липиды в бактериях
Хотя археол, обладающий эфирной связью между изопреноидной цепью и глицерином, считается убедительным биомаркером архей, липиды эфирных мембран также были обнаружены в некоторых из них. аэробный и анаэробный бактерии, включая липиды с одной сложноэфирной связью и одной простой эфирной связью с алкильными цепями. Многие строго аноксические бактерии и несколько аэробных видов содержат плазмалогены (Pla), у которых есть алкильная цепь, связанная с sn-1 положением глицерина через винилэфирная связь. Считается, что, как и археи, эти липиды увеличивают устойчивость бактерий к неблагоприятным условиям окружающей среды. Более поразительным является открытие неизопреноидных диэфирных липидов диалкилглицерина (DGD) и разветвленных диалкилглицеринтетраэфирных липидов (brGDGT), которые образуются аналогично археолу путем связывания алкильных цепей (но не изопреноидных цепей) с молекулами глицерина через эфир связь. Примечательно, что эти липиды отличаются от липидов эфиров архей только боковыми цепями и позициями связывания на глицерине. Сообщается о DGD у термофильных бактерий, у некоторых мезофильный бактерии и агрегации миксобактерии.[8][9]
Используется как липидный биомаркер
Археол в отложениях обычно возникает в результате гидролиза фосфолипидов мембран архей во время диагенеза. Из-за его высокого потенциала сохранения он часто обнаруживается и используется геохимиками-органиками в качестве биомаркера активности архей, особенно биомассы и активности метаногена. В качестве заместителя метаногена он используется Michinari Sunamura et al. для прямого измерения метаногенов в отложениях Токийский залив,[10] а также использовалась Кэти Л. Х. Лим и соавт. как индикатор метаногенез в водонасыщенных почвах.[11] C. A. McCartney et al. использовали его как прокси для производства метана у крупного рогатого скота.[12]
Между тем, он также используется для понимания древней биогеохимии. Ричард Д. Панкост и соавт. Использовали его в качестве биомаркера. чтобы реконструировать Голоцен биогеохимия в омбротрофный торфяники.[13] Пилотное исследование под руководством Яна Д. Булла и соавт. также использовали археол в качестве биомаркера, чтобы выявить различия между ферментирующими пищеварительными системами в передняя кишка и задняя кишка древних травоядный млекопитающие.[14]
Кроме того, из-за разной кинетики деградации интактных археол и кальдархеол, отношение археол к кальдархеолу было предложено как соленость прокси в высокогорных озерах, обеспечивая инструмент для изучения палеозолености.[15]
В некоторых случаях археол также может гидролизоваться, при этом его боковые цепи сохраняются в виде фитан или же пристань в зависимости от окислительно-восстановительных условий.[16]
Измерение
Чтобы проанализировать археол, липиды обычно извлекаются с помощью традиционной процедуры Блая-Дайера,[17] обычно с последующим фракционированием (тонкослойной или колоночной хроматографией) и дериватизация. Казухиро Демизу и др.[18]и Садами Оцубо и др.[19] предложил аналогичные процессы, включающие кислотную экстракцию Блая и Дайера, кислотную обработку и дериватизацию, при этом основные липиды, наконец, подвергаются хроматография.
Для определения концентрации археола, присутствующего в образце, обычно используются хроматографические технологии, в том числе высокоэффективная жидкостная хроматография (ВЭЖХ),[18][19][20] газовая хроматография (GC),[21] и сверхкритическая жидкостная хроматография (SFC),[22][23] с масс-спектрометрии (MS) часто применяется для облегчения идентификации.
Смотрите также
Рекомендации
- ^ Отредактированный Рикардо Кавиккиоли (2007), Археи, Вашингтон, округ Колумбия: ASM Press, ISBN 978-1-55581-391-8, OCLC 172964654CS1 maint: дополнительный текст: список авторов (связь)
- ^ а б Кога, Й. Нишихара, М. Мори, Х. Акагава-Мацусита, М. (1993). «Эфирные полярные липиды метаногенных бактерий: строение, сравнительные аспекты, биосинтез». Микробиологические обзоры. 57 (1): 164–82. Дои:10.1128 / MMBR.57.1.164-182.1993. OCLC 680443863. ЧВК 372904. PMID 8464404.CS1 maint: несколько имен: список авторов (связь)
- ^ а б Gambacorta, A .; Gliozzi, A .; Де Роса, М. (1995). «Архейские липиды и их биотехнологическое применение». Всемирный журнал микробиологии и биотехнологии. 11 (1): 115–131. Дои:10.1007 / BF00339140. PMID 24414415.
- ^ Ямаути, Киёси; Дои, Куниюки; Киношита, Масаёши; Кии, Фумико; Фукуда, Хидеки (октябрь 1992 г.). «Архебактериальные липидные модели: мембраны с высокой солеустойчивостью из 1,2-дифитанилглицеро-3-фосфохолина». Biochimica et Biophysica Acta (BBA) - Биомембраны. 1110 (2): 171–177. Дои:10.1016 / 0005-2736 (92) 90355-п. ISSN 0005-2736. PMID 1390846.
- ^ Ямаути, Киёси; Дои, Кумиюки; Ёсида, Ёичи; Киношита, Масаёши (март 1993 г.). «Архебактериальные липиды: мембраны с высокой проницаемостью для протонов из 1,2-дифитанил-sn-глицеро-3-фосфолина». Biochimica et Biophysica Acta (BBA) - Биомембраны. 1146 (2): 178–182. Дои:10.1016/0005-2736(93)90353-2. ISSN 0005-2736. PMID 8383997.
- ^ Кога, Йосуке (2012). «Термическая адаптация липидных мембран архей и бактерий». Археи. 2012: 789652. Дои:10.1155/2012/789652. ISSN 1472-3646. ЧВК 3426160. PMID 22927779.
- ^ а б Джайн, Самта (2014). «Биосинтез эфирных липидов мембран архей». Границы микробиологии. 5: 641. Дои:10.3389 / fmicb.2014.00641. ЧВК 4244643. PMID 25505460.
- ^ Гросси, Винсент; Моллекс, Дэмиен; Винсон-Ложье, Арно; Хакиль, Флоренция; Пактон, Мюриэль; Краво-Лаюро, Кристиана (2015). "Липиды моно- и диалкилглицеринового эфира в анаэробных бактериях: биосинтетические выводы из мезофильного сульфатредуктора Desulfatibacillum alkenivorans PF2803T". Прикладная и экологическая микробиология. 81 (9): 3157–3168. Дои:10.1128 / AEM.03794-14. ЧВК 4393425. PMID 25724965.
- ^ Лоренцен, Вольфрам; Арендт, Тилман; Божююк, Кенан А. Дж .; Боде, Хельге Б. (11.05.2014). «Многофункциональный фермент участвует в биосинтезе липидов простого эфира бактерий». Природа Химическая Биология. 10 (6): 425–427. Дои:10.1038 / nchembio.1526. ISSN 1552-4450. PMID 24814673.
- ^ Сунамура, Мичинари; Кога, Йосуке; Охвада, Коити (1999-11-01). «Измерение биомассы метаногенов в отложениях Токийского залива с использованием липидов архей». Морская биотехнология. 1 (6): 562–568. Дои:10.1007 / PL00011811. ISSN 1436-2228. PMID 10612681.
- ^ Лим, Кэти Л. Х .; Панкост, Ричард Д .; Хорнибрук, Эдвард Р. К .; Максфилд, Питер Дж .; Эвершед, Ричард П. (2012). «Археол: индикатор метаногенеза в водонасыщенных почвах». Археи. 2012: 896727. Дои:10.1155/2012/896727. ISSN 1472-3646. ЧВК 3512251. PMID 23226972.
- ^ Dewhurst, R.J .; Ян, Т .; Bull, I. D .; Маккартни, К. А. (01.02.2013). «Оценка археола как молекулярного заместителя для производства метана у крупного рогатого скота». Журнал молочной науки. 96 (2): 1211–1217. Дои:10.3168 / jds.2012-6042. ISSN 0022-0302. PMID 23261373.
- ^ Панкост, Ричард Д .; McClymont, Erin L .; Bingham, Elizabeth M .; Робертс, Зои; Чарман, Дэн Дж .; Хорнибрук, Эдвард Р.К .; Бланделл, Энтони; Чемберс, Фрэнк М .; Лим, Кэти Л.Х. (ноябрь 2011 г.). «Археол как биомаркер метаногена в омбротрофных болотах». Органическая геохимия. 42 (10): 1279–1287. Дои:10.1016 / j.orggeochem.2011.07.003.
- ^ Гилл, Фиона Л .; Дьюхерст, Ричард Дж .; Dungait, Jennifer A.J .; Эвершед, Ричард П .; Айвз, Люк; Ли, Ченг-Сен; Панкост, Ричард Д .; Салливан, Мартин; Бера, Субир (май 2010 г.). «Археол - биомаркер ферментации передней кишки у современных и древних травоядных млекопитающих?». Органическая геохимия. 41 (5): 467–472. Дои:10.1016 / j.orggeochem.2010.02.001.
- ^ Ван, Хуанье; Лю, Вэйго; Zhang, Chuanlun L .; Цзян, Хунчэн; Донг, Хайлянь; Лу, Хунсюань; Ван, Цзиньсян (январь 2013 г.). «Оценка отношения археола к кальдархеолу в качестве показателя солености в высокогорных озерах на северо-востоке Цинхай-Тибетского плато». Органическая геохимия. 54: 69–77. Дои:10.1016 / j.orggeochem.2012.09.011.
- ^ Роуленд, С.Дж. (Январь 1990 г.). «Производство ациклических изопреноидных углеводородов путем лабораторного созревания метаногенных бактерий». Органическая геохимия. 15 (1): 9–16. Дои:10.1016 / 0146-6380 (90) 90181-х. ISSN 0146-6380.
- ^ Bligh, E. G .; Дайер, В. Дж. (Август 1959 г.). «Быстрый метод экстракции и очистки общих липидов». Канадский журнал биохимии и физиологии. 37 (8): 911–917. Дои:10.1139 / o59-099. ISSN 0576-5544. PMID 13671378. S2CID 7311923.
- ^ а б Демизу, Казухиро; Оцубо, Садами; Коно, Шухей; Миура, Исао; Нишихара, Масатеру; Кога, Йосуке (1992). «Количественное определение метаногенных клеток на основе анализа глицеролипидов, связанных простым эфиром, методом высокоэффективной жидкостной хроматографии». Журнал ферментации и биоинженерии. 73 (2): 135–139. Дои:10.1016 / 0922-338x (92) 90553-7. ISSN 0922-338X.
- ^ а б Оцубо, С. (май 1993 г.). «Чувствительный метод количественного определения уксусных метаногенов и оценки общего количества метаногенных клеток в естественной среде на основе анализа глицеролипидов, связанных эфиром». FEMS Microbiology Ecology. 12 (1): 39–50. Дои:10.1016 / 0168-6496 (93) 90023-з. ISSN 0168-6496.
- ^ Марц, Роберт Ф .; Себахер, Даниэль I .; Уайт, Дэвид К. (февраль 1983 г.). «Измерение биомассы метанобразующих бактерий в пробах окружающей среды». Журнал микробиологических методов. 1 (1): 53–61. Дои:10.1016/0167-7012(83)90007-6. ISSN 0167-7012. PMID 11540801.
- ^ Smith, G.C .; Фладгейт, Г.Д. (октябрь 1992 г.). «Химический метод оценки метаногенной биомассы». Исследования континентального шельфа. 12 (10): 1187–1196. Bibcode:1992CSR .... 12.1187S. Дои:10.1016 / 0278-4343 (92) 90078-х. ISSN 0278-4343.
- ^ Holzer, Gunther U .; Келли, Патрик Дж .; Джонс, Уильям Дж. (Июль 1988 г.). «Анализ липидов из метаногена гидротермального источника и связанного с ним осадка с помощью сверхкритической жидкостной хроматографии». Журнал микробиологических методов. 8 (3): 161–173. Дои:10.1016/0167-7012(88)90017-6. ISSN 0167-7012.
- ^ Кинг, Джерри (2002-01-22), "Технология сверхкритических жидкостей для экстракции, фракционирования и реакций липидов", Липидная биотехнология, CRC Press, Дои:10.1201 / 9780203908198.ch34, ISBN 9780824706197
