Нарколепсия - Narcolepsy
| Нарколепсия | |
|---|---|
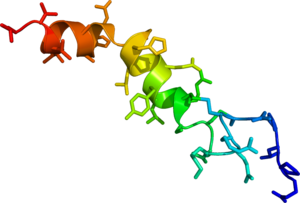 | |
| Концентрация орексин-А нейропептиды в спинномозговая жидкость у нарколептиков обычно очень низкий | |
| Произношение | |
| Специальность | Снотворное, неврология |
| Симптомы | Повышенная дневная сонливость, непроизвольные эпизоды сна, внезапная потеря мышечной силы, галлюцинации[1] |
| Осложнения | Столкновения автомобилей, падает[1] |
| Обычное начало | Детство[1] |
| Продолжительность | Долгосрочный[1] |
| Причины | Неизвестный[1] |
| Факторы риска | Семейный анамнез, травма головного мозга[1] |
| Диагностический метод | На основании симптомов и исследования сна[1] |
| Дифференциальная диагностика | Апноэ во сне, сильное депрессивное расстройство, анемия, сердечная недостаточность, пить алкоголь, не высыпается[1] |
| Уход | Регулярный короткий сон, гигиена сна[1] |
| Медикамент | Модафинил, оксибат натрия, стимуляторы, антидепрессанты[1] |
| Частота | От 0,2 до 600 на 100 000[2] |
Нарколепсия это долгосрочный неврологическое расстройство что включает в себя снижение способности регулировать циклы сна-бодрствования.[1] Симптомы часто включают периоды: повышенная дневная сонливость и кратковременные эпизоды непроизвольного сна.[1] Около 70% пострадавших также испытывают эпизоды внезапной потери мышечной силы, известные как катаплексия.[1] Эти переживания могут быть вызваны сильными эмоциями.[1] Реже могут быть яркие галлюцинации или невозможность двигаться (сонный паралич ) во время засыпания или пробуждения.[1] Люди с нарколепсией склонны спать примерно такое же количество часов в день, как и у людей без сна, но качество сна имеет тенденцию к снижению.[1]
Точная причина нарколепсии неизвестна, возможно, несколько причин.[1][3] До 10% случаев имеется семейный анамнез заболевания.[1] Часто у пострадавших низкий уровень нейропептид орексин, что может быть связано с аутоиммунное заболевание.[1] В редких случаях нарколепсия может быть вызвана черепно-мозговой травмой, опухолями или другими заболеваниями, поражающими части мозга, которые регулируют бодрствование или Быстрый сон.[1] Диагноз обычно основывается на симптомах и исследования сна, после исключения других возможных причин.[1] Чрезмерная дневная сонливость также может быть вызвана другими причинами. нарушения сна Такие как апноэ во сне, сильное депрессивное расстройство, анемия, сердечная недостаточность, пить алкоголь и не высыпается.[1] Катаплексию можно принять за припадки.[1]
Хотя нет лекарства, некоторые изменения образа жизни и лекарства могут помочь.[1] Изменения в образе жизни включают регулярный короткий сон и гигиена сна.[1] Используемые лекарства включают: модафинил, оксибат натрия и метилфенидат.[1] Несмотря на первоначальную эффективность, толерантность к преимуществам со временем может развиться.[1] Трициклические антидепрессанты и селективные ингибиторы обратного захвата серотонина (СИОЗС) могут улучшить катаплексию.[1]
Оценки частоты колеблются от 0,2 до 600 на 100 000 человек в разных странах.[2] Заболевание часто начинается в детстве, когда мужчины и женщины страдают одинаково.[1] Нелеченная нарколепсия увеличивает риск столкновения автомобилей и падает.[1]
Признаки и симптомы
Есть две основные характеристики нарколепсии: повышенная дневная сонливость и ненормальный Быстрый сон.[4] Чрезмерная дневная сонливость возникает даже после полноценного ночного сна. Человек с нарколепсией, вероятно, станет сонливым или засыпает, часто в неподходящее или нежелательное время и в неподходящем месте, или просто очень устал в течение дня. Нарколептики могут быть не в состоянии испытать объем восстанавливающего глубокого сна, который испытывают здоровые люди, из-за ненормальной регуляции REM - они не «слишком спят». У нарколептиков обычно более высокая плотность быстрого сна, чем у ненарколептиков, но у них также наблюдается больше фаз быстрого сна без атонии.[5] У многих нарколептиков достаточно фазы быстрого сна, но они не чувствуют себя отдохнувшими или бодрыми в течение дня.[6] Может показаться, что всю жизнь они проживают в состоянии постоянного недосыпания.[требуется медицинская цитата ]
Чрезмерная сонливость может различаться по степени выраженности и чаще всего проявляется в монотонных ситуациях, не требующих особого взаимодействия.[6] Дневной сон может происходить без особого предупреждения и может быть физически непреодолимым. Этот сон может происходить несколько раз в день. Обычно они освежают, но только на несколько часов или меньше. Яркие сны можно видеть регулярно, даже во время очень короткого сна. Сонливость может сохраняться длительное время или оставаться постоянной. Кроме того, ночной сон может быть фрагментированным, с частыми пробуждениями. Второй заметный симптом нарколепсии - это ненормальный быстрый сон. Нарколептики уникальны тем, что они входят в фазу быстрого сна в начале сна, даже когда спите днем.[4]
Классические симптомы расстройства, часто называемого «тетрадой нарколепсии», включают: катаплексия, сонный паралич, гипнагогические галлюцинации и чрезмерная дневная сонливость.[7] Другие симптомы могут включать автоматическое поведение и бодрствование в ночное время.[4][8][9] Эти симптомы могут возникать не у всех людей с нарколепсией.
- Катаплексия - это эпизодическая потеря мышечной функции, варьирующаяся от небольшой слабости, такой как вялость в шее или коленях, провисания лицевых мышц, слабости в коленях, часто называемой «искривлением колен»,[10] или неспособность четко говорить, вплоть до полного разрушения тела. Эпизоды могут быть вызваны внезапными эмоциональными реакциями, такими как: смех, злость, сюрприз или страх. Человек остается в сознании на протяжении всего эпизода. В некоторых случаях катаплексия может напоминать эпилептические припадки.[11] Обычно речь невнятная, и зрение ухудшается (двоение в глазах, неспособность сосредоточиться), но слух и осознание остаются в норме. Катаплексия также оказывает серьезное эмоциональное воздействие на нарколептиков, поскольку может вызывать крайнюю тревогу, страх и избегать людей или ситуаций, которые могут вызвать приступ. Катаплексия обычно считается уникальной для нарколепсии и аналогична сонному параличу в том, что обычно механизм защитного паралича, возникающий во время сна, неправильно активируется. Противоположность этой ситуации (неспособность активировать этот защитный паралич) происходит в расстройство поведения при быстром движении глаз.[требуется медицинская цитата ]
- Периоды бодрствования ночью[4]
- Сонный паралич - это временная неспособность говорить или двигаться при пробуждении (или, реже, при засыпании). Это может длиться от нескольких секунд до минут. Это часто пугает, но не опасно.[требуется медицинская цитата ]
- Гипнагогические галлюцинации - это яркие, часто пугающие, похожие на сновидения переживания, которые происходят во время дремоты или засыпания. Гипнопомпические галлюцинации относятся к тем же ощущениям при пробуждении ото сна. Эти галлюцинации могут проявляться в виде зрительных или слуховых ощущений.[4]
В большинстве случаев первым признаком нарколепсии является чрезмерная и подавляющая дневная сонливость. Другие симптомы могут проявляться сами по себе или в сочетании через несколько месяцев или лет после дневного сна. Существуют широкие вариации развития, тяжести и порядка появления катаплексии, сонного паралича и гипнагогических галлюцинаций у людей. Только от 20 до 25 процентов людей с нарколепсией испытывают все четыре симптома. Чрезмерная дневная сонливость обычно сохраняется на протяжении всей жизни, но сонный паралич и гипнагогические галлюцинации - нет.
Многие люди с нарколепсией также страдают бессонница в течение длительного периода времени. Чрезмерная дневная сонливость и катаплексия часто становятся достаточно серьезными, чтобы вызвать серьезные проблемы в социальной, личной и профессиональной жизни человека. Обычно, когда человек бодрствует, мозговые волны показать правильный ритм. Когда человек впервые засыпает, мозговые волны становятся медленнее и менее регулярными, что называется небыстрым движением глаз (NREM ) спать. Примерно через полтора часа медленного сна мозговые волны снова начинают проявлять более активный паттерн, называемый Быстрый сон (сон с быстрым движением глаз), когда больше всего вспоминают сновидение происходит. Связанная с наблюдаемыми на ЭЭГ волнами во время быстрого сна, мышечная атония называется REM атония.[требуется медицинская цитата ]
При нарколепсии нарушаются порядок и продолжительность периодов медленного и быстрого сна, причем быстрый сон наступает в начале сна, а не после периода медленного сна. Кроме того, некоторые аспекты быстрого сна, которые обычно возникают только во время сна, такие как отсутствие мышечного контроля, сонный паралич и яркие сны, иногда возникают у людей с нарколепсией. Например, отсутствие мышечного контроля может происходить во время бодрствования в эпизоде катаплексии; Говорят, что во время бодрствования наблюдается вторжение REM-атонии. Сонный паралич и яркие сны могут возникать при засыпании или пробуждении. Проще говоря, мозг не проходит через нормальные стадии дремоты и глубокого сна, а переходит непосредственно в фазу быстрого сна (и выходит из нее).[требуется медицинская цитата ]
Как следствие, ночной сон не включает в себя столько глубокого сна, поэтому мозг пытается «наверстать упущенное» в течение дня, отсюда и чрезмерная дневная сонливость. Люди с нарколепсией могут заметно засыпать в непредвиденные моменты (часто встречаются такие движения, как покачивание головой). Люди с нарколепсией быстро засыпают, как представляется, очень глубоким сном, они внезапно просыпаются и при этом могут быть дезориентированы (головокружение - обычное явление). У них очень яркие сны, которые они часто очень подробно вспоминают. Люди с нарколепсией могут видеть сны, даже если засыпают всего на несколько секунд. Известно, что наряду с яркими сновидениями у людей с нарколепсией перед сном возникают звуковые или визуальные галлюцинации.[требуется медицинская цитата ]
Нарколептики могут набрать лишний вес; дети могут набрать от 9 до 18 кг (от 20 до 40 фунтов), когда у них впервые разовьется нарколепсия; у взрослых индекс массы тела примерно на 15% выше среднего.[12][13]
Причины
Точная причина нарколепсии неизвестна, и она может быть вызвана несколькими различными факторами.[1][3] Механизм предполагает потерю орексин -освобождение нейронов внутри боковой гипоталамус (около 70 000 нейронов[14]).[15][16]
До 10% случаев имеется семейный анамнез заболевания. Семейный анамнез чаще встречается при нарколепсии с катаплексией.[1] Существует сильная связь с определенными генетическими вариантами.[15] В дополнение к генетическим факторам, низкие уровни пептидов орексина коррелировали с прошлой историей инфекции, диетой, контактом с токсинами, такими как пестициды, и травмами мозга из-за травм головы, опухолей мозга или инсультов.[4][15] Аутоиммунитет также может сыграть роль.[17]
Генетика
Первичный генетический фактор, который сильно повлиял на развитие нарколепсии, включает область хромосома 6 известный как человеческий лейкоцитарный антиген (HLA) комплекс.[15][18] Специфические вариации генов HLA сильно коррелируют с наличием нарколепсии;[15] однако эти вариации не требуются для возникновения состояния и иногда возникают у людей без нарколепсии.[15][19] Считается, что эти генетические вариации в комплексе HLA увеличивают риск аутоиммунный ответ на орексин - высвобождение нейронов в боковой гипоталамус.[15][16][19]
В аллель HLA-DQB1 * 06: 02 гена человека HLA-DQB1 был зарегистрирован более чем у 90% людей с нарколепсией, а аллели других HLA гены, такие как HLA-DQA1 * 01: 02, были связаны. Исследование 2009 г. обнаружило сильную связь с полиморфизмом в ПРОФ генный локус (dbSNP Идентификаторы rs1154155, rs12587781 и rs1263646).[14] В обзорной статье 2013 года сообщалось о дополнительных, но более слабых связях с локусами генов. TNFSF4 (rs7553711), Катепсин H (rs34593439) и P2RY11 -DNMT1 (rs2305795).[20]Другой локус гена, связанный с нарколепсией, - это EIF3G (rs3826784).[21]
Вакцина против гриппа H1N1
Связь между GlaxoSmithKline вакцина против гриппа H1N1 Pandemrix и нарколепсия была обнаружена как у детей, так и у взрослых.[22] Финляндия Национальный институт здоровья и социального обеспечения рекомендовал приостановить вакцинацию Pandemrix в ожидании дальнейшего расследования нарколепсии.[23][24]
Патофизиология
Потеря нейронов
Орексин, также известный как гипокретин, представляет собой нейропептид который действует в мозге, регулируя аппетит и бодрствование, а также ряд других когнитивных и физиологических процессов.[15][25][26] Потеря этих нейронов, продуцирующих орексин, вызывает нарколепсию, и у большинства людей с нарколепсией количество этих нейронов в мозгу сокращается.[15][16][19] Селективное разрушение нейронов HCRT / OX с сохранением ближайших структур предполагает высокоспецифичную аутоиммунную патофизиологию.[27] Цереброспинальная жидкость HCRT-1 / OX-A не определяется у 95% пациентов с нарколепсией 1 типа.[27]
Система, регулирующая сон, возбуждение и переходы между этими состояниями у человека, состоит из трех взаимосвязанных подсистем: орексин прогнозы из боковой гипоталамус, то ретикулярная активирующая система, а вентролатеральное преоптическое ядро.[16] У нарколептиков все эти системы связаны с нарушениями из-за значительного уменьшения количества нейронов проекции орексина в гипоталамусе и значительно меньшего количества нейропептидов орексина в организме. спинномозговая жидкость и нервной ткани по сравнению с людьми, не страдающими нарколепсией.[16] Люди с нарколепсией обычно испытывают REM стадия сна в течение пяти минут после засыпания, в то время как люди, не страдающие нарколепсией (если они не испытывают значительного недосыпания)[28] не испытывайте REM до тех пор, пока не пройдет период медленный сон, который длится около первого часа цикла сна.[1]
Нарушенные состояния сна
Нейронный контроль нормального состояния сна и связь с нарколепсией понятны лишь частично. У людей нарколептический сон характеризуется тенденцией резко переходить из состояния бодрствования в состояние Быстрый сон с небольшим вмешательством или без него медленный сон. Изменения в моторе и проприоцептивный системы во время быстрого сна изучались как на людях, так и на животных. Во время нормального быстрого сна, спинного мозга и ствола мозга альфа двигательный нейрон гиперполяризация производит почти полный атония из скелетные мышцы через тормозной нисходящий ретикулоспинальный путь. Ацетилхолин может быть одним из нейротрансмиттеры участвует в этом пути. При нарколепсии подавление рефлекса двигательной системы, наблюдаемое при катаплексия имеет особенности, обычно наблюдаемые только в нормальном фазе быстрого сна.[1]
Диагностика
Третье издание Международная классификация нарушений сна (ICSD-3) различает нарколепсию с катаплексией (тип 1) и нарколепсию без катаплексии (тип 2), в то время как пятое издание Диагностическое и Статистическое Руководство по Психическим Расстройствам (DSM-5) использует диагноз нарколепсии только для обозначения нарколепсии 1 типа. В DSM-5 нарколепсия без катаплексии называется нарушением гиперсонливости.[29] Самое последнее издание Международная классификация болезней МКБ-11 в настоящее время определяет три типа нарколепсии: нарколепсия 1-го типа, нарколепсия 2-го типа и неуточненная нарколепсия.[30]
Диагностические критерии ICSD-3 предполагают, что человек должен испытывать «ежедневные периоды неудержимой потребности во сне или дневные провалы в сне» для обоих подтипов нарколепсии.[29] Этот симптом должен длиться не менее трех месяцев. Для постановки диагноза нарколепсии 1 типа человек должен иметь либо катаплексию, либо задержка сна менее 8 минут и два или более периодов REM в начале сна (SOREMPs), либо они должны присутствовать при концентрации гипокретина-1 менее 110 пг / мл.[29] Диагноз нарколепсии 2 типа требует средней задержки сна менее 8 минут, двух или более SOREMP и концентрации гипокретина-1 более 110 пг / мл. Кроме того, результаты гиперсонливости и задержки сна нельзя лучше объяснить другими причинами.[29]
Критерии нарколепсии DSM-5 требуют, чтобы человек демонстрировал повторяющиеся периоды «неудержимой потребности во сне, засыпании или дремоте» по крайней мере три раза в неделю в течение трех месяцев.[29] У человека также должно быть одно из следующего: катаплексия, концентрация гипокретина-1 менее 110 пг / мл, латентность быстрого сна менее 15 минут или тест множественной задержки сна (MSLT) показывает задержку сна менее 8 минут и два или более SOREMP.[29] Для диагностики расстройство гиперсонливости, человек должен проявлять чрезмерную сонливость, несмотря на как минимум 7-часовой сон, а также либо периодические провалы в дневном сне, эпизоды невосстановительного сна продолжительностью 9 или более часов, либо трудности с бодрствованием после пробуждения. Кроме того, гиперсонливость должна происходить не реже трех раз в неделю в течение трех месяцев и должна сопровождаться значительным расстройством или ухудшением состояния. Это также нельзя объяснить другим нарушением сна, сопутствующими психическими или медицинскими расстройствами или лекарствами.[31]
Тесты
Диагностика относительно проста, когда присутствуют все симптомы нарколепсии, но если приступы сна изолированы, а катаплексия легкая или отсутствует, диагностика более трудна. Для диагностики нарколепсии обычно используются три теста: полисомнография (ПСГ), то тест множественной задержки сна (MSLT), а Шкала сонливости Эпворта (ESS). Эти тесты обычно проводятся специалист по сну.[нужна цитата ]
Полисомнография включает непрерывную регистрацию мозговых волн во время сна и ряда нервных и мышечных функций во время ночного сна. При тестировании люди с нарколепсией быстро засыпают, рано входят в фазу быстрого сна и часто могут просыпаться ночью. Полисомнограмма также помогает обнаружить другие возможные нарушения сна, которые могут вызвать дневную сонливость.[нужна цитата ]
Шкала сонливости Эпворта - это краткий опросник, который вводится для определения вероятности наличия нарушения сна, включая нарколепсию.[нужна цитата ]
Тест множественной задержки сна выполняется после того, как человек проходит исследование ночного сна. Человека просят поспать каждые 2 часа, и время, необходимое ему для этого, записывается. Большинство людей засыпают в течение 5-8 минут, а также быстрее проявляют фазу быстрого сна, чем люди, не страдающие нарколепсией.[32]
Измерение уровня орексина в организме человека спинномозговая жидкость отобраны в спинномозговая пункция может помочь в диагностике нарколепсии, при этом аномально низкие уровни служат индикатором расстройства.[33] Этот тест может быть полезен, когда результаты MSLT неубедительны или трудно интерпретировать.[34]
Уход
Людям с нарколепсией можно существенно помочь, но нельзя вылечить. Однако технология существует на ранней стадии, например, эксперименты по использованию препроорексин трансген посредством редактирования генов восстановил нормальную функцию в моделях мышей, заставив другие нейроны продуцировать орексин после того, как исходный набор был разрушен, или замена отсутствующих орексинергических нейронов трансплантацией гипокретиновых стволовых клеток - оба шага в этом направлении для эффективной постоянной фиксации биологии после применения у людей .[35][36] Кроме того, эффективные идеальные методы негенного редактирования и химические препараты включают методы лечения гипокретином, такие как будущие препараты, такие как агонисты гипокретина (такие как TAK-994). [37] который предприятие планирует сделать доступным к 2024 году, или замену гипокретина в виде гипокретин 1 данный внутривенный (вводится в вены), внутрицистернальный (прямая инъекция в мозг), и интраназальный (распыляется через нос), причем последний имеет низкую эффективность при небольшом количестве, используемом в текущих экспериментах, но может быть эффективным при очень высоких дозах в будущем.[38][39]
Могут быть полезны общие стратегии, такие как образование людей и семьи, соблюдение гигиены сна и соблюдение лекарств, а также обсуждение вопросов безопасности, например, водительские права. Также можно устранить возможные побочные эффекты лекарств.[6] Регулярное наблюдение полезно, чтобы иметь возможность отслеживать реакцию на лечение, оценивать наличие других нарушений сна, таких как обструктивное апноэ во сне, и обсуждать психосоциальные проблемы.[6]
Основное лечение чрезмерной дневной сонливости при нарколепсии - это Центральная нервная система стимуляторы Такие как метилфенидат, амфетамин, декстроамфетамин, модафинил, и армодафинил. В конце 2007 г. Министерство здравоохранения выпустило предупреждение о серьезных побочных реакциях кожи на модафинил. FDA.[40]
Несколько исследований также показали, что оксибат натрия эффективен при лечении катаплексии.[6]
Другой применяемый препарат - атомоксетин, не стимулирующее и ингибитор обратного захвата норэпинефрина (NRI), который не вызывает зависимости или рекреационных эффектов. Во многих случаях запланированный регулярный короткий сон может снизить потребность в фармакологическом лечении EDS, но только на короткое время улучшить симптомы. 120-минутный сон улучшил бдительность человека на 3 часа, тогда как 15-минутный сон не принес пользы.[41] Дневной сон не заменяет ночной сон. Постоянное общение между врачом, человеком и членами их семей важно для оптимального лечения нарколепсии.
Другой одобренный FDA вариант лечения нарколепсии - это оксибат натрия,[42] также известный как натрий гамма-гидроксибутират (GHB). Его можно использовать для катаплексия связаны с нарколепсией и повышенная дневная сонливость связанные с нарколепсией.[42][43][6][44]
Солриамфетол - новая молекула, показанная при нарколеспии 1 и 2 типа.[45]
Антидепрессанты
Нарколепсию иногда лечат селективные ингибиторы обратного захвата серотонина и трициклические антидепрессанты, Такие как кломипрамин, имипрамин, или же протриптилин, а также другие препараты, подавляющие быстрый сон.[46] Венлафаксин, антидепрессант, блокирующий обратный захват серотонина и норадреналина, показал свою полезность при лечении симптомов катаплексии,[47] однако он имеет заметные побочные эффекты, включая нарушение сна.[48] Класс антидепрессантов используется в основном для лечения катаплексии, у людей с нарколепсией без катаплексии они обычно не используются.[49]
Дети
Общие поведенческие методы лечения детской нарколепсии включают улучшение гигиены сна, запланированный дневной сон и физические упражнения.[50]
Многие лекарства используются для лечения взрослых и могут применяться для лечения детей. Эти лекарства включают стимуляторы центральной нервной системы, такие как метилфенидат, модафинил, амфетамин и декстроамфетамин.[51] Другие лекарства, такие как оксибат натрия[45] или же атомоксетин также может использоваться для противодействия сонливости. Лекарства, такие как оксибат натрия, венлафаксин, флуоксетин, и кломипрамин может быть назначен, если у ребенка катаплексия.[52]
Эпидемиология
Оценки частоты колеблются от 0,2 на 100 000 в Израиле до 600 на 100 000 в Японии.[2] Эти различия могут быть связаны с тем, как проводились исследования, или с самими популяциями.[2]
в Соединенные Штаты, по оценкам, нарколепсия поражает до 200 000 американцев, но диагностировано менее 50 000 человек. Распространенность нарколепсии составляет около 1 на 2 000 человек.[53] Нарколепсию часто принимают за депрессия, эпилепсия, то побочные эффекты лекарств, плохого сна или рекреационное употребление наркотиков, что делает вероятным ошибочный диагноз.[нужна цитата ] Хотя симптомы нарколепсии часто путают с депрессией, между этими двумя расстройствами существует связь. Исследования показали неоднозначные результаты о совместном возникновении депрессии у людей с нарколепсией, поскольку цифры, приведенные в различных исследованиях, составляют от 6% до 50%.[54]
Нарколепсия может возникать как у мужчин, так и у женщин в любом возрасте, хотя типичные симптомы появляются в юность и молодость. Диагностика нарколепсии у взрослых занимает около десяти лет.[13] Задокументированы когнитивные, образовательные, профессиональные и психосоциальные проблемы, связанные с чрезмерной дневной сонливостью при нарколепсии. Особенно разрушительно то, что это происходит в решающие подростковые годы, когда происходит образование, развитие самооценки и формирование профессионального выбора. Хотя когнитивные нарушения действительно возникают, они могут быть только отражением чрезмерной дневной сонливости.[55]
Общество и культура
В 2015 году сообщалось, что британцы Департамент здравоохранения платил за оксибат натрия лекарства стоимостью 12000 фунтов стерлингов в год для 80 человек, которые обращаются в суд по поводу проблем, связанных с использованием Pandemrix вакцина против свиного гриппа. Оксибат натрия недоступен для людей с нарколепсией через Национальный центр здоровья.[56]
Имя
Термин «нарколепсия» происходит от французского нарколепсия.[57] Французский термин впервые был использован в 1880 г. Жан-Батист-Эдуар Желино, кто использовал Греческий νάρκη (нарке), что означает «онемение», и λῆψις (лепсис), что означает «атака».[57]
Исследование
Лекарства, содержащие гистамин
Еще неизвестно, будет ли Антагонисты H3 (то есть такие соединения, как питолизант которые способствуют высвобождению стимулирующей бодрствование молекулы амина гистамина), будут особенно полезны в качестве агентов, способствующих бодрствованию.[58] Тем не менее, использование в настоящее время существует в различных странах, таких как Франция, Великобритания (NHS по состоянию на сентябрь 2016 г.[59][60][61][62]) после получения разрешения на продажу Европейской Комиссией по рекомендации Европейское агентство по лекарствам и в Соединенных Штатах с одобрения Управление по контролю за продуктами и лекарствами (FDA) по состоянию на август 2019 г.[63]
ГАМК-препараты
Учитывая возможную роль гиперактивных ГАМКА рецепторы первичной гиперсомнии (нарколепсия и идиопатическая гиперсомния), лекарства, которые могут противодействовать этой активности, изучаются, чтобы проверить их потенциал для улучшения сонливости. В настоящее время они включают кларитромицин и флумазенил.[64][65]
Флумазенил
Флумазенил - единственный ГАМКА антагонист рецептора представлен на рынке с января 2013 года, и в настоящее время он производится только в виде препарата для внутривенного введения. Учитывая его фармакологию, исследователи считают его многообещающим лекарством для лечения первичной гиперсомнии. Результаты небольшого двойного слепого рандомизированного контролируемого клинического исследования были опубликованы в ноябре 2012 года. Это исследование показало, что флумазенил приносит облегчение большинству людей, у которых в спинномозговой жидкости содержится неизвестный «сомноген», усиливающий функцию ГАМКА рецепторы, что делает их более восприимчивыми к сонливому эффекту ГАМК. Для одного человека ежедневный прием флумазенила в виде пастилок и кремов для местного применения доказал свою эффективность в течение нескольких лет.[64][66] Отчет 2014 года также показал улучшение симптомов первичной гиперсомнии после лечения непрерывной подкожной инфузией флумазенила.[67] Первоначально предполагалось, что предложение генерического флумазенила слишком мало для удовлетворения потенциального спроса на лечение первичной гиперсомнии.[68] Однако этот дефицит уменьшился, и сейчас десятки людей получают флумазенил не по назначению.[69]
Кларитромицин
В модели пробирки кларитромицин (антибиотик, одобренный FDA для лечения инфекций), как было обнаружено, возвращал функцию системы ГАМК в норму у людей с первичной гиперсомнией. Поэтому исследователи лечили несколько человек с нарколепсией неконтролируемым кларитромицином, и большинство из них почувствовали, что их симптомы улучшились после этого лечения. Чтобы определить, действительно ли кларитромицин полезен для лечения нарколепсии и идиопатической гиперсомнии, в 2012 году было завершено небольшое двойное слепое рандомизированное контролируемое клиническое исследование.[65] «В этом пилотном исследовании кларитромицин улучшил субъективную сонливость при гиперсомнии, связанной с ГАМК. Необходимы более масштабные и более длительные испытания».[70] В 2013 году ретроспективный обзор, посвященный оценке длительного использования кларитромицина, показал его эффективность у большого процента людей с гиперсомнией, связанной с ГАМК.[71] «Важно отметить, что положительный эффект кларитромицина является вторичным по отношению к эффекту антагониста бензодиазепина, а не к его антибиотическим эффектам, и лечение необходимо продолжать».[58]
Агонисты рецепторов орексина
Орексин-А (a.k.a. hypocretin-1), как было показано на животных моделях, сильно способствует пробуждению, но, к сожалению, он не проникает через гематоэнцефалический барьер. Поэтому компании разработали рецептор орексина антагонисты, как суворексант, для лечения бессонницы. Также вероятно, что рецептор орексина-А агонист будут найдены и разработаны для лечения гиперсомнии.[58]
В августе 2015 года Нагахара и др. Опубликовали свою работу по синтезу первого агониста HCRT / OX2R, соединения 26, с хорошей эффективностью и селективностью.[27]
L-карнитин
Аномально низкие уровни ацилкарнитин наблюдались у людей с нарколепсией.[72] Эти же низкие уровни были связаны с первичной гиперсомнией в целом в исследованиях на мышах. «Мыши с системным дефицитом карнитина демонстрируют более высокую частоту фрагментированного бодрствования и сна с быстрым движением глаз (REM), а также сниженную двигательную активность». Администрация ацетил-L-карнитин было показано, что эти симптомы улучшаются у мышей.[73] Последующее испытание на людях показало, что люди с нарколепсией, получавшие L-карнитин, проводили меньше времени в дневном сне, чем люди, которым давали плацебо.[74]
Модели животных
Исследования на животных пытаются имитировать заболевание у людей либо путем модификации рецепторов гипокретина / орексина, либо путем удаления этого пептида.[75] Дефицит орексина, вызванный дегенерацией нейронов гипоталамуса, считается одной из причин нарколепсии.[76] Более поздние клинические исследования как на животных, так и на людях также показали, что гипокретин участвует в других функциях, помимо регуляции бодрствования и сна. Эти функции включают вегетативную регуляцию, эмоциональную обработку, поощрение обучаемого поведения или энергетический гомеостаз. В исследованиях, где концентрация гипокретина измерялась при различных обстоятельствах, было замечено, что уровни гипокретина повышались при положительной эмоции, гневе или социальном взаимодействии, но оставались низкими во время сна или во время переживания боли.[77]
Наиболее надежными и достоверными разработанными моделями на животных являются модели собак (нарколептические собаки) и грызунов (мыши с дефицитом орексина), которые помогли исследовать нарколепсию и сосредоточили внимание на роли орексина в этом заболевании.[76]
Модели собак
Собаки, а также другие виды животных, такие как кошки или лошади, также могут проявлять спонтанную нарколепсию с симптомами, аналогичными той, которая наблюдается у людей. Приступы катаплексии у собак могут включать частичный или полный коллапс.[76] Нарколепсия с катаплексией была выявлена у нескольких пород, таких как лабрадор-ретривер или доберман-пинчер, где исследовалась возможность наследования этого заболевания в аутосомно-рецессивном режиме.[78] В соответствии с [75] Надежной собачьей моделью нарколепсии будет та, в которой нарколептические симптомы являются результатом мутации в гене HCRT 2. Пораженные животные проявляли чрезмерную дневную сонливость с пониженным состоянием бдительности и тяжелой катаплексией, возникшей после вкусной еды и взаимодействия с владельцы или с другими животными.[75]
Модели грызунов
Мыши, генетически сконструированные так, чтобы не иметь генов орексина, демонстрируют много общего с нарколепсией человека. В ночные часы, когда обычно находятся мыши, мыши, лишенные орексина, демонстрировали мышиный катаплексия и электрическая активность мозга и мышц, аналогичная активности во время быстрого и медленного сна. Эта катаплексия может быть вызвана социальным взаимодействием, бегом на колесах и ультразвуковой вокализацией. После пробуждения мыши также демонстрируют поведение, соответствующее чрезмерной дневной сонливости.[76]
Модели на мышах также использовались для проверки того, является ли недостаток орексина нейроны коррелирует с нарколепсией. У мышей, у которых были удалены орексиновые нейроны, наблюдалась фрагментация сна, SOREMP и ожирение.[76]
Модели на крысах использовались для демонстрации связи между дефицитом орексина и нарколептическими симптомами. Крысы, потерявшие большую часть своих орексинергических нейронов, демонстрировали несколько SOREMP, а также меньшую бодрствование в течение ночных часов, укороченную латентность REM и короткие периоды катаплексии.[76]
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах "Изложение фактов о нарколепсии". NINDS. Публикация NIH № 03-1637. В архиве из оригинала 27 июля 2016 г.. Получено 19 августа 2016.
- ^ а б c d Госвами М., Торпи М.Дж., Панди-Перумал С.Р. (2016). Нарколепсия: клиническое руководство (2-е изд.). Springer. п. 39. ISBN 9783319237398. В архиве из оригинала от 23 августа 2016 г.. Получено 19 августа 2016.
- ^ а б "Информационная страница о нарколепсии". NINDS. Архивировано из оригинал 7 января 2017 г.. Получено 7 января 2017.
- ^ а б c d е ж Зеленый S (2011). Биологические ритмы, сон и гипноз. Basingstoke, Хэмпшир, Англия: Пэлгрейв Макмиллан. ISBN 9780230252653.
- ^ Довилье, Ив; Ромпре, Сильви; Ганьон, Жан-Франсуа; Вендетт, Мелани; Пети, Доминик; Монплезир, Жак (1 июля 2007 г.). «Характеристики быстрого сна при нарколепсии и расстройстве поведения во сне». Спать. 30 (7): 844–849. Дои:10.1093 / сон / 30.7.844. ISSN 0161-8105. ЧВК 1978363. PMID 17682654.
- ^ а б c d е ж Мудрый М.С., Аранд Д.Л., Оже Р.Р., Брукс С.Н., Уотсон Н.Ф. (декабрь 2007 г.). «Лечение нарколепсии и других гиперсомний центрального происхождения». Спать. 30 (12): 1712–27. Дои:10.1093 / сон / 30.12.1712. ЧВК 2276130. PMID 18246981.
- ^ Кандел Э. Р., Шварц Дж. Х., Джессел Т. М., ред. (2000). Принципы нейронологии (4-е изд.). Макгроу-Хилл. п.949. ISBN 978-0-8385-7701-1.
- ^ Cunha JP. Шил WC младший (ред.). «Нарколепсия». MedicineNet. В архиве из оригинала 24 марта 2016 г.. Получено 15 марта 2016.
- ^ Зорик Ф.Дж., Салис П.Дж., Рот Т., Крамер М. (апрель 1979 г.). «Нарколепсия и автоматическое поведение: история болезни». Журнал клинической психиатрии. 40 (4): 194–7. PMID 422531.
- ^ «О нарколепсии». Стэнфордский центр нарколепсии. В архиве из оригинала 18 марта 2016 г.. Получено 15 января 2016.
- ^ Данхэм СК (2010). «Нарколепсия в виде псевдосудорожных припадков». Помощник по первичной медико-санитарной помощи журнала клинической психиатрии. 12 (2). Дои:10.4088 / PCC.09l00793whi. ЧВК 2910991. PMID 20694129.
- ^ Скаммелл TE (декабрь 2015 г.). «Нарколепсия». Медицинский журнал Новой Англии. 373 (27): 2654–62. Дои:10.1056 / NEJMra1500587. PMID 26716917.
- ^ а б Невсималова С (август 2014). «Диагностика и лечение детской нарколепсии». Текущие отчеты по неврологии и неврологии. 14 (8): 469. Дои:10.1007 / s11910-014-0469-1. PMID 24954623. S2CID 22408801.
- ^ а б Сегал А., Миньот Е. (июль 2011 г.). «Генетика сна и нарушений сна». Клетка. 146 (2): 194–207. Дои:10.1016 / j.cell.2011.07.004. ЧВК 3153991. PMID 21784243.
- ^ а б c d е ж грамм час я Mahlios J, De la Herrán-Arita AK, Mignot E (октябрь 2013 г.). «Аутоиммунные основы нарколепсии». Текущее мнение в нейробиологии. 23 (5): 767–73. Дои:10.1016 / j.conb.2013.04.013. ЧВК 3848424. PMID 23725858.
Нарколепсия - неврологическое расстройство, характеризующееся чрезмерной дневной сонливостью, катаплексией, гипнагоническими галлюцинациями, параличом сна и нарушением режима ночного сна.
- ^ а б c d е Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 12: Сон и возбуждение». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 294–296, 303. ISBN 9780071481274.
потеря нейронов орексина поднимает интересную возможность того, что нарколепсия может быть вызвана аутоиммунным разрушением этих нейронов по аналогии с аутоиммунным разрушением инсулин-секретирующих β-островковых клеток при диабете I типа.
- ^ "Изложение фактов о нарколепсии". Природа. 2013. Дои:10.1038 / природа.2013.14413. S2CID 74850662. В архиве из оригинала 22 марта 2019 г.. Получено 25 ноября 2018.
- ^ Кляйн Дж., Сато А. (сентябрь 2000 г.). «Система HLA. Вторая из двух частей». Медицинский журнал Новой Англии. 343 (11): 782–6. Дои:10.1056 / NEJM200009143431106. PMID 10984567.
- ^ а б c Mignot E (ноябрь 2001 г.). «Комментарий к нейробиологии системы гипокретин / орексин». Нейропсихофармакология. 25 (5 Прил.): S5–13. Дои:10.1016 / S0893-133X (01) 00316-5. PMID 11682267.
- ^ Сингх А.К., Малиос Дж., Миньот Е. (июнь 2013 г.). «Генетическая ассоциация, сезонные инфекции и аутоиммунные основы нарколепсии». Журнал аутоиммунитета. 43: 26–31. Дои:10.1016 / j.jaut.2013.02.003. ЧВК 4118764. PMID 23497937.
- ^ Holm A, Lin L, Faraco J, Mostafavi S, Battle A, Zhu X и др. (Ноябрь 2015 г.). «EIF3G ассоциируется с нарколепсией среди этнических групп». Европейский журнал генетики человека. 23 (11): 1573–80. Дои:10.1038 / ejhg.2015.4. ЧВК 4613472. PMID 25669430.
- ^ Сарканен Т., Алакуйяла А., Юлкунен И., Партинен М. (июнь 2018 г.). «Нарколепсия, связанная с вакциной Pandemrix». Текущие отчеты по неврологии и неврологии. 18 (7): 43. Дои:10.1007 / s11910-018-0851-5. HDL:10138/302445. PMID 29855798. S2CID 46926146.
- ^ «MPA расследует сообщения о нарколепсии у пациентов, вакцинированных Pandemrix». Шведское агентство медицинских продуктов. 18 августа 2010 г. В архиве из оригинала 17 февраля 2011 г.. Получено 19 августа 2010.
- ^ "Terveyden ja hyvinvoinnin laitos suosittaa Pandemrix-rokotusten keskeyttämistä". Национальный институт здоровья и социального обеспечения. 24 августа 2010. Архивировано с оригинал 20 июля 2011 г.. Получено 24 августа 2010.
- ^ Ли Дж., Ху З., де Лесеа Л. (январь 2014 г.). «Гипокретины / орексины: интеграторы множества физиологических функций». Британский журнал фармакологии. 171 (2): 332–50. Дои:10.1111 / бут.12415. ЧВК 3904255. PMID 24102345.
Анальгетические свойства пептидов орексина хорошо известны.
- ^ Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. п. 179. ISBN 9780071481274.
Орексинэргические проекции в ЦНС. Орексиновые нейроны с клеточными телами в латеральной области гипоталамуса (LHA) и заднем гипоталамусе (PH) проецируются по всему мозгу (за исключением мозжечка) с плотными проекциями на норадренергический локус Ceruleus (LC), гистаминергическое туберомамиллярное ядро (TMN), серотонинергические ядра шва , холинергические латеродорсальные и педункулопонтинные ядра (LDT и PPT) и дофаминергическая вентральная тегментальная область (VTA).
- ^ а б c Чоу М., Цао М. (2016). «Система гипокретин / орексин при нарушениях сна: доклинические исследования и клинический прогресс». Природа и наука сна. 8: 81–6. Дои:10.2147 / NSS.S76711. ЧВК 4803263. PMID 27051324.
 Текст был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Текст был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Beersma DG, Dijk DJ, Blok CG, Everhardus I (август 1990 г.). «Депривация быстрого сна в течение 5 часов приводит к немедленному восстановлению быстрого сна и к подавлению интенсивности не-быстрого сна» (PDF). Электроэнцефалография и клиническая нейрофизиология. 76 (2): 114–22. Дои:10.1016/0013-4694(90)90209-3. PMID 1697239.
- ^ а б c d е ж Руофф К., Рай Д. (октябрь 2016 г.). «Рекомендации ICSD-3 и DSM-5 по диагностике нарколепсии: клиническая значимость и практичность». Текущие медицинские исследования и мнения. 32 (10): 1611–1622. Дои:10.1080/03007995.2016.1208643. PMID 27359185. S2CID 19380758.
- ^ Всемирная организация здравоохранения (2018 г.). «Международная классификация болезней» (11-е изд.).
- ^ Американская психиатрическая ассоциация (2013). Диагностическое и Статистическое Руководство по Психическим Расстройствам (5-е изд.). Арлингтон, Вирджиния: Американская психиатрическая ассоциация.
- ^ Рахман Т., Фарук О, Хейят ББ, Сиддики М.М. (март 2016 г.). «Обзор нарколепсии». Международный журнал перспективных исследований в области науки, техники и технологий. 3 (3). Дои:10.17148 / IARJSET.2016.3320 (неактивно 9 ноября 2020 г.).CS1 maint: DOI неактивен по состоянию на ноябрь 2020 г. (связь)
- ^ «Исследование нарколепсии - часто задаваемые вопросы». Стэнфордский центр нарколепсии. В архиве из оригинала 13 ноября 2015 г.. Получено 15 января 2016.
- ^ Миньот Э., Ламмерс Г.Дж., Рипли Б., Окун М., Невсималова С., Оверим С. и др. (Октябрь 2002 г.). «Роль измерения гипокретина спинномозговой жидкости в диагностике нарколепсии и других гиперсомний». Архив неврологии. 59 (10): 1553–62. Дои:10.1001 / archneur.59.10.1553. PMID 12374492.
- ^ Кантор С., Мочизуки Т., Лопс С.Н., Ко Б., Клейн Е., Кларк Е. и др. (Август 2013). «Генная терапия орексином восстанавливает время бодрствования и поддерживает бодрствование у нарколептических мышей». Спать. 36 (8): 1129–38. Дои:10.5665 / сон.2870. ЧВК 3700709. PMID 23904672.
- ^ Миеда М., Вилли Дж. Т., Хара Дж., Синтон К. М., Сакураи Т., Янагисава М. (март 2004 г.). «Пептиды орексина предотвращают катаплексию и улучшают бодрствование в модели нарколепсии с удалением орексинового нейрона у мышей». Труды Национальной академии наук Соединенных Штатов Америки. 101 (13): 4649–54. Дои:10.1073 / pnas.0400590101. ЧВК 384801. PMID 15070772.
- ^ Хартман Д. (14 ноября 2019 г.). «Агонисты OX2R для лечения нарколепсии I типа» (PDF). Такеда.
- ^ Dauvilliers Y, Arnulf I, Mignot E (февраль 2007 г.). «Нарколепсия с катаплексией». Ланцет. 369 (9560): 499–511. Дои:10.1016 / S0140-6736 (07) 60237-2. PMID 17292770. S2CID 11041392.
- ^ Иранзо А (2011). «Современные диагностические критерии нарколепсии у взрослых». В Baumann CR, Bassetti CL, Scammell TE (ред.). Нарколепсия: патофизиология, диагностика и лечение. Springer. С. 369–381. Дои:10.1007/978-1-4419-8390-9_34. ISBN 978-1-4419-8390-9.
- ^ «Модафинил (продается как Провигил): серьезные кожные реакции». Постмаркетинговые обзоры. 1 (1). Осень 2007 г. В архиве из оригинала 4 марта 2016 г.. Получено 15 марта 2016.
- ^ Хельмус Т., Розенталь Л., Бишоп К., Рорс Т., Сайрон М.Л., Рот Т. (апрель 1997 г.). «Предупреждающие эффекты короткого и длительного сна у нарколептиков, недосыпающих и бдительных людей». Спать. 20 (4): 251–7. Дои:10.1093 / сон / 20.4.251. PMID 9231950.
- ^ а б «XYREM® (оксибат натрия)» (PDF). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Jazz Pharmaceuticals, Inc., 11 апреля 2014 г. В архиве (PDF) из оригинала 4 марта 2016 г.. Получено 9 августа 2015.
- ^ «Письмо об одобрении FDA для Xyrem; Показания: катаплексия, связанная с нарколепсией; 17 июля 2002 г.» (PDF). В архиве (PDF) из оригинала 17 октября 2012 г.
- ^ Boscolo-Berto R, Viel G, Montagnese S, Raduazzo DI, Ferrara SD, Dauvilliers Y (октябрь 2012 г.). «Нарколепсия и эффективность гамма-гидроксибутирата (GHB): систематический обзор и метаанализ рандомизированных контролируемых исследований». Отзывы о медицине сна. 16 (5): 431–43. Дои:10.1016 / j.smrv.2011.09.001. PMID 22055895.
- ^ а б Барато Л., Довилье Y (2019). «Последние достижения в лечении нарколепсии». Терапевтические достижения при неврологических расстройствах. 12: 1756286419875622. Дои:10.1177/1756286419875622. ЧВК 6767718. PMID 31632459.
- ^ Gowda CR, Lundt LP (декабрь 2014 г.). «Механизм действия препаратов от нарколепсии» (PDF). Спектры ЦНС. 19 Приложение 1 (S1): 25–33, тест 25–7, 34. Дои:10.1017 / S1092852914000583. PMID 25403789. S2CID 13660411.
- ^ Caputo F, Zoli G (март 2007 г.). «Лечение нарколепсии с катаплексией». Ланцет. 369 (9567): 1080–1. Дои:10.1016 / S0140-6736 (07) 60522-4. PMID 17398302.
- ^ «НАМИ, Национальный альянс по психическим заболеваниям, эффексорам, частым побочным эффектам». Архивировано из оригинал 18 июля 2012 г.. Получено 23 сентября 2019.
- ^ Александр С, Скаммелл TE (2011). «Серотонинергическая система во сне и нарколепсия». В Baumann CR, Bassetti CL, Scammell TE (ред.). Нарколепсия: патофизиология, диагностика и лечение. Springer. С. 73–84. Дои:10.1007/978-1-4419-8390-9_7. ISBN 978-1-4419-8390-9.
- ^ Postiglione E, Antelmi E, Pizza F, Lecendreux M, Dauvilliers Y, Plazzi G (апрель 2018 г.). «Клинический спектр детской нарколепсии». Отзывы о медицине сна. 38: 70–85. Дои:10.1016 / j.smrv.2017.04.003. PMID 28666745.
- ^ Петерсон П.С., Хусейн А.М. (ноябрь 2008 г.). «Детская нарколепсия». Мозг и развитие. 30 (10): 609–23. Дои:10.1016 / j.braindev.2008.02.004. PMID 18375081. S2CID 3416096.
- ^ Гийемино С., Фромхерц С. (2005). «Нарколепсия: диагностика и лечение». В Kryger MH, Roth T, Dement WC (ред.). Принципы и практика медицины сна (4-е изд.). W.B. Сондерс. С. 780–790. Дои:10.1016 / B0-72-160797-7 / 50072-0. ISBN 978-0-7216-0797-9.
- ^ "Кто подвержен риску нарколепсии?". В архиве из оригинала от 22 сентября 2008 г.
- ^ «Связь между нарколепсией и психическим здоровьем». В архиве из оригинала от 9 августа 2014 г.. Получено 6 июн 2014.
- ^ Торпи MJ, Krieger AC (май 2014 г.). «Поздняя диагностика нарколепсии: характеристика и последствия». Снотворное. 15 (5): 502–7. Дои:10.1016 / j.sleep.2014.01.015. PMID 24780133.
- ^ «DH финансирует частные рецепты на лекарства, в которых отказано пациентам NHS». Журнал службы здравоохранения. 20 июля 2015 г. В архиве из оригинала 24 сентября 2015 г.. Получено 20 июля 2015.
- ^ а б Харпер, Дуглас (2010). «Нарколепсия». Dictionary.com. Интернет-словарь этимологии. В архиве из оригинала 8 марта 2016 г.. Получено 19 августа 2016.
- ^ а б c Mignot EJ (октябрь 2012 г.). «Практическое руководство по терапии синдромов нарколепсии и гиперсомнии». Нейротерапия. 9 (4): 739–52. Дои:10.1007 / s13311-012-0150-9. ЧВК 3480574. PMID 23065655.
- ^ О'Нил, Мэтт (23 мая 2016 г.). «Питолизант / Вакикс». Нарколепсия Великобритания.
- ^ «Лечение нарколепсии рекомендовано к одобрению». Европейское агентство по лекарствам. 20 ноября 2015.
- ^ «Рекомендация по сохранению статуса сирот на момент получения регистрационного удостоверения: Вакикс (питолизант) для лечения нарколепсии» (PDF). Европейское агентство по лекарствам. 19 апреля 2016 г.
- ^ «Нарколепсия с катаплексией или без нее у взрослых: питолизант». Национальный институт здравоохранения и передового опыта (NICE). 14 марта 2017.
- ^ Syed YY (сентябрь 2016 г.). «Питолизант: первое мировое одобрение». Наркотики. 76 (13): 1313–1318. Дои:10.1007 / s40265-016-0620-1. PMID 27438291. S2CID 42684839.
- ^ а б Линн Мари Тротти, доктор медицины (9 августа 2010 г.). «Флумазенил для лечения первичной гиперсомнии». Университет Эмори - Исследовательский альянс Джорджии. ClinicalTrials.gov. В архиве из оригинала 28 октября 2012 г.
- ^ а б Линн Мари Тротти, доктор медицины (15 июня 2010 г.). «Кларитромицин для лечения первичной гиперсомнии». Университет Эмори - Исследовательский альянс Джорджии. ClinicalTrials.gov. В архиве из оригинала от 1 декабря 2012 г.
- ^ Рожь Д. Б., Бливайз Д. Л., Паркер К., Тротти Л. М., Сайни П., Фэрли Дж. И др. (Ноябрь 2012 г.). «Модуляция бдительности при первичной гиперсомнии за счет эндогенного усиления рецепторов ГАМК». Научная трансляционная медицина. 4 (161): 161ra151. Дои:10.1126 / scitranslmed.3004685. PMID 23175709. S2CID 44236050.
- ^ Келти Е., Мартин В., О'Нил Дж., Халс Дж. (Июль 2014 г.). «Использование подкожных препаратов флумазенила для лечения идиопатической гиперсомнии: отчет о болезни». Журнал психофармакологии. 28 (7): 703–6. Дои:10.1177/0269881114523865. PMID 24554692. S2CID 31846588.
- ^ Бек М. (10 декабря 2012 г.). «Ученые пытаются разгадать загадку слишком длительного сна». Журнал "Уолл Стрит. В архиве из оригинала от 8 августа 2017 года.
- ^ «Обновление гиперсомнии». Университет Эмори. В архиве из оригинала 31 мая 2014 г.. Получено 22 апреля 2014.
- ^ Тротти Л.М., Сайни П., Фриман А.А., Бливайз Д., Дженкинс А., Гарсия П., Рай Д. (июнь 2013 г.). «Кларитромицин для лечения гиперсомнии: рандомизированное, двойное слепое, плацебо-контролируемое, перекрестное испытание». Спать. 36: A248.
- ^ Тротти Л.М., Сайни П., Фриман А.А., Бливайз Д.Л., Гарсия П.С., Дженкинс А., Рай Д. Б. (июль 2014 г.). «Улучшение дневной сонливости с помощью кларитромицина у пациентов с ГАМК-связанной гиперсомнией: клинический опыт». Журнал психофармакологии. 28 (7): 697–702. Дои:10.1177/0269881113515062. PMID 24306133. S2CID 13121904.
- ^ Миягава Т., Миядера Х, Танака С., Кавасима М, Шимада М, Хонда Y и др. (Март 2011 г.). «Аномально низкие уровни ацилкарнитина в сыворотке крови у пациентов с нарколепсией». Спать. 34 (3): 349–53A. Дои:10.1093 / сон / 34.3.349. ЧВК 3041711. PMID 21358852.
- ^ Miyagawa T, Honda M, Kawashima M, Shimada M, Tanaka S, Honda Y, Tokunaga K (30 апреля 2009 г.). «Полиморфизм, расположенный между CPT1B и CHKB и гаплотипом HLA-DRB1 * 1501-DQB1 * 0602, придает восприимчивость к гиперсомнии ЦНС (эссенциальной гиперсомнии)». PLOS ONE. 4 (4): e5394. Bibcode:2009PLoSO ... 4.5394M. Дои:10.1371 / journal.pone.0005394. ЧВК 2671172. PMID 19404393.
- ^ Миягава Т., Кавамура Х., Обучи М., Икесаки А., Одзаки А., Токунага К. и др. (2013). «Эффекты перорального приема L-карнитина у пациентов с нарколепсией: рандомизированное, двойное слепое, перекрестное и плацебо-контролируемое исследование». PLOS ONE. 8 (1): e53707. Bibcode:2013PLoSO ... 853707M. Дои:10.1371 / journal.pone.0053707. ЧВК 3547955. PMID 23349733.
- ^ а б c Кумар С., Сагили Х (февраль 2014 г.). «Этиопатогенез и нейробиология нарколепсии: обзор». Журнал клинико-диагностических исследований. 8 (2): 190–5. Дои:10.7860 / JCDR / 2014 / 7295.4057. ЧВК 3972560. PMID 24701532.
- ^ а б c d е ж Тотх Л.А., Бхаргава П. (апрель 2013 г.). «Животные модели нарушений сна». Сравнительная медицина. 63 (2): 91–104. ЧВК 3625050. PMID 23582416.
- ^ Liblau RS, Vassalli A, Seifinejad A, Tafti M (март 2015 г.). «Биология гипокретина (орексина) и патофизиология нарколепсии с катаплексией». Ланцет. Неврология. 14 (3): 318–28. Дои:10.1016 / S1474-4422 (14) 70218-2. PMID 25728441. S2CID 18455770.
- ^ Бейкер Т.Л., Фаутц А.С., Макнерни В., Митлер М.М., Демент В.К. (март 1982 г.). «Собачья модель нарколепсии: генетические детерминанты и факторы развития». Экспериментальная неврология. 75 (3): 729–42. Дои:10.1016/0014-4886(82)90038-3. PMID 7199479. S2CID 41039138.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
- "Информационная страница о нарколепсии". Национальный институт неврологических расстройств и инсульта.
