Пиразин - Pyrazine
| |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Пиразин | |||
| Другие имена 1,4-Диазабензол, п-Диазин, 1,4-Диазин, Парадиазин, Пиазин, ООН 1325 | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.480 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C4ЧАС4N2 | |||
| Молярная масса | 80,09 г / моль | ||
| Внешность | Белые кристаллы | ||
| Плотность | 1,031 г / см3 | ||
| Температура плавления | 52 ° С (126 ° F, 325 К) | ||
| Точка кипения | 115 ° С (239 ° F, 388 К) | ||
| Растворимый | |||
| Кислотность (пKа) | 0.37[1] (протонированный пиразин) | ||
| -37.6·10−6 см3/ моль | |||
| Опасности | |||
| R-фразы (устарело) | R11, R36 / 37/38 | ||
| S-фразы (устарело) | S16, S26, S36 | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 55 ° С (131 ° F, 328 К) c.c. | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пиразин это гетероциклический ароматный органическое соединение с химическая формула C4ЧАС4N2. Это симметричная молекула с точечная группа D2ч. Пиразин менее прост, чем пиридин, пиридазин и пиримидин.
Пиразин и различные алкилпиразины представляют собой вкусовые и ароматические соединения, содержащиеся в выпечке и жареных изделиях. Тетраметилпиразин (также известный как лигустразин), как сообщается, удаляет супероксид-анион и уменьшить оксид азота производство в человеческом полиморфноядерные лейкоциты.[2]
Синтез
Существует множество методов для органический синтез пиразина и его производных. Некоторые из них являются одними из самых старых реакций синтеза, которые все еще используются.
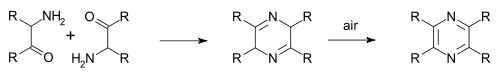
в Синтез пиразина Штеделя – Ругхаймера (1876) 2-хлорацетофенон реагирует с аммиак до аминокетона, затем конденсируется и затем окисляется до пиразина.[3] Вариант - это Синтез пиразина Gutknecht (1879) также на основе этого самоконденсация, но отличаются способом синтеза альфа-кетоамина.[4][5]
В Синтез Гастальди (1921) - еще одна вариация:[6][7]
Смотрите также
- Алкилпиразины
- Бензол, аналог без атомов азота
- Метоксипиразины
- Пиридазин, аналог со вторым атомом азота в позиции 2
- Пиридин, аналог только с одним атомом азота
- Пиримидин, аналог со вторым азот атом в позиции 3
- Простые ароматические кольца
Рекомендации
- ^ Brown, H.C. и др., В Baude, E.A. и Наход, ФК, Определение органических структур физическими методами, Academic Press, Нью-Йорк, 1955.
- ^ Чжан, Чжаохуэй (2003). «Тетраметилпиразин улавливает супероксид-анион и снижает выработку оксида азота в полиморфно-ядерных лейкоцитах человека». Науки о жизни. 72 (22): 2465–2472. Дои:10.1016 / S0024-3205 (03) 00139-5. PMID 12650854.
- ^ Ueber die Einwirkung von Ammoniak auf Chloracetylbenzol (стр. 563–564) W. Staedel, L. Rügheimer Дои:10.1002 / cber.187600901174 Berichte der deutschen chemischen Gesellschaft Том 9, выпуск 1, стр. 563–564, 1876 г.
- ^ Mittheilungen Ueber Nitrosoäthylmethylketon Х. Гуткнехт Berichte der deutschen chemischen Gesellschaft Том 12, выпуск 2, стр. 2290–2292, 1879 г. Дои:10.1002 / cber.187901202284
- ^ Гетероциклическая химия T.L. Гилкрист ISBN 0-582-01421-2
- ^ Г. Гастальди, Gazz. Чим. Ital. 51, (1921) 233
- ^ Амины: синтез, свойства и применение Стивен А. Лоуренс 2004 Издательство Кембриджского университета ISBN 0-521-78284-8