Рак мочевого пузыря - Bladder cancer
| Рак мочевого пузыря | |
|---|---|
 | |
| Переходно-клеточный рак мочевого пузыря. Белый цвет в мочевом пузыре контрастный. | |
| Специальность | Онкология, урология |
| Симптомы | Кровь в моче, боль при мочеиспускании[1] |
| Обычное начало | От 65 до 84 лет[2] |
| Типы | Переходно-клеточная карцинома, плоскоклеточная карцинома, аденокарцинома[1] |
| Факторы риска | Курение, семейная история, до радиационная терапия, часто инфекции мочевого пузыря, некоторые химические вещества[1] |
| Диагностический метод | Цистоскопия с биопсия тканей[1] |
| Уход | Хирургия, лучевая терапия, химиотерапия, иммунотерапия[1] |
| Прогноз | Пятилетняя выживаемость ~ 77% (США)[2] |
| Частота | 549000 новых случаев (2018)[3] |
| Летальные исходы | 200,000 (2018)[3] |
Рак мочевого пузыря любой из нескольких типов рак вытекающие из ткани из мочевой пузырь.[1] Симптомы включают: кровь в моче, боль при мочеиспускании, и боли в пояснице.[1]
Факторы риска рака мочевого пузыря включают: курение, семейная история, до радиационная терапия, часто инфекции мочевого пузыря и воздействие определенных химикатов.[1] Самый распространенный тип - переходно-клеточная карцинома.[1] Другие типы включают плоскоклеточная карцинома и аденокарцинома.[1] Диагноз обычно ставится цистоскопия с биопсия тканей.[4] Стадия рака определяется трансуретральная резекция и медицинская визуализация.[1][5][6]
Лечение зависит от стадия рака.[1] Он может включать некоторую комбинацию хирургического вмешательства, лучевой терапии, химиотерапия, или же иммунотерапия.[1] Хирургические варианты могут включать трансуретральную резекцию, частичное или полное удаление мочевого пузыря или отведение мочи.[1] Типичный пятилетняя выживаемость в США - 77%, в Канаде - 75% и в Европе - 68%.[2][7][8]
По состоянию на 2018 год от рака мочевого пузыря во всем мире пострадало около 1,6 миллиона человек, из них 549 000 новых случаев заболевания и 200 000 смертей.[3] Возраст начала заболевания чаще всего составляет от 65 до 84 лет.[2] Мужчины болеют чаще, чем женщины.[2] В 2018 году самый высокий уровень заболеваемости раком мочевого пузыря был зарегистрирован в Южной и Западной Европе, за которой следовала Северная Америка с показателями 15, 13 и 12 случаев на 100000 человек.[3] Самые высокие показатели смертности от рака мочевого пузыря наблюдались в Северной Африке и Западной Азии, за которыми следовала Южная Европа.[3]
Признаки и симптомы

Рак мочевого пузыря обычно вызывает кровь в моче, которые можно увидеть или обнаружить только под микроскопом. Кровь в моче является наиболее частым симптомом рака мочевого пузыря и протекает безболезненно. Видимая кровь в моче может быть кратковременной, и может потребоваться анализ мочи для подтверждения невидимой крови. От 80 до 90% людей с раком мочевого пузыря изначально имели видимую кровь.[9] Кровь в моче также может быть вызвана другими состояниями, такими как мочевой пузырь или камни мочеточника, инфекция, заболевание почек, рак почек или сосудистые мальформации, хотя эти состояния (кроме рак почек ) обычно было бы болезненно.
Другие возможные симптомы включают: боль при мочеиспускании, частое мочеиспускание или чувство позывов к мочеиспусканию без возможности сделать это. Эти признаки и симптомы не являются специфическими для рака мочевого пузыря, а также могут быть вызваны незлокачественными заболеваниями, в том числе: предстательная железа инфекции, гиперактивность мочевого пузыря или цистит. Некоторые редкие формы рака мочевого пузыря, такие как урахальная аденокарцинома производить муцин, который затем выводится с мочой, делая ее густой.[10]
Люди с запущенным заболеванием могут испытывать боль в области таза или костей, нижних конечностях. припухлость, или же боль в боку.[11] В редких случаях при физикальном осмотре можно обнаружить пальпируемое образование.[12]
Причины
Табак курение является основным известным фактором развития рака мочевого пузыря; в большинстве групп населения курение связано более чем с половиной случаев рака мочевого пузыря у мужчин и одной третью случаев у женщин,[13] однако эта пропорция уменьшилась за последние годы, поскольку в Европе и Северной Америке стало меньше курильщиков.[14] Существует почти линейная зависимость между продолжительностью курения (в годах), упаковать годы и риск рака мочевого пузыря. Можно наблюдать плато риска при выкуривании около 15 сигарет в день (это означает, что те, кто выкуривает 15 сигарет в день, подвергаются примерно такому же риску, как и те, кто выкуривает 30 сигарет в день). Курение (сигары, трубки, египетские кальяны и бездымный табак) в любой форме увеличивает риск рака мочевого пузыря.[15] Отказ от курения снижает риск. Риск рака мочевого пузыря снижается на 30% в течение 1–4 лет и продолжает снижаться на 60% через 25 лет после отказа от курения.[16] Однако бывшие курильщики, скорее всего, всегда будут подвержены более высокому риску рака мочевого пузыря по сравнению с людьми, которые никогда не курили.[14] Пассивное курение также представляет собой риск.[17][18]
Опиум потребление увеличивает риск рака мочевого пузыря в 3 раза, а одновременное употребление опиума и курения увеличивает риск рака мочевого пузыря в 5 раз по сравнению с населением в целом.[19]
Тридцать процентов опухолей мочевого пузыря, вероятно, возникают в результате профессионального воздействия канцерогенов на рабочем месте. Профессиональное или косвенное воздействие следующих веществ считается причиной рака мочевого пузыря; бензидин (производство красителей), 4-аминобифенил (резиновая промышленность), 2-нафтиламин (производство азокрасителей, литейный дым, резиновая промышленность, сигаретный дым и исследования рака), фенацетин (обезболивающее), мышьяк и хлорированный алифатические углеводороды в питьевой воде, аурамин (производство красителей), пурпурный (производство красителей), орто-толуидин (производство красителей), эпоксидная смола и полиуретан отвердители смол (промышленность пластмасс), хлорнафазин, каменноугольный пек.[20][21][22][23][24] Риску подвержены водители автобусов, резиновые рабочие, маляры, механики, кожевники (включая сапожники), кузнецы, наладчики станков и механики.[25][26] Считается, что парикмахеры также подвержены риску из-за того, что они часто используют стойкие краски для волос.[27]
Заражение Schistosoma haematobium (бильгарция или шистосомоз ) может вызвать рак мочевого пузыря, особенно плоскоклеточного типа.[28] Шистосома яйца вызывает хронический воспалительный состояние стенки мочевого пузыря, приводящее к фиброзу тканей.[29] Более высокие уровни N-нитрозо соединения были обнаружены в образцах мочи людей с шистосомозом.[30] Соединения N-нитрозо вовлечены в патогенез рака мочевого пузыря, связанного с шистосомозом. Они вызывают повреждение ДНК алкилирования, особенно Гуанин к Аденин переходные мутации в HRAS и p53 ген-супрессор опухоли.[31] Мутации p53 обнаруживаются в 73% опухолей, BCL-2 мутации составляют 32%, а комбинация этих двух составляет 13%.[32] Другие причины плоскоклеточная карцинома мочевого пузыря включают хроническую катетеризацию у людей с повреждение спинного мозга и история лечения циклофосфамидом.[33][34]
Проглатывание аристолоховая кислота присутствует во многих китайских лекарственные травы было показано, что вызывает уротелиальную карциному и почечная недостаточность.[35] Аристолоховая кислота активирует пероксидаза в уротелий и причины трансверсия мутация в TP53 подавитель опухолей ген.
Люди, которые проходят дистанционная лучевая терапия (ДЛТ) рака простаты имеют более высокий риск развития инвазивного рака мочевого пузыря.[36]
В дополнение к этим основным факторам риска существует также множество других модифицируемых факторов, которые менее сильно (т. Е. Увеличение риска на 10-20%) связаны с раком мочевого пузыря, например, ожирение.[37] Хотя они могут рассматриваться как второстепенные эффекты, снижение риска в общей популяции все же может быть достигнуто за счет одновременного снижения распространенности ряда меньших факторов риска.[38]
Генетика
Мутации в FGFR3, TP53, PIK3CA, KDM6A, ARID1A, KMT2D, HRAS, TERT, KRAS, CREBBP, RB1 и TSC1 гены могут быть связаны с некоторыми случаями рака мочевого пузыря.[39][40][41] Удаление частей или всего хромосома 9 часто встречается при раке мочевого пузыря.[42] Известно, что рак низкой степени злокачественности содержит мутации в Путь RAS и ген рецептора 3 фактора роста фибробластов (FGFR3), оба из которых играют роль в Путь MAPK / ERK. p53 и РБ генные мутации вовлечены в высокосортные мышечные инвазивные опухоли.[43] Восемьдесят девять процентов инвазивных видов рака имеют мутации в ремоделирование хроматина и гены, модифицирующие гистоны.[44]Удаление обеих копий GSTM1 ген имеет умеренное увеличение риска рака мочевого пузыря. Продукт гена GSTM1 глутатион S-трансфераза M1 (GSTM1) участвует в процессе детоксикации канцерогенов, таких как полициклические ароматические углеводороды найдено в сигаретном дыме.[45] Точно так же мутации в NAT2 (N-ацетилтрансфераза ) связан с повышенным риском рака мочевого пузыря. N-ацетилтрансфераза помогает в детоксикации канцерогены подобно ароматические амины (также присутствует в сигаретном дыме).[46] Различные однонуклеотидные полиморфизмы в Ген PSCA присутствует на хромосома 8 показали, что увеличивают риск рака мочевого пузыря. Ген PSCA промоутер регион имеет андроген область ответа. Утрата реактивности этой области к андрогенам считается причиной большего количества агрессивных опухолей у женщин (в отличие от мужчин, у которых больше андрогенов).[47]
Мышечно-инвазивный рак мочевого пузыря неоднороден по своей природе. В целом их можно генетически разделить на базальный и просветный подтипы. Базальный подтип показывает изменения с участием RB и NFE2L2 и люминальный тип показывают изменения в генах FGFR3 и KDM6A.[48] Базальный подтип подразделяется на базальный и Клодин группы низкого типа и агрессивны и демонстрируют метастазы при обращении, однако они реагируют на химиотерапию на основе платины. Люминальный подтип можно разделить на р53-подобный и люминальный. р53-подобные опухоли люминального подтипа, хотя и не столь агрессивны, как базальный тип, но проявляют устойчивость к химиотерапия[49]
Диагностика

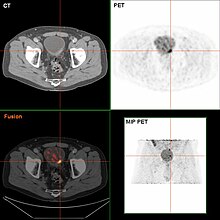
В настоящее время лучший диагноз состояния мочевого пузыря - это цистоскопия, при которой гибкая или жесткая трубка (называемая цистоскоп) с камерой и различными инструментами вводится в мочевой пузырь через уретра. Гибкая процедура позволяет проводить визуальный осмотр мочевого пузыря, выполнять незначительные восстановительные работы и брать образцы подозрительных поражений для последующего исследования. биопсия. Жесткий цистоскоп используется под общей анестезией в операционной и может поддерживать лечебные работы и биопсию, а также более обширное удаление опухоли. В отличие от папиллярных поражений, которые прорастают в полость мочевого пузыря и хорошо видны, карцинома in situ поражения плоские и неясные. Выявление карциномы in situ требует проведения нескольких биопсий из разных областей внутренней стенки мочевого пузыря.[50] Фотодинамическое обнаружение (цистоскопия в синем свете) может помочь в обнаружении карциномы in situ. При фотодинамическом обнаружении краситель вводится в мочевой пузырь с помощью катетера. Раковые клетки поглощают этот краситель и видны в синем свете, обеспечивая визуальные подсказки на участках, подлежащих биопсии или резекции.[51]
Однако визуального обнаружения в любой из перечисленных выше форм недостаточно для определения патологической классификации, типа клеток или стадии данной опухоли. Так называемая холодная чашка биопсия во время обычной цистоскопии (жесткой или гибкой) также будет недостаточно для определения стадии патологии. Следовательно, после визуального обнаружения необходимо провести трансуретральную операцию. Процедура называется трансуретральная резекция опухоли мочевого пузыря (ТУРБТ). Кроме того, до и после ТУР следует провести ректальное и вагинальное бимануальное исследование, чтобы определить, есть ли пальпируемое образование или опухоль зафиксирована («привязана») к стенке таза. Патологическая классификация и информация о стадиях, полученная с помощью процедуры TURBT, имеют фундаментальное значение для правильного выбора последующего лечения и / или последующих процедур.[52]
Если инвазивный или высокой степени (включая карцинома in situ ) рак выявляется на ТУР, МРТ и / или компьютерная томография брюшной полости и таза или урограмма и КТ грудной клетки или Рентгеновский грудную клетку следует проводить для определения стадии заболевания и поиска распространения рака (метастаз ). Увеличить в щелочная фосфатаза уровни без признаков заболевания печени следует оценивать на предмет костный метастаз по рентген.[53] Несмотря на то что 18F-фтордезоксиглюкоза (ФДГ) -позитронно-эмиссионная томография (ПЭТ) / КТ была изучена как жизнеспособный метод определения стадии, но нет единого мнения, подтверждающего ее роль в рутинных клинических оценках.[51]
Цитология мочи может быть получен при мочеиспускании или во время цистоскопии («промывание мочевого пузыря»). Цитология не очень чувствительна к опухолям низкой степени злокачественности или степени 1 (отрицательный результат не может надежно исключить рак мочевого пузыря), но имеет высокую специфичность (положительный результат надежно обнаруживает рак мочевого пузыря).[54] Существуют более новые неинвазивные маркеры связывания мочи, доступные в качестве вспомогательных средств в диагностике рака мочевого пузыря, в том числе у человека. фактор дополнения H родственный белок, высокомолекулярный карциноэмбриональный антиген и ядерный матриксный белок 22 (NMP22).[55] В Соединенных Штатах FDA одобрила тесты NMP22, NMP22 BladderChek и UroVysion для обнаружения и наблюдения за раком мочевого пузыря, а тесты ImmunoCyt, BTA-TRAK и BTA-STAT были утверждены только для наблюдения. BTA-STAT и BladderChek могут выполняться в клинике, а другие - в лаборатории.[56][57] Другие неинвазивные тесты мочи включают анализ рака мочевого пузыря CertNDx, который выявляет FGFR3 мутации и тест на рак мочевого пузыря (UBC), который представляет собой бутерброд ELISA за Цитокератин 8 / 18 фрагмент. Точно так же NMP22 - это бутерброд ELISA и NMP22 BladderChek - щуп иммуноанализ, оба они обнаруживают белок ядерного митотического аппарата (NuMA) онкомаркер (тип белка ядерного матрикса).[58] UroVysion - это флуоресценция in situ гибридизация который обнаруживает анеуплоидию в хромосомах 3, 7, 17 и потерю локуса 9p21.[59][60] ImmunoCyt - это Иммунофлуоресценция тест, который обнаруживает гликозилированный CEA и МУСИН -подобные антигены (M344, LDQ10, 19A11).[58][59] БТА-СТАТ - щуп иммуноанализ для обнаружения человека фактор дополнения H родственный белок. БТА-ТРАК - бутерброд ELISA который также определяет белок, связанный с фактором комплемента Н. человека.[58] Чувствительность по биомаркерам варьировала от 0,57 до 0,82 и особенности от 0,74 до 0,88. Биомаркеры показали лучшие результаты при использовании в сочетании с цитологическим исследованием мочи, чем при использовании по отдельности. Однако точность обнаружения рака низкой степени злокачественности низкая, и 10% случаев рака все еще не учитываются.[56] Текущие руководства не рекомендуют использовать биомаркеры мочи для обнаружения и наблюдения.[61]
Классификация

| Тип | Относительная заболеваемость | Подтипы |
|---|---|---|
| Переходно-клеточная карцинома | 95%[62][63] | Папиллярный (70%[62]) |
| Непапиллярный (30%[62]) | ||
| Непереходно-клеточная карцинома | 5% [62][63] | Плоскоклеточный рак, аденокарциномы, саркомы, мелкоклеточные карциномы и вторичные отложения от рака в других частях тела.[63] |
Непапиллярная карцинома включает карциному in situ (CIS), микроинвазивную карциному и откровенно инвазивную карциному.[64] Карцинома на месте (CIS) неизменно состоит из цитологически высокосортных опухолевых клеток.[65]
Переходно-клеточная карцинома может дифференцироваться (25%) на свои варианты.[64][66][67] При наблюдении под микроскопом папиллярная переходно-клеточная карцинома может проявляться в своей типичной форме или как одна из ее разновидностей (плоскоклеточный, железистая дифференцировка или микропапиллярный вариант). Ниже перечислены различные варианты непапиллярной переходно-клеточной карциномы.
| Вариант | Гистология | Процент непапиллярных случаев | Подразумеваемое[68] |
|---|---|---|---|
| Плоская дифференциация | Наличие межклеточных мостиков или ороговение | 60% | Результаты аналогичны обычному переходно-клеточному раку. |
| Железистая дифференцировка | Наличие истинных железистых пространств | 10% | |
| Саркоматоидные очаги | Наличие как эпителиальной, так и мезенхимальной дифференцировки | 7% | Клинически агрессивный[69] |
| Микропапиллярный вариант | Похоже на папиллярно-серозная карцинома яичника или напоминающий микропапиллярный рак груди или легкого[70] | 3.7% | Клинически агрессивная, рекомендуется ранняя цистэктомия |
| Карцинома уротелия с мелкими канальцами и микрокистозной формой | Наличие кист размером от микроскопических до 1-2 мм. | Редкий | |
| Лимфоэпителиомоподобная карцинома | Похоже на лимфоэпителиома носоглотки | ||
| Лимфомоподобные и плазмоцитоидные варианты | Злокачественные клетки напоминают клетки злокачественных лимфома или плазмоцитома | ||
| Вложенный вариант | Гистологически похожи на гнезда фон Брунна. | Может быть ошибочно диагностирован как доброкачественная болезнь фон Брунна или неинвазивная папиллярная уротелиальная карцинома низкой степени злокачественности. | |
| Уротелиальная карцинома с гигантскими клетками | Наличие гигантских клеток эпителиальной опухоли и выглядит как гигантоклеточный рак легкого | ||
| Трофобластическая дифференциация | Наличие синцитиотрофобластических гигантских клеток или хориокарциноматозной дифференцировки может выражаться ХГЧ | ||
| Вариант с чистой ячейкой | Чистый клеточный узор с богатой гликогеном цитоплазмой | ||
| Плазмацитоид | Клетки с высоким содержанием липидов, имитирующие аденокарциному с перстневым кольцом желудка / дольчатый рак молочной железы | Клинически агрессивный, склонность к перитонеальному распространению | |
| Необычные стромальные реакции | Наличие подписчиков; псевдосаркоматозная строма, стромальная костная или хрящевая метаплазия, гигантские клетки типа остеокластов, лимфоидный инфильтрат |
Постановка
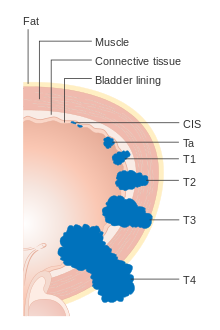




Рак мочевого пузыря классифицируется (классифицируется по степени распространения рака) и классифицируется (насколько аномальные и агрессивные клетки выглядят под микроскопом) для определения лечения и оценки результатов. Определение стадии обычно следует за первой трансуретральной резекцией опухоли мочевого пузыря (ТУР мочевого пузыря). Папиллярные опухоли, ограниченные слизистой оболочкой или поражающие собственная пластинка классифицируются как Ta или T1. Плоские поражения классифицируются как Tis. Оба сгруппированы вместе как неинвазивные заболевания мышц для терапевтических целей.
в Промежуточная система TNM (8-е издание, 2017 г.) при раке мочевого пузыря:[71][72]
Т (первичная опухоль)
- TX Первичная опухоль не поддается оценке
- T0 Нет доказательств первичной опухоли
- Та Неинвазивная папиллярная карцинома
- Это Карцинома in situ (плоская опухоль)
- Т1 Опухоль поражает субэпителиальную соединительную ткань
- T2a Опухоль поражает поверхностную мышцу (внутреннюю половину детрузорная мышца )[73]
- T2b Опухоль поражает глубокую мышцу (внешнюю половину мышцы детрузора)[73]
- Т3 Опухоль поражает перивезикальную ткань:
- T3a Микроскопически
- T3b Макроскопически (экстрапузырная масса)
- T4a Опухоль вторгается предстательная железа, матка или влагалище
- T4b Опухоль вторгается стенка таза или брюшная стенка
N (лимфатические узлы)
- NX Региональные лимфатические узлы не могут быть оценены
- N0 Нет метастазов в регионарные лимфатические узлы
- N1 Метастаз в единичном лимфатическом узле в истинном тазу (гипогастральный, запирательный, наружная подвздошная кость, или пресакральные узлы)
- N2 Метастазы во множественные лимфатические узлы в истинном тазу (гипогастральный, запирательный, наружные подвздошные или пресакральные узлы)
- N3 Метастаз в общие подвздошные лимфатические узлы
М (отдаленные метастазы)
- MX Отдаленные метастазы не поддаются оценке
- M0 Нет отдаленных метастазов
- M1 Отдаленные метастазы.
- M1a: Рак распространился только на лимфатические узлы за пределами таза.
- M1b: Рак распространился на другие части тела.
Наиболее частыми местами метастазов рака мочевого пузыря являются лимфатические узлы, кости, легкие, печень и брюшина.[74] Самый распространенный сторожевые лимфатические узлы дренирующий рак мочевого пузыря - запирательный и внутренние подвздошные лимфатические узлы. Расположение лимфатического распространения зависит от расположения опухолей. Опухоли на надбоковой стенке мочевого пузыря распространяются на внешние подвздошные лимфатические узлы. Опухоли шеи, передней стенки и глазного дна обычно распространяются на внутренние подвздошные лимфатические узлы.[75] Из регионарных лимфатических узлов (то есть запирательных, внутренних и внешних лимфатических узлов) рак распространяется на отдаленные участки, такие как общие подвздошные лимфатические узлы и парааортальные лимфатические узлы.[76] Пропущено лимфатический узел при раке мочевого пузыря поражения не наблюдаются.[75]
Числовой
Вышеупомянутые этапы могут быть интегрированы в числовую стадию (с римские цифры ) следующим образом:[77]
| стадия | Опухоль | Узлы | Метастаз | 5-летняя выживаемость в США[78] |
|---|---|---|---|---|
| Этап 0а | Та | N0 | M0 | 98% |
| Этап 0is | Это | N0 | M0 | 95% |
| I этап | Т1 | N0 | M0 | 63% |
| II этап | T2a | N0 | M0 | |
| T2b | ||||
| Стадия IIIA | T3a | N0 | M0 | 35% |
| T3b | ||||
| T4a | ||||
| T1-4a | N1 | |||
| Стадия IIIB | T1-4a | N2 | M0 | |
| N3 | ||||
| Стадия IVA | T4b | Любой N | M0 | |
| Любой T | M1a | |||
| Стадия IVB | Любой T | ny N | M1b | 5% |
Оценка
Согласно классификации ВОЗ (1973) рак мочевого пузыря гистологически подразделяется на:[79]
- G1 - хорошо дифференцированный,
- G2 - Умеренно дифференцированный
- G3 - Слабо дифференцированный
Классификация ВОЗ (2004/2016)[80][81]
- Папиллярные поражения
- Уротелиальная папиллома
- Папиллярное уротелиальное новообразование низкого злокачественного потенциала (PUNLMP)
- Низкая оценка
- Высокий класс
- Плоские поражения
- Уротелиальное разрастание с неопределенным злокачественным потенциалом
- Реактивная атипия
- Атипия неизвестного значения
- Уротелиальная дисплазия
- Уротелиальный КИС (всегда высокого класса)
- Начальный
- Вторичный
- Одновременный
Стратификация риска
Люди с немышечно-инвазивным раком мочевого пузыря (NMIBC) стратифицируются по риску на основе клинических и патологических факторов, так что они получают соответствующее лечение в зависимости от их вероятности прогрессирования и / или рецидива.[82] Люди с неинвазивными мышечными опухолями делятся на группы с низким, средним и высоким риском или имеют числовую оценку риска. Структура стратификации риска обеспечивается Американской ассоциацией урологов / Обществом урологической онкологии (стратификация AUA / SUO), рекомендациями Европейской ассоциации урологов (EAU), таблицами риска Европейской организации по исследованию и лечению рака (EORTC) и Club Urológico Español de Tratamiento. Модель оценки Oncológico (CUETO).[83][84][85]
| Низкий риск | Промежуточный риск | Высокий риск |
|---|---|---|
| Солитарная опухоль Ta низкой степени злокачественности, менее 3 см | Рецидив в течение 1 года, опухоль Ta низкой степени злокачественности | Высший сорт Т1 |
| Папиллярное уротелиальное новообразование низкой злокачественности | Одиночная опухоль Ta низкой степени злокачественности размером более 3 см | Любая рецидивирующая опухоль или любой Ta высокой степени злокачественности |
| Низкая степень Та, мультифокальные опухоли | Высококачественный Та, более 3 см (или мультифокальный) | |
| Высококачественный Та, менее 3 см | Любая карцинома in situ | |
| Низкий класс Т1 | Любая неудача БЦЖ при опухолях высокой степени злокачественности | |
| Любой вариант гистологии | ||
| Любая лимфоваскулярная инвазия | ||
| Любое поражение простаты и уретры высокой степени |
В моделях EORTC и CUETO используется совокупная оценка, полученная на основе индивидуальных прогностических факторов, которые затем преобразуются в риск прогрессирования и рецидива. Шесть прогностических факторов, включенных в модель EORTC, - это количество опухолей, частота рецидивов, Т-стадия, наличие карциномы in-situ и степень опухоли. Оценка повторения в модели CUETO включает 6 переменных; возраст, пол, степень, статус опухоли, количество опухолей и наличие тис. Для оценки прогрессии используются предыдущие 6 переменных плюс этап T.[86][87]
| Модель | Накопительный балл за рецидив | Повторяемость через 1 год (%) | Повторяемость через 5 лет (%) |
|---|---|---|---|
| EORTC | 0 | 15 | 31 |
| 1-4 | 24 | 46 | |
| 5-9 | 38 | 62 | |
| 10-17 | 61 | 78 | |
| CUETO | 0-4 | 8.2 | 21 |
| 5-6 | 12 | 36 | |
| 7-9 | 25 | 48 | |
| 10-16 | 42 | 68 |
| Модель | Накопительный балл за прогресс | Прогресс через 1 год (%) | Прогресс через 5 лет (%) |
|---|---|---|---|
| EORTC | 0 | 0.2 | 0.8 |
| 2-6 | 1 | 6 | |
| 7-13 | 5 | 17 | |
| 12-23 | 17 | 45 | |
| CUETO | 0-4 | 1.2 | 3.7 |
| 5-6 | 3 | 12 | |
| 7-9 | 5.5 | 21 | |
| 10-16 | 14 | 34 |
Профилактика
По состоянию на 2019 год существует ограниченное количество доказательств высокого уровня, позволяющих предположить, что употребление овощей и фруктов снижает риск рака мочевого пузыря.[46] Исследование 2008 г. пришло к выводу, что "специфические фрукты и овощи может снизить риск рака мочевого пузыря ».[90] Фрукты и желто-оранжевые овощи, особенно морковь и те, которые содержат селен,[91] вероятно, связаны с умеренно сниженным риском рака мочевого пузыря. Цитрусовые фрукты и крестоцветные овощи были также определены как обладающие возможно защитным действием. Однако анализ 47 909 мужчин в рамках последующего исследования медицинских работников показал слабую связь между снижением рака и высоким потреблением фруктов и овощей в целом или желтых или зеленолистных овощей в частности, по сравнению со снижением, наблюдаемым среди тех мужчин, которые потребляли большое количество крестоцветные овощи. Обратное соотношение между поступлениями флавонолы и лигнаны (дифенольный соединения, обнаруженные в цельное зерно, бобовые, фрукты и овощи) описан также агрессивный рак мочевого пузыря.[92]
Хотя предполагается, что полифенольные соединения в чай может оказывать ингибирующее действие на образование и рост опухоли мочевого пузыря, есть ограниченные доказательства того, что употребление чая снижает риск рака мочевого пузыря.[46]
В 10-летнем исследовании с участием почти 49000 мужчин исследователи обнаружили, что мужчины, которые выпивают не менее 1,44 л воды (около 6 чашек) в день, имеют меньший риск рака мочевого пузыря по сравнению с мужчинами, которые меньше пьют. Также было обнаружено, что «риск рака мочевого пузыря снижается на 7% на каждые 240 мл добавленной жидкости».[93] Авторы предположили, что рак мочевого пузыря может частично быть вызван прямым контактом мочевого пузыря. канцерогены которые выводятся с мочой, хотя это еще не было подтверждено другими исследованиями.[90]
Скрининг
По состоянию на 2019 год недостаточно доказательств, чтобы определить, скрининг при раке мочевого пузыря у людей без симптомов эффективен или нет.[94]
Уход

Лечение рака мочевого пузыря зависит от того, насколько глубоко опухоль проникает в стенку мочевого пузыря.
Стратегии лечения рака мочевого пузыря включают:[95][96]
- Немышечные инвазивные: трансуретральная резекция опухоли мочевого пузыря (ТУР мочевого пузыря) с или без интавезикальной химиотерапии или иммунотерапии
- Мышечный инвазивный
- Этап II / Этап IIIA: радикальная цистэктомия плюс неоадъювантная химиотерапия (мультимодальная терапия, предпочтительно) или трансуретральная резекция с химиолучевой терапией (тримодальная терапия, тщательно отобранные люди) или частичная цистэктомия плюс неоадъювантная химиотерапия (у тщательно отобранных людей)
- Стадия IIIB / IVA: химиотерапия на основе цисплатина с последующей радикальная цистэктомия или химиолучевое лечение, или наблюдение в зависимости от ответа на лечение
- Стадия IVB (местнораспространенная; неоперабельные опухоли): паллиативная лучевая терапия
- Метастатическое заболевание: цисплатин химиотерапия на основе
- Метастатическое заболевание, но не подходит для химиотерапии на основе цисплатина: карбоплатин химиотерапия на основе
- Метастатическое заболевание с противопоказанием к химиотерапии: ингибиторы КПП, если запрограммированная смерть лиганд 1 (PD L1 ) положительный
- Плоскоклеточный рак или аденокарцинома мочевого пузыря: радикальная цистэктомия
Немышечные инвазивные
Трансуретральная резекция
Немышечный инвазивный рак мочевого пузыря (не проникающий в мышечный слой мочевого пузыря) можно «сбрить» с помощью электрокаутеризация устройство, подключенное к цистоскоп, который в этом случае называется резектоскопом. Процедура называется трансуретральной резекцией опухоли мочевого пузыря (ТУР мочевого пузыря) и служит в первую очередь для определения стадии патологии. В случае немышечно-инвазивного рака мочевого пузыря ТУР мочевого пузыря сама по себе является лечением, но в случае мышечно-инвазивного рака эта процедура недостаточна для окончательного лечения.[52] Дополнительно синий свет цистоскопия с препаратом для оптической визуализации Гексаминолевулинат (HAL) рекомендуется при первичной ТУР, чтобы увеличить обнаружение поражения (особенно карциномы in situ) и улучшить качество резекции, тем самым уменьшив рецидив.[97][98] Важно оценить качество резекции, если есть доказательства неполной резекции или в образце нет мышцы (без которой невозможно определить инвазивность мышц), настоятельно рекомендуется повторная ТУР. Более того, почти у половины людей с неинвазивным заболеванием высокой степени злокачественности остается остаточная опухоль после первичной ТУР МГНТ, в таких случаях важна повторная ТУР МГ, чтобы избежать заниженной стадии.[99][100] На этом этапе рекомендуется классифицировать людей по группам риска. Лечение и наблюдение для различных групп риска указаны в таблице ниже.
Химиотерапия

Однократная инстилляция химиотерапии в мочевой пузырь после первичной ТУРМТ показала преимущество в снижении рецидива на 35% при немышечно-инвазивном заболевании.[101] Лекарства, которые можно использовать для этой цели: митомицин С (MMC), эпирубицин, пирарубицин и гемцитабин. Инстилляцию послеоперационной химиотерапии следует проводить в течение первых нескольких часов после ТУР. Известно, что со временем остаточные опухолевые клетки прочно прилипают и покрываются внеклеточным матриксом, что снижает эффективность инстилляции.[100] Наиболее частый побочный эффект - химический цистит и раздражение кожи.[101] Если есть подозрение на перфорацию мочевого пузыря во время ТУР, химиотерапию не следует вводить в мочевой пузырь, поскольку известно, что серьезные побочные эффекты возникают из-за экстравазации лекарственного средства. Исследования показали, что эффективность химиотерапии повышается при использовании химиотерапии с помощью устройства.[102] Эти технологии используют различные механизмы для облегчения всасывания и действия химиотерапевтического препарата, введенного непосредственно в мочевой пузырь. Другая технология - электродвижущее лекарственное средство (EMDA) - использует электрический ток для увеличения абсорбции лекарственного средства после хирургического удаления опухоли.[103][104] Другая технология, термотерапия, использует радиочастотную энергию для прямого нагрева стенки мочевого пузыря, что вместе с химиотерапией (химиогипертермией) проявляет синергетический эффект, усиливая способность друг друга уничтожать опухолевые клетки.[105]
Иммунотерапия
Иммунотерапия к Бациллы Кальметта – Герена (BCG ) доставка в мочевой пузырь также используется для лечения и предотвращения рецидивов NMIBC.[106] БЦЖ - это вакцина против туберкулез приготовленный из аттенуированной (ослабленной) живой палочки туберкулеза крупного рогатого скота, Mycobacterium bovis, который потерял вирулентность в людях. BCG иммунотерапия эффективен в 2/3 случаев на данном этапе, а в рандомизированные испытания было показано, что превосходит стандартные химиотерапия.[107] Точный механизм, с помощью которого БЦЖ предотвращает рецидив, неизвестен. Однако было показано, что бактерии поглощаются раковыми клетками.[108] Инфекция этих клеток в мочевом пузыре может вызвать локализованную иммунную реакцию, которая очищает остаточные раковые клетки.[109][110]
BCG проводится как вводный курс, так и курс обслуживания. Индукционный курс состоит из 6-недельного курса внутрипузырной и чрескожной БЦЖ.[111] Затем следует курс обслуживания. Нет единого мнения относительно графика технического обслуживания, однако наиболее распространенным является график Юго-западной онкологической группы (SWOG).[112] График обслуживания SWOG состоит из внутрипузырного и чрескожного введения. BCG каждую неделю в течение 3 недель в 3, 6, 12, 18, 24, 30 и 36 месяцев.[111] Трехнедельный поддерживающий режим с индукцией продемонстрировал частоту полного ответа на уровне 84% по сравнению с 69% у людей, получавших 6-недельную индукцию. BCG только в 6 месяцев. Во многих исследованиях изучались альтернативные схемы лечения и режимы BCG но не показал клинического значения.[111] Эффективность различных штаммов BCG (Connaught, TICE, Pasteur, Tokio-172), как было показано, не отличается, однако нет доказательств высокого уровня.[113]
Побочные эффекты терапии БЦЖ включают: цистит, простатит, эпидидимоорхит, баланит, обструкция мочеточника, сокращение мочевого пузыря, микобактериальные остеомиелит, реактивный артрит, микобактериальная пневмония, гранулематозный гепатит, гранулематозный нефрит, интерстициальный нефрит, инфекционный васкулит и диссеминированная инфекция.[114][115]
Местная инфекция (т.е. простатит, эпидидимоорхит, баланит ) из-за БЦЖ следует лечить тройной туберкулезной терапией, при этом один из препаратов фторхинолон от 3 до 6 месяцев. Людям с системными инфекциями следует прекратить терапию БЦЖ и начать противотуберкулезное лечение множественными препаратами в течение не менее 6 месяцев. Для этого лечения можно использовать следующие лекарства: INH, рифампицин, этамбутол, фторхинолоны, кларитромицин, аминогликозиды, и доксициклин. Штаммы БЦЖ не чувствительны к пиразинамид поэтому он не должен быть частью противотуберкулезного лечения.[116]
Неудача лечения БЦЖ
Неэффективность лечения БЦЖ можно разделить на 3 группы; Рецидив БЦЖ, резистентность к БЦЖ и непереносимость БЦЖ. При рецидиве БЦЖ опухоль рецидивирует после периода без болезни. БЦЖ-резистентные опухоли - это опухоли, которые не реагируют на индукционные и поддерживающие дозы БЦЖ или прогрессируют во время терапии. При непереносимости БЦЖ опухоль рецидивирует из-за неполного лечения, поскольку человек, получающий ее, не может переносить индукционный курс БЦЖ. Около 50% людей не проходят курс лечения БЦЖ и нуждаются в дальнейшем лечении.[111]
Людям, у которых опухоли рецидивировали после лечения БЦЖ или которые не ответили на лечение, лечить труднее.[117] В таких людях радикальная цистэктомия это рекомендация[118][119] У людей, которые не реагируют на терапию БЦЖ и не подходят или не хотят ее проходить. радикальная цистэктомия, можно рассмотреть спасательные методы лечения. Спасательная терапия включает внутрипузырную химиотерапию с такими агентами, как валрубицин, гемцитабин или доцетаксел, химиолучевая или химиогипертермия.[120]
| Риск | Прочие соображения | Химиотерапия | Иммунотерапия (БЦЖ) | Цистоскопия (наблюдение) | Визуализация (наблюдение) |
|---|---|---|---|---|---|
| Низкий | через 3 месяца с последующей цистоскопией через 12 месяцев, затем ежегодно в течение 5 лет | КТ / МРТ урография и КТ / МРТ брюшной полости и таза на исходном уровне | |||
| Средний | Первичная опухоль с историей химиотерапии | Внутрипузырная химиотерапия в течение 1 года ИЛИ Внутрипузырная БЦЖ в течение 1 года (предпочтительно) | через 3 месяца с цитологией, затем один раз в 3–6 месяцев в течение 5 лет, а затем ежегодно | КТ / МРТ урография и КТ / МРТ брюшной полости и таза на исходном уровне | |
| Рецидивирующие опухоли с предшествующей химиотерапией в анамнезе | Внутрипузырная БЦЖ на 1 год | ||||
| Высоко | Внутрипузырная БЦЖ в течение 3 лет (по переносимости) | через 3 месяца с цитологическим исследованием, затем каждые 3 месяца в течение 2 лет, после этого, 6 месяцев в течение 5 лет, затем ежегодно | КТ / МРТ урография и КТ / МРТ брюшной полости и таза на исходном уровне, КТ / МР-урография 1-2 раза в год в течение 10 лет | ||
| T1G3 / Высокая степень, лимфоваскулярная инвазия, наличие вариантной гистологии | Рассмотрите возможность радикальной цистэктомии | ||||
Мышечный инвазивный

Мультимодальная терапия (стандартное лечение)
Необработанные, неинвазивные опухоли в мышцах могут постепенно начать проникать в мышечную стенку мочевого пузыря (мышечно-инвазивный рак мочевого пузыря). Опухоли, которые проникают в стенку мочевого пузыря, требуют более радикального хирургического вмешательства, когда часть (частичная цистэктомия ) или все (радикальная цистэктомия ) мочевого пузыря удаляется (цистэктомия), и поток мочи направляется в изолированную петлю кишечника (так называемый подвздошный канал или уростома ). В некоторых случаях опытные хирурги могут создать замену мочевого пузыря ( новый пузырь ) из сегмента кишечной ткани, но это во многом зависит от предпочтений человека, возраста человека, почечная функция, и место болезни. Двусторонняя тазовая лимфаденэктомия должна сопровождаться радикальной цистэктомией. Как минимум, стандартный шаблон лимфаденэктомия следует удалить внешний и внутренняя подвздошная кость и запирательный лимфатический узел.[121] Радикальная цистэктомия сопряжена с серьезными осложнениями. Около 50-65% людей испытывают осложнения в течение 90 дней после операции.[122][123] Летальность составила 7% в течение 90 дней после операции. Центры с большим объемом имеют лучшие результаты, чем центры с низким объемом.[124] Некоторые центры внедряют рекомендации общества «Улучшенное восстановление после операции» (ERAS) по снижению заболеваемости после радикальной цистэктомии. Однако из-за отсутствия конкретных доказательств в урологической хирургии протокол ERAS не получил широкого распространения в урологической клинической помощи.[125]
Даже после хирургического удаления мочевого пузыря у 50% людей с мышечно-инвазивным заболеванием (T2-T4) в течение двух лет развиваются метастазы из-за микрометастазов.[126] В таком, неоадъювантная химиотерапия (химиотерапия перед основным лечением, т. е. хирургическим вмешательством) показала увеличение общей выживаемости через 5 лет с 45% до 50% с абсолютным преимуществом выживаемости на 5%.[127][128][129] В настоящее время два наиболее используемых режима химиотерапии для неоадъювантной химиотерапии основаны на платине; метотрексат, винбластин, доксорубицин, цисплатин (MVAC) и гемцитабин с цисплатин (GC).[130] Другие схемы включают плотные дозы MVAC (DDMVC) и цисплатин, метотрексат и винбластин (CMV). Хотя оптимальный режим не установлен, предпочтительным режимом для неоадъювантной терапии является MVAC.[130]
Роль адъювантной химиотерапии (химиотерапия после основного лечения) ограничена людьми с опухолями высокой степени злокачественности (pT3 / T4 и / или N +), которые не получали неоадъювантную терапию.[121] Адъювантная лучевая терапия не показала никаких преимуществ при лечении рака мочевого пузыря.[131]
| MVAC | DDMVAC | Гемцитабин + цисплатин |
|---|---|---|
| Метотрексат (30 мг / м2 IV) - день 1,15,22 Винбластин (3 мг / м2 IV) - 2, 15, 22 день Доксорубицин (30 мг / м2 IV) - день 2 Цисплатин (70 мг / м2 IV) - день 2 Повторять каждые 4 недели 3 цикла | Метотрексат (30 мг / м2 IV) - день 1 Винбластин (3 мг / м2 IV) - день 2 Доксорубицин (30 мг / м2 IV) - день 2 Цисплатин (70 мг / м2 IV) - день 2 Колониестимулирующий фактор гранулоцитов (Г-КСФ) (240 мкг / м2 SC) - день 4-10 Повторяйте каждые 2 недели 3–4 цикла. | Гемцитабин (1000 мг / м2 IV) - 1,8,15 день Цисплатин (70 мг / м2) - день 2 Повторяйте каждые 4 недели в течение 4 циклов. |
Тримодальная терапия (альтернативное лечение)
Сочетание радиация и химиотерапия (химиолучевая терапия) в сочетании с трансуретральной (эндоскопической) резекцией опухоли мочевого пузыря может использоваться как альтернатива у некоторых людей.[134] Обзор доступных больших серий данных об этой так называемой тримодальной терапии показал аналогичные показатели долгосрочной специфической выживаемости при раке с улучшенным общим качеством жизни, как у людей, перенесших радикальную цистэктомию с реконструкцией мочи. Однако в настоящее время отсутствуют рандомизированные контрольные исследования, в которых сравнивалась бы тримодальная терапия с радикальной цистэктомией. Люди, которые проходят тримодальную терапию, обычно тщательно отбираются и обычно имеют заболевание Т2 без гидронефроза и / или карциномы in-situ.[135] Пятилетняя специфическая выживаемость при раке и общая выживаемость после тримодальной терапии составляет от 50% до 82% и от 36% до 74%.[134]
При тримодальной терапии проводят максимальную ТУРМТ с последующей химиолучевой терапией. Используются схемы химиотерапии, повышающие чувствительность к облучению, состоящие из цисплатина или 5-флуроурацила и митомицина С. Радиационная терапия через внешнюю лучевую терапию фасолью (EBRT ) с целевой лечебной дозой 64-66 Гр.[136] Наблюдение за прогрессированием или рецидивом должно проводиться с помощью Компьютерная томография, цистоскопия и цитология мочи.[121] Побочные эффекты химиолучевой терапии включают: тошнота, рвота, потеря аппетита, выпадение волос, язвы во рту, понос, запор, повышенный риск инфекций и кровотечение и усталость.[137]
У людей, у которых тримодальная терапия неэффективна, радикальная цистэктомия рассматривается при наличии инвазивных или рецидивирующих опухолей в мышцах. Примерно 25-30% пациентов не проходят лечение и подвергаются радикальной цистэктомии.[134] ТУРМТ с внутрипузырной терапией показана после неудачного лечения немышечно-инвазивного заболевания.[121]
Частичная цистэктомия
У людей с единственной опухолью без сопутствующей карциномы in situ в области, где могут быть достигнуты чистые хирургические границы, выполняется частичная цистэктомия с лимфаденэктомия можно считать. План управления, включая частичная цистэктомия должен сопровождаться неоадъювантный химиотерапия.[96] У людей с урахальной аденокарциномой мочевого пузыря частичная цистэктомия с в блоке резекция урахальная связка и пупок можно рассмотреть.[10]
Метастатическое заболевание
Лечение первой линии
Цисплатин -содержащая комбинированная химиотерапия является стандартом лечения метастатического мочевого пузыря.[138] Пригодность к химиотерапии на основе цисплатина оценивается до начала лечения. Человек считается непригодным, если верно хоть одно из следующих утверждений.[139]
- Статус работы Восточной кооперативной онкологической группы 2
- Клиренс креатинина <60 мл / мин
- Потеря слуха степени ≥ 2
- Оценка ≥ 2 невропатия
- Сердечная недостаточность класса III по Нью-Йоркской кардиологической ассоциации
Люди, которые считаются подходящими, получают схемы на основе платины; метотрексат, винбластин, доксорубицин, с цисплатином (MVAC) или гемцитабин с цисплатином (ГК). Альтернативные схемы включают: паклитаксел с гемцитабином и цисплатином (PCG, тройная терапия) и цисплатином, метотрексатом и винбластином (CMV). Частота ответа на комбинацию на основе цисплатина колеблется от 39 до 65%, а полный ответ наблюдается у 12-35 человек.[140] MVAC лучше переносится, если он сочетается с колониестимулирующий фактор гранулоцитов и режим известен как режим плотной дозы MVAC (DDMVAC). Эта комбинация снижает смертность от всех причин.[141] Режим MVAC агрессивен. Фебрильная нейтропения (лихорадка из-за уменьшения лейкоцитов) встречается у 10-14%, а смерть из-за токсичности - примерно в 3-4%. Общие побочные эффекты MVAC включают подавление Костный мозг, лихорадка из-за снижения лейкоцитов, сепсис, мукозит, и тошнота и рвота.[140] Напротив, режим ГК показал более низкие показатели нейтропенический сепсис и 3/4 класс мукозит по сравнению с MVAC.[142] Были предприняты попытки повысить переносимость схемы на основе цисплатина путем замены ее на карбоплатин химиотерапия на основе. Однако терапия на основе цисплатина превосходит карбоплатин химиотерапия для достижения общего и полного ответа.[143] Тем не менее, почти половина людей с метастазами «непригодны» для терапии на основе цисплатина. У таких людей сочетание карбоплатин и гемцитабин (GemCarbo) можно использовать в качестве первой линии химиотерапия.[144] У людей, которые не имеют права на получение платиновых химиотерапия и имеют PD-L1 выражение, Атезолизумаб и Пембролизумаб может быть использован.
Люди с метастазами в кости должны получать бисфосфонаты или деносумаб для предотвращения событий, связанных со скелетом (например, переломы, сдавление спинного мозга, боль в костях).[145]
| DDMVAC | Гемцитабин + Цисплатин |
|---|---|
| Метотрексат (30 мг / м2 IV) - день 1 Винбластин (3 мг / м2 IV) - день 2 Доксорубицин (30 мг / м2 IV) - день 2 Цисплатин (70 мг / м2 IV) - день 2 Колониестимулирующий фактор гранулоцитов (Г-КСФ) (240 мкг / м2 SC) - день 4-10 Повторяйте каждые 2 недели в течение 3-4 циклов. | Гемцитабин (1000 мг / м2 IV) - 1,8,15 день Цисплатин (70 мг / м2) - день 2 Повторяйте каждые 4 недели в течение 4 циклов. |
| Атезолизумаб (в PD-L1 +) | Гемцитабин + карбоплатин | Пембролизумаб (в составе PD-L1 +) |
|---|---|---|
| Атезолизумаб (атезолизумаб 1200 мг внутривенно) каждые 3 недели | Гемцитабин (1000 мг / м2 IV) - 1,8 день Карбоплатин (4,5 × [скорость клубочковой фильтрации + 25]) - день 1 и каждые 3 недели | Пембролизумаб 200 мг каждые 3 недели |
Лечение второй линии
Рефрактерный рак мочевого пузыря или его прогрессирование после химиотерапии на основе платины можно лечить с помощью химиотерапии второй линии или иммунотерапии.
Наиболее часто используемая химиотерапия второй линии - это режимы монотерапии. Таксаны (Паклитаксел, наб-паклитаксел и Доцетаксел ). Другие режимы с одним агентом включают: Винфлунин, третье поколение алкалоид барвинка (одобрено в Европе), Гемцитабин, Пеметрексед, Оксалиплатин, и Ифосфамид.[146][147][148] Побочные эффекты Винфлунин включают нейтропения, запор, усталость и анемия и ограничил его использование в качестве агента второй линии. Ответ на химиотерапию второй линии наблюдается у 5–20% людей. Средняя выживаемость без прогрессирования заболевания при химиотерапии второй линии составляет 3-4 месяца.[149]
У людей с рецепторы фактора роста фибробластов (FGFR ) мутации и неэффективность стандартной химиотерапии на основе платины эрдафитиниб может быть использован. Эрдафитиниб показал ответ 40% у этих пациентов.[150] В США разрешено использовать пять иммунотерапевтических агентов для лечения метастатического рака мочевого пузыря. Они действуют, подавляя белок запрограммированной гибели клеток 1 (PD-1) или лиганд запрограммированной гибели клеток 1 (PD-L1). Пембролизумаб и ниволумаб, и являются ингибиторами лиганд запрограммированной гибели клеток 1 (PD-1). Авелумаб, атезолизумаб и дурвалумаб являются ингибиторами PD-L1.[151][152]
| Атезолизумаб | Ниволумаб | Пембролизумаб | Дурвалумаб | Авелумаб |
|---|---|---|---|---|
| Атезолизумаб 1200 мг в / в каждые 3 недели | Ниволумаб 3 мг / кг в / в каждые 2 недели | Пембролизумаб 200 мг каждые 3 недели | Дурвалумаб 10 мг / кг каждые 2 недели в течение 12 месяцев | Авелумаб 10 мг / кг в / в каждые 2 недели |
Наблюдение и ответ
Контраст повышен CT используется для контроля метастазов в легких, печени и лимфатических узлах. А рентген используется для обнаружения и мониторинга метастазов в кости.[153] Ответ на лечение измеряется с использованием критериев оценки ответа в солидных опухолях (RECIST ) в одну из следующих групп; ответ (полный или частичный), стабильное заболевание и прогрессирующее заболевание.[154]
Прогноз
Люди с неинвазивными мышечными опухолями имеют благоприятный исход (5-летняя выживаемость составляет 95% против 69% при мышечно-инвазивном раке мочевого пузыря).[155][156] Однако у 70% из них будет рецидив после начального лечения, а у 30% из них будет инвазивное заболевание мышц.[157] Рецидив и переход к более высокой стадии заболевания имеют менее благоприятный исход.[158]
Выживание после радикальная цистэктомия и таз лимфатический узел рассечение зависит от патологической стадии. Если болезнь не распространилась на лимфатический узел и ограничивается мочевой пузырь (T1 или T2, N0) 5-летняя выживаемость составляет 78%. Если он распространился локально по области мочевого пузыря без лимфатический узел вовлечены (T3, N0), то 5-летняя выживаемость падает до 47%. При заболевании с распространением лимфатических узлов (N +, независимо от стадии T) 5-летняя выживаемость составляет 31%. Местнораспространенное и метастатическое заболевание резко снижает выживаемость, при этом средняя выживаемость без химиотерапии составляет 3–6 месяцев. Цисплатин химиотерапия на основе химиотерапии увеличила среднюю выживаемость до 15 месяцев. Однако 5-летняя выживаемость все еще составляет 15%.[159]
Существует несколько прогностических факторов, которые определяют выживаемость при раке после радикальной цистэктомии. Факторами, отрицательно влияющими на выживаемость рака, являются пожилой возраст, более высокая степень опухоли и патологическая стадия, лимфатический узел метастаз, присутствие лимфоваскулярная инвазия и положительный край мягких тканей.[160] Плотность лимфатических узлов (положительные лимфатические узлы / всего лимфатический узел наблюдается в образце после операции) является предиктором выживаемости при поражении лимфатических узлов. Чем выше плотность, тем ниже выживаемость.[161]
Качество жизни
После радикальной цистэктомии мочевыделительная и сексуальная функция остаются хуже, чем у населения в целом. Люди с неоцистическим мочевым пузырем обладают лучшими эмоциональными функциями и внешним видом тела по сравнению с людьми с кожным отводом (которым необходимо носить мешок для сбора мочи через живот).[162] Социальные факторы, такие как семья, отношения, здоровье и финансы, в значительной степени определяют хорошее качество жизни людей, у которых был диагностирован рак мочевого пузыря.[163]
У большого процента людей с раком мочевого пузыря беспокойство и депрессия.[164] Молодые, одинокие люди с запущенным клиническим заболеванием имеют высокий риск получить диагноз психического заболевания после лечения. Люди, которые после лечения страдают психическим заболеванием, имеют худшую выживаемость в отношении рака и общую выживаемость.[165][166]
Эпидемиология
| Классифицировать | Страна | Общий | Мужчины | Женщины |
|---|---|---|---|---|
| 1 | Ливан | 25 | 40 | 9 |
| 2 | Греция | 21 | 40 | 4 |
| 3 | Дания | 18 | 29 | 8 |
| 4 | Венгрия | 17 | 27 | 9 |
| 5 | Албания | 16 | 27 | 6 |
| 5 | Нидерланды | 16 | 26 | 8 |
| 7 | Бельгия | 16 | 27 | 6 |
| 8 | Италия | 15 | 27 | 6 |
| 9 | Германия | 15 | 26 | 6 |
| 10 | Испания | 15 | 27 | 6 |

Во всем мире в 2017 году рак мочевого пузыря привел к 196000 смертей, что составляет 5,4% (с поправкой на возраст ) уменьшение по сравнению с 2007 годом.[170] В 2018 году скорректированные по возрасту показатели новых случаев рака мочевого пузыря составили 6 случаев на 100000 человек и с поправкой на возраст коэффициент смертности составил 2 смерти на 100 000 человек. Ливан и Греция имеют самый высокий уровень новых случаев. В Ливан, этот высокий риск связан с большим количеством курильщиков и нефтехимический загрязнение воздуха.[171]
Риск возникновения рака мочевого пузыря у мужчин в четыре раза выше, чем у женщин.[3] Курение может лишь частично объяснить этот более высокий уровень у мужчин в западном полушарии.[172] Еще одна причина в том, что рецептор андрогенов, который гораздо активнее у мужчин, чем у женщин, может играть определенную роль в развитии рака.[173] Эта гипотеза также подтверждается тем фактом, что мужчины, проходящие супрессивную терапию андрогенами по несвязанной причине, имеют более низкий риск развития рака мочевого пузыря.[174] В Африка, мужчины более склонны к полевым работам и подвержены заражению Шистосома, это может до некоторой степени объяснить разрыв в заболеваемости плоскоклеточным раком в регионах, где рак мочевого пузыря является эндемическим.[172] Однако у женщин более агрессивное заболевание и худшие результаты, чем у мужчин. Эта разница в результатах объясняется многочисленными факторами, такими как различие в воздействии канцерогенов, генетика, социальная и качественная помощь.[47] Одним из распространенных признаков рака мочевого пузыря является гематурия, который довольно часто ошибочно диагностируется как инфекция мочевыводящих путей у женщин, что приводит к задержке постановки диагноза.[47] Более того, как упоминалось ранее Ген PSCA может играть роль в агрессивных опухолях у женщин.
Канада
Рак мочевого пузыря является шестым по распространенности раком, на который приходится 3,7% новых случаев рака. в 2018 году 30700 канадцев жили с раком мочевого пузыря, было диагностировано 9160 новых случаев, 2467 умерли от него.[175] По оценкам, в 2019 году будет диагностировано 11800 новых случаев заболевания, и 2500 человек умрут от этого.[176] Из 11 800 новых случаев 9100 будут у мужчин и 2700 - у женщин. Из 2500 человек, которые умрут от этого, 1800 мужчин и 700 женщин.[176]
Китай
Рак мочевого пузыря занимает 14-е место по распространенности и 16-е место среди причин смерти от рака. В 2018 году на его долю пришлось 82,3 тысячи новых случаев заболевания и 38,2 тысячи смертей.[177] Количество новых случаев сравнительно ниже по сравнению с западными аналогами. У большинства людей диагностировано немышечно-инвазивное заболевание (75%), а у остальных - мышечно-инвазивное заболевание (25%). Карцинома in situ присутствовала только в 2,4% случаев.[178]
Европа
В 2015 году в Европейском союзе было диагностировано 131 000 новостных случаев, из которых 40 000 умерли. Это 5-й по частоте рак и 9-й по частоте причиной смерти от рака. Относительная 5-летняя выживаемость для рака мочевого пузыря, диагностированного между 2000 и 2007 годами, составляет 69%. Географические различия наблюдаются в показателях выживаемости: 5-летняя выживаемость составляет от 75% в Северной и 65% в Восточной Европе.[179]
Великобритания
Рак мочевого пузыря является девятым по распространенности раком в Великобритания на них приходится 2,7% всех новых случаев рака. В 2018 году было зарегистрировано 12 200 новых случаев заболевания, от которых умерли 6100 человек.[180]
НАС
в Соединенные Штаты в 2019 году ожидается 80 470 случаев заболевания и 17 670 смертей, что сделает его шестым по распространенности типом рака в регионе.[2] Рак мочевого пузыря - четвертый по распространенности тип рака у мужчин и двенадцатый по частоте у женщин.[181] В 2019 году около 62000 мужчин и 19000 женщин заболели раком мочевого пузыря.[182] В период с 2012 по 2016 год ежегодный уровень новых случаев рака мочевого пузыря снижался на один процент в год.[183]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я j k л м п «Лечение рака мочевого пузыря (PDQ®) - версия для пациентов - Национальный институт рака». www.cancer.gov. 11 мая 2020. Получено 4 июн 2020.
- ^ а б c d е ж "Рак мочевого пузыря - статистика рака". ВИДЯЩИЙ. Получено 30 октября 2019.
- ^ а б c d е ж «Информационный бюллетень по раку мочевого пузыря» (PDF). Глобальная обсерватория рака. Получено 8 ноября 2019.
- ^ «Лечение рака мочевого пузыря». Национальный институт рака. 5 июня 2017. В архиве из оригинала 14 июля 2017 г.. Получено 18 июля 2017.
- ^ «Рекомендации ЕАУ: немышечно-инвазивный рак мочевого пузыря». Uroweb.
- ^ «Рак мочевого пузыря - стадии и степени». Cancer.Net. 25 июня 2012 г.
- ^ "Рак мочевого пузыря". Всемирный фонд исследования рака. 24 апреля 2018.
- ^ «Статистика выживаемости при раке мочевого пузыря - Канадское онкологическое общество». www.cancer.ca.
- ^ Авеллино Дж. Дж., Бозе С., Ван Д. С. (июнь 2016 г.). «Диагностика и лечение гематурии». Хирургические клиники Северной Америки. 96 (3): 503–15. Дои:10.1016 / j.suc.2016.02.007. PMID 27261791.
- ^ а б Klaile Y, Schlack K, Boegemann M, Steinestel J, Schrader AJ, Krabbe LM (октябрь 2016 г.). «Вариант гистологии рака мочевого пузыря: как он должен изменить лечение немышечно-инвазивных и мышечно-инвазивных заболеваний?». Трансляционная андрология и урология. 5 (5): 692–701. Дои:10.21037 / тау.2016.06.13. ЧВК 5071184. PMID 27785426.
- ^ Клиническая онкология Абелова. Нидерхубер, Джон Э., Армитаж, Джеймс О., 1946-, Дорошоу, Джеймс Х., Кастан, МБ (Майкл Б.), Теппер, Джоэл Э., Предшественник: Абелофф, Мартин Д. (шестой ред.). Филадельфия, Пенсильвания. 8 января 2019. с. 1388. ISBN 978-0-323-56815-9. OCLC 1089396489.CS1 maint: другие (ссылка на сайт)
- ^ Ходжес, Стефани С.; Холт, Гарри Р .; Деджордж, Кэтрин С.(15 октября 2017 г.). «Рак мочевого пузыря: диагностика и лечение». Американский семейный врач. 96 (8): 507–514. PMID 29094888.
- ^ Зигерс, член парламента, Тан Ф., Дорант Э., ван ден Брандт, Пенсильвания (август 2000 г.). «Влияние характеристик курения сигарет на риск рака мочевыводящих путей: метаанализ эпидемиологических исследований». Рак. 89 (3): 630–9. Дои:10.1002 / 1097-0142 (20000801) 89: 3 <630 :: AID-CNCR19> 3.0.CO; 2-Q. PMID 10931463.
- ^ а б van Osch FH, Jochems SH, van Schooten FJ, Bryan RT, Zeegers MP (июнь 2016 г.). «Количественная связь между воздействием табакокурения и риском рака мочевого пузыря: метаанализ 89 обсервационных исследований». Международный журнал эпидемиологии. 45 (3): 857–70. Дои:10.1093 / ije / dyw044. PMID 27097748.
- ^ Letašiová S, Medve'ová A, Šovčíková A, Dušinská M, Volkovová K, Mosoiu C, Bartonová A (июнь 2012 г.). «Рак мочевого пузыря, обзор факторов риска окружающей среды». Состояние окружающей среды. 11 Приложение 1: S11. Дои:10.1186 / 1476-069X-11-S1-S11. ЧВК 3388449. PMID 22759493.
- ^ Brennan P, Bogillot O, Cordier S, Greiser E, Schill W., Vineis P, et al. (Апрель 2000 г.). «Курение сигарет и рак мочевого пузыря у мужчин: объединенный анализ 11 исследований случай-контроль». Международный журнал рака. 86 (2): 289–94. Дои:10.1002 / (sici) 1097-0215 (20000415) 86: 2 <289 :: aid-ijc21> 3.0.co; 2-m. PMID 10738259.
- ^ Ян Х, Ин И, Се Х, Ли Дж, Ван Х, Хе Л. и др. (2018). «Пассивное курение увеличивает риск рака мочевого пузыря у некурящих: метаанализ». Лечение рака и исследования. 10: 3781–3791. Дои:10.2147 / CMAR.S175062. ЧВК 6159806. PMID 30288109.
- ^ «Риск для здоровья от пассивного курения». www.cancer.org. Получено 21 ноября 2019.
- ^ Афшари М., Джанбабаей Г., Бахрами М.А., Мусазаде М. (2017). «Опиум и рак мочевого пузыря: систематический обзор и метаанализ отношения шансов употребления опия и риска рака мочевого пузыря». PLOS ONE. 12 (6): e0178527. Bibcode:2017PLoSO..1278527A. Дои:10.1371 / journal.pone.0178527. ЧВК 5460843. PMID 28586371.
- ^ Рабочая группа МАИР по оценке канцерогенного риска для человека (2012 г.). 4-AMINOBIPHENYL. Международное агентство по изучению рака.
- ^ Сен-Жак Н., Паркер Л., Браун П., Даммер Т. Дж. (Июнь 2014 г.). «Мышьяк в питьевой воде и раковые заболевания мочевыводящих путей: систематический обзор эпидемиологических данных за 30 лет». Состояние окружающей среды. 13: 44. Дои:10.1186 / 1476-069X-13-44. ЧВК 4088919. PMID 24889821.
- ^ Clin B, Pairon JC (ноябрь 2014 г.). «Медицинское наблюдение за рабочими, подвергшимися воздействию канцерогенов мочевого пузыря: французское прагматическое заявление, основанное на фактах». BMC Public Health. 14: 1155. Дои:10.1186/1471-2458-14-1155. ЧВК 4230399. PMID 25377503.
- ^ Рабочая группа МАИР по оценке канцерогенного риска для человека (2012 г.). ХЛОРНАФАЗИН. Международное агентство по изучению рака.
- ^ Люди, Рабочая группа МАИР по оценке канцерогенного риска (2012 г.). 2-НАФТИЛАМИН. Международное агентство по изучению рака.
- ^ Реулен Р.К., Келлен Э., Бантинкс Ф., Бринкман М., Зигерс депутат (сентябрь 2008 г.). «Мета-анализ связи между раком мочевого пузыря и профессией». Скандинавский журнал урологии и нефрологии. Дополнение. 42 (218): 64–78. Дои:10.1080/03008880802325192. PMID 18815919. S2CID 30510231.
- ^ Гуха Н., Стинланд Н.К., Мерлетти Ф., Алтьери А., Коглиано В., Стрейф К. (август 2010 г.). «Риск рака мочевого пузыря у художников: метаанализ». Медицина труда и окружающей среды. 67 (8): 568–73. Дои:10.1136 / oem.2009.051565. PMID 20647380.
- ^ Харлинг М., Шаблон А., Шедльбауэр Г., Дюлон М., Ниенхаус А. (май 2010 г.). «Рак мочевого пузыря у парикмахеров: метаанализ». Медицина труда и окружающей среды. 67 (5): 351–8. Дои:10.1136 / oem.2009.050195. ЧВК 2981018. PMID 20447989.
- ^ Мостафа М.Х., Шевейта С.А., О'Коннор П.Дж. (январь 1999 г.). «Связь между шистосомозом и раком мочевого пузыря». Обзоры клинической микробиологии. 12 (1): 97–111. Дои:10.1128 / CMR.12.1.97. ЧВК 88908. PMID 9880476.
- ^ Заглул М.С. (декабрь 2012 г.). «Рак мочевого пузыря и шистосомоз». Журнал Египетского национального института рака. 24 (4): 151–9. Дои:10.1016 / j.jnci.2012.08.002. PMID 23159285.
- ^ Мостафа М.Х., Хельми С., Бадави А.Ф., Трикер А.Р., Шпигельхалдер Б., Преуссманн Р. (апрель 1994 г.). «Нитраты, нитриты и летучие N-нитрозосоединения в моче пациентов, инфицированных Schistosoma haematobium и Schistosoma mansoni». Канцерогенез. 15 (4): 619–25. Дои:10.1093 / carcin / 15.4.619. PMID 8149471.
- ^ Бадави А.Ф. (август 1996 г.). «Молекулярные и генетические события при раке мочевого пузыря человека, ассоциированном с шистосомозом: роль онкогенов и генов-супрессоров опухолей». Письма о раке. 105 (2): 123–38. Дои:10.1016 / 0304-3835 (96) 04284-х. PMID 8697435.
- ^ Чаудхари К.С., Лу К.Л., Абель П.Д., Кхандан-Ниа Н., Шома А.М., эль-Баз М. и др. (Январь 1997 г.). «Экспрессия онкопротеинов bcl-2 и p53 в связанной с шистосомозом переходной и плоскоклеточной карциноме мочевого пузыря». Британский журнал урологии. 79 (1): 78–84. Дои:10.1046 / j.1464-410x.1997.30717.x. PMID 9043502.
- ^ Шокейр А.А. (январь 2004 г.). «Плоскоклеточный рак мочевого пузыря: патология, диагностика и лечение». BJU International. 93 (2): 216–20. Дои:10.1111 / j.1464-410x.2004.04588.x. PMID 14690486. S2CID 10487371.
- ^ Monach PA, Арнольд Л.М., Меркель PA (январь 2010 г.). «Частота и профилактика токсичности мочевого пузыря от циклофосфамида при лечении ревматических заболеваний: обзор, основанный на данных». Артрит и ревматизм. 62 (1): 9–21. Дои:10.1002 / арт.25061. PMID 20039416.
- ^ Ян Х.Й., Чен ПК, Ван Дж.Д. (2014). «Китайские травы, содержащие аристолоховую кислоту, связанные с почечной недостаточностью и уротелиальной карциномой: обзор эпидемиологических наблюдений и причинно-следственных связей». BioMed Research International. 2014: 569325. Дои:10.1155/2014/569325. ЧВК 4241283. PMID 25431765.
- ^ Суриано Ф, Альтобелли Э, Серги Ф, Бускарини М (2013). «Рак мочевого пузыря после лучевой терапии рака простаты». Отзывы в урологии. 15 (3): 108–12. ЧВК 3821989. PMID 24223022.
- ^ Сунь Дж.В., Чжао Л.Г., Ян Й, Ма Х, Ван Й.Й, Сян Ю.Б. (24 марта 2015 г.). «Ожирение и риск рака мочевого пузыря: метаанализ доза-эффект 15 когортных исследований». PLOS ONE. 10 (3): e0119313. Bibcode:2015PLoSO..1019313S. Дои:10.1371 / journal.pone.0119313. ЧВК 4372289. PMID 25803438.
- ^ Аль-Залабани А.Х., Стюарт К.Ф., Весселиус А., Схолс А.М., Зигерс депутат (сентябрь 2016 г.). «Модифицируемые факторы риска для профилактики рака мочевого пузыря: систематический обзор метаанализов». Европейский журнал эпидемиологии. 31 (9): 811–51. Дои:10.1007 / s10654-016-0138-6. ЧВК 5010611. PMID 27000312.
- ^ «Браузер по генетике рака». Cance.sanger.ac.uk. Получено 21 ноября 2019.
- ^ Онлайн-менделевское наследование в человеке (OMIM): 109800
- ^ Чжан Х, Чжан И (сентябрь 2015 г.). «Рак мочевого пузыря и генетические мутации». Биохимия клетки и биофизика. 73 (1): 65–9. Дои:10.1007 / s12013-015-0574-z. PMID 27352265. S2CID 14316154.
- ^ "Рак мочевого пузыря". Домашний справочник по генетике.
- ^ Ахмад И., Сансом О.Дж., Люн Х.Й. (май 2012 г.). «Изучение молекулярной генетики рака мочевого пузыря: уроки, извлеченные из мышиных моделей». Модели и механизмы заболеваний. 5 (3): 323–32. Дои:10.1242 / дмм.008888. ЧВК 3339826. PMID 22422829.
- ^ Хамфри PA, Moch H, Cubilla AL, Ulbright TM, Reuter VE (июль 2016 г.). «Классификация опухолей мочевыделительной системы и мужских половых органов, составленная ВОЗ 2016 г., часть B: опухоли предстательной железы и мочевого пузыря» (PDF). Европейская урология. 70 (1): 106–119. Дои:10.1016 / j.eururo.2016.02.028. PMID 26996659.
- ^ Энгель Л.С., Тайоли Э., Пфайфер Р., Гарсия-Клосас М., Маркус П.М., Лан К. и др. (Июль 2002 г.). «Объединенный анализ и мета-анализ глутатион-S-трансферазы M1 и рака мочевого пузыря: обзор HuGE». Американский журнал эпидемиологии. 156 (2): 95–109. Дои:10.1093 / aje / kwf018. PMID 12117698.
- ^ а б c «Отчет о раке мочевого пузыря» (PDF). Всемирный фонд исследования рака: Международный. Получено 9 ноября 2019.
- ^ а б c Marks P, Soave A, Shariat SF, Fajkovic H, Fisch M, Rink M (октябрь 2016 г.). «Женщина с раком мочевого пузыря: в чем и почему разница?». Трансляционная андрология и урология. 5 (5): 668–682. Дои:10.21037 / тау.2016.03.22. ЧВК 5071204. PMID 27785424.
- ^ Чой В., Очоа А., МакКонки Д.Д., Айн М., Хёглунд М., Ким В.Й. и др. (Сентябрь 2017 г.). "Генетические изменения в молекулярных подтипах рака мочевого пузыря: иллюстрация в наборе данных Атласа генома рака". Европейская урология. 72 (3): 354–365. Дои:10.1016 / j.eururo.2017.03.010. ЧВК 5764190. PMID 28365159.
- ^ Чой В., Черняк Б., Очоа А., Су Х, Зифкер-Радтке А., Динни С., МакКонки DJ (июль 2014 г.). «Внутренние базальные и просветные подтипы мышечно-инвазивного рака мочевого пузыря». Обзоры природы. Урология. 11 (7): 400–10. Дои:10.1038 / nrurol.2014.129. PMID 24960601. S2CID 24723395.
- ^ «Рекомендации ЕАУ: Диагностика рака мочевого пузыря без инвазии в мышечный слой». Uroweb. Получено 12 ноября 2019.
- ^ а б «Рекомендации ЕАУ: диагностика мышечно-инвазивного и метастатического рака мочевого пузыря». Uroweb. Получено 12 ноября 2019.
- ^ а б c «Uroweb - Европейская ассоциация урологов (EAU)». Uroweb. Получено 7 ноября 2019.
- ^ «Лечение рака мочевого пузыря». Национальный институт рака. 8 мая 2020. Получено 4 июн 2020.
- ^ Лотан Й., Рёрборн К.Г. (январь 2003 г.). «Чувствительность и специфичность общедоступных онкомаркеров мочевого пузыря по сравнению с цитологией: результаты всестороннего обзора литературы и метаанализов». Урология. 61 (1): 109–18, обсуждение 118. Дои:10.1016 / S0090-4295 (02) 02136-2. PMID 12559279.
- ^ Шариат С.Ф., Карам Дж. А., Лотан Ю., Каракевич П. И. (2008). «Критическая оценка маркеров мочи для выявления и мониторинга рака мочевого пузыря». Отзывы в урологии. 10 (2): 120–35. ЧВК 2483317. PMID 18660854.
- ^ а б Чоу Р., Гор Дж. Л., Бакли Д., Фу Р., Густафсон К., Гриффин Дж. К. и др. (Декабрь 2015 г.). «Биомаркеры в моче для диагностики рака мочевого пузыря: систематический обзор и метаанализ». Анналы внутренней медицины. 163 (12): 922–31. Дои:10.7326 / M15-0997. PMID 26501851.
- ^ Сантони Дж., Морелли МБ, Амантини С., Баттелли Н. (2018). «Мочевые маркеры при раке мочевого пузыря: новая информация». Границы онкологии. 8: 362. Дои:10.3389 / fonc.2018.00362. ЧВК 6137202. PMID 30245975.
- ^ а б c Мияке М, Овари Т., Хори С., Накаи Ю., Фудзимото К. (2018). «Новые биомаркеры для диагностики и мониторинга уротелиальной карциномы». Исследования и отчеты в урологии. 10: 251–261. Дои:10.2147 / RRU.S173027. ЧВК 6299471. PMID 30588457.
- ^ а б Гудисон С., Россер С. Дж., Уркиди В. (апрель 2013 г.). «Выявление и мониторинг рака мочевого пузыря: оценка маркерных тестов мочи и крови». Молекулярная диагностика и терапия. 17 (2): 71–84. Дои:10.1007 / s40291-013-0023-х. ЧВК 3627848. PMID 23479428.
- ^ Здравоохранение, Центр приборов и радиологии (7 октября 2019 г.). «Тесты на основе нуклеиновых кислот». FDA.
- ^ Сория Ф., Дроллер М.Дж., Лотан Й., Гонтеро П., Д'Андреа Д., Густ К.М. и др. (Декабрь 2018 г.). «Обновленный каталог доступных биомаркеров в моче для наблюдения за немышечно-инвазивным раком мочевого пузыря». Всемирный журнал урологии. 36 (12): 1981–1995. Дои:10.1007 / s00345-018-2380-х. ЧВК 6280823. PMID 29931526.
- ^ а б c d Андреассен, Б. К .; Aagnes, B .; Gislefoss, R .; Андреассен, М .; Вальквист, Р. (2016). «Заболеваемость и выживаемость уротелиальной карциномы мочевого пузыря в Норвегии, 1981-2014 гг.». BMC Рак. 16 (1): 799. Дои:10.1186 / с12885-016-2832-х. ISSN 1471-2407. ЧВК 5064906. PMID 27737647.
- ^ а б c «Типы рака мочевого пузыря: ОКР и другие варианты». CancerCenter.com. Получено 10 августа 2018.
- ^ а б Амин МБ (июнь 2009 г.). «Гистологические варианты уротелиальной карциномы: диагностические, терапевтические и прогностические последствия». Современная патология. 22 Дополнение 2 (S2): S96 – S118. Дои:10.1038 / modpathol.2009.26. PMID 19494856.
- ^ Тан DH, Чанг СС (декабрь 2015 г.). «Лечение рака мочевого пузыря in situ: передовая практика и последние разработки». Терапевтические достижения в урологии. 7 (6): 351–64. Дои:10.1177/1756287215599694. ЧВК 4647140. PMID 26622320.
- ^ Чаласани В., Чин Дж. Л., Идзава Дж. И. (декабрь 2009 г.). «Гистологические варианты уротелиального рака мочевого пузыря и неуротелиальная гистология рака мочевого пузыря». Журнал Канадской урологической ассоциации. 3 (6 Прил. 4): S193-8. Дои:10.5489 / cuaj.1195. ЧВК 2792446. PMID 20019984.
- ^ Moschini M, D'Andrea D, Korn S, Irmak Y, Soria F, Compérat E, Shariat SF (ноябрь 2017 г.). «Характеристики и клиническое значение гистологических вариантов рака мочевого пузыря». Обзоры природы. Урология. 14 (11): 651–668. Дои:10.1038 / nrurol.2017.125. PMID 28895563. S2CID 6351401.
- ^ Уоррик Джи (октябрь 2017 г.). «Клиническая значимость гистологических вариантов рака мочевого пузыря». Журнал Национальной комплексной онкологической сети. 15 (10): 1268–1274. Дои:10.6004 / jnccn.2017.7027. PMID 28982751.
- ^ Venyo AK, Titi S (2014). «Саркоматоидный вариант уротелиальной карциномы (карциносаркома, веретено-клеточная карцинома): обзор литературы». ISRN Урология. 2014: 794563. Дои:10.1155/2014/794563. ЧВК 3920806. PMID 24587922.
- ^ «Варианты уротелиальной карциномы - Американская урологическая ассоциация». www.auanet.org.
- ^ «Рекомендации ЕАУ - СИСТЕМЫ СТАДИИ И КЛАССИФИКАЦИИ». Uroweb.
- ^ Магерс М.Дж., Лопес-Бельтран А., Монтирони Р., Уильямсон С.Р., Каймаклиотис Х.З., Ченг Л. (январь 2019 г.). «Стадия рака мочевого пузыря». Гистопатология. 74 (1): 112–134. Дои:10.1111 / his.13734. PMID 30565300.
- ^ а б «Рак мочевого пузыря: стадии и степени». Cancer.net. Утверждено редакционной коллегией Cancer.Net 05/2019
- ^ Shinagare AB, Ramaiya NH, Jagannathan JP, Fennessy FM, Taplin ME, Van den Abbeele AD (январь 2011 г.). «Метастатическая картина рака мочевого пузыря: корреляция с характеристиками первичной опухоли». AJR. Американский журнал рентгенологии. 196 (1): 117–22. Дои:10.2214 / AJR.10.5036. PMID 21178055.
- ^ а б Мао Ю., Хедгире С., Прапруттам Д., Харисингани М. (16 сентября 2014 г.). «Визуализация тазовых лимфатических узлов». Текущие отчеты о радиологии. 2 (11). Дои:10.1007 / s40134-014-0070-z.
- ^ Шанкар П.Р., Баркмайер Д., Хаджийски Л., Кохан Р.Х. (октябрь 2018 г.). «Наглядный обзор узловых метастазов рака мочевого пузыря». Трансляционная андрология и урология. 7 (5): 804–813. Дои:10.21037 / тау.2018.08.25. ЧВК 6212631. PMID 30456183.
- ^ "Как ставится рак мочевого пузыря?". Американское онкологическое общество. В архиве из оригинала от 3 ноября 2019 г. Последний медицинский обзор: 02.11.2019
- ^ «Показатели выживаемости при раке мочевого пузыря по стадиям». Американское онкологическое общество. В архиве из оригинала 13 октября 2015 г. Последний медицинский обзор: 26.02.2014
- ^ Сет П. Лернер. «Обзор диагностики и лечения немышечно-инвазивного рака мочевого пузыря» (PDF). Управление по контролю за продуктами и лекарствами. ODAC 14 сентября 2016 г.
- ^ Эпштейн Д.И., Амин МБ, Рейтер В.Р., Мостофи Ф.К. (декабрь 1998 г.). «Консенсусная классификация уротелиальных (переходно-клеточных) новообразований мочевого пузыря Всемирной организацией здравоохранения / Международным обществом урологической патологии. Конференция по консенсусу по мочевому пузырю». Американский журнал хирургической патологии. 22 (12): 1435–48. Дои:10.1097/00000478-199812000-00001. PMID 9850170.
- ^ Комперат Э.М., Бургер М., Гонтеро П., Мостафид А.Х., Палоу Дж., Рупрет М. и др. (Май 2019 г.). «Классификация уротелиальной карциномы и новая» Классификация опухолей мочевыделительной системы и мужских половых органов Всемирной организацией здравоохранения 2016 г."". Европейский фокус урологии. 5 (3): 457–466. Дои:10.1016 / j.euf.2018.01.003. PMID 29366854.
- ^ а б Чанг С.С., Бурджян С.А., Чоу Р., Кларк П.Е., Данешманд С., Конети Б.Р. и др. (Октябрь 2016 г.). «Диагностика и лечение немышечно-инвазивного рака мочевого пузыря: руководство AUA / SUO». Журнал урологии. 196 (4): 1021–9. Дои:10.1016 / j.juro.2016.06.049. PMID 27317986.
- ^ а б «Рак мочевого пузыря: руководство по неинвазивным мышечным заболеваниям - Американская урологическая ассоциация». www.auanet.org.
- ^ Соукуп В., Чапун О., Коэн Д., Эрнандес В., Бургер М., Комперат Е. и др. (Ноябрь 2018 г.). «Инструменты стратификации риска и прогностические модели при немышечно-инвазивном раке мочевого пузыря: критическая оценка Европейской ассоциации урологов Группы руководящих принципов немышечно-инвазивного рака мочевого пузыря». Европейский фокус урологии. 6 (3): 479–489. Дои:10.1016 / j.euf.2018.11.005. PMID 30470647.
- ^ Sylvester RJ, van der Meijden AP, Oosterlinck W., Witjes JA, Bouffioux C, Denis L, et al. (Март 2006 г.). «Прогнозирование рецидива и прогрессирования у отдельных пациентов с раком мочевого пузыря стадии Ta T1 с использованием таблиц риска EORTC: комбинированный анализ 2596 пациентов из семи исследований EORTC». Европейская урология. 49 (3): 466–5, обсуждение 475–7. Дои:10.1016 / j.eururo.2005.12.031. PMID 16442208.
- ^ Sylvester RJ, van der Meijden AP, Oosterlinck W., Witjes JA, Bouffioux C, Denis L, et al. (Март 2006 г.). «Прогнозирование рецидива и прогрессирования у отдельных пациентов с раком мочевого пузыря стадии Ta T1 с использованием таблиц риска EORTC: комбинированный анализ 2596 пациентов из семи исследований EORTC». Европейская урология. 49 (3): 466–5, обсуждение 475–7. Дои:10.1016 / j.eururo.2005.12.031. PMID 16442208.
- ^ Фернандес-Гомес Дж., Мадеро Р., Сольсона Э., Унда М., Мартинес-Пиньейро Л., Гонсалес М. и др. (Ноябрь 2009 г.). «Прогнозирование рецидива и прогрессирования немышечно-инвазивного рака мочевого пузыря у пациентов, получавших лечение бациллой Кальметта-Герена: оценочная модель CUETO». Журнал урологии. 182 (5): 2195–203. Дои:10.1016 / j.juro.2009.07.016. PMID 19758621.
- ^ «Рекомендации ЕАУ: немышечно-инвазивный рак мочевого пузыря». Uroweb.
- ^ Чой СИ, Рю Дж.Х., Чанг И.Х., Ким Т.Х., Мён С.К., Мун Ю.Т. и др. (Октябрь 2014 г.). «Прогнозирование рецидива и прогрессирования неинвазивного рака мочевого пузыря у корейских пациентов: сравнение моделей EORTC и CUETO». Корейский журнал урологии. 55 (10): 643–9. Дои:10.4111 / kju.2014.55.10.643. ЧВК 4198762. PMID 25324946.
- ^ а б Бринкман М., Зигерс депутат (сентябрь 2008 г.). «Питание, общая жидкость и рак мочевого пузыря». Скандинавский журнал урологии и нефрологии. Дополнение. 42 (218): 25–36. Дои:10.1080/03008880802285073. PMID 18815914. S2CID 21780999.
- ^ Бринкман М, Бантинкс Ф, Мулс Э., Зигерс М.П. (сентябрь 2006 г.). «Использование селена в химиопрофилактике рака мочевого пузыря». Ланцет. Онкология. 7 (9): 766–74. Дои:10.1016 / S1470-2045 (06) 70862-2. PMID 16945772.
- ^ Замора-Рос Р., Сасердот С., Риччери Ф., Вейдерпасс Е, Росвалл Н., Бакленд Г. и др. (Октябрь 2014 г.). «Потребление флавоноидов и лигнанов в зависимости от риска рака мочевого пузыря в исследовании Европейского проспективного исследования рака и питания (EPIC)». Британский журнал рака. 111 (9): 1870–80. Дои:10.1038 / bjc.2014.459. ЧВК 4453722. PMID 25121955.
- ^ Валтин Х (ноябрь 2002 г.). ""Выпивайте не менее восьми стаканов воды в день. »Правда? Есть ли научные доказательства того, что« 8 x 8 »?». Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология. 283 (5): R993-1004. Дои:10.1152 / ajpregu.00365.2002. PMID 12376390. S2CID 2256436.
- ^ «Заключительное обновление: рак мочевого пузыря у взрослых: скрининг - Целевая группа по профилактическим услугам США». www.uspreventiveservicestaskforce.org. Получено 13 ноября 2019.
- ^ Камат А.М., Хан Н.М., Эфстатиу Дж.А., Лернер С.П., Мальмстрём ПУ, Чой В. и др. (Декабрь 2016 г.). "Рак мочевого пузыря". Ланцет. 388 (10061): 2796–2810. Дои:10.1016 / S0140-6736 (16) 30512-8. PMID 27345655. S2CID 29104789.
- ^ а б c «Рекомендации NCCN по раку мочевого пузыря 2018» (PDF). Получено 25 ноября 2019.
- ^ Witjes JA, Babjuk M, Gontero P, Jacqmin D, Karl A, Kruck S и др. (Ноябрь 2014 г.). «Клиническая и экономическая эффективность цистоскопии в синем свете под контролем гексаминолевулината: обзор доказательств и обновленные рекомендации экспертов». Европейская урология. 66 (5): 863–71. Дои:10.1016 / j.eururo.2014.06.037. PMID 25001887.
- ^ Daneshmand S, Schuckman AK, Bochner BH, Cookson MS, Downs TM, Gomella LG и др. (Октябрь 2014 г.). «Цистоскопия гексаминолевулинатом в синем свете при немышечно-инвазивном раке мочевого пузыря: обзор клинических данных и консенсусное заявление о надлежащем использовании в США». Обзоры природы. Урология. 11 (10): 589–96. Дои:10.1038 / nrurol.2014.245. PMID 25245244.
- ^ Милади М., Пейромор М., Зербиб М., Сайги Д., Дебре Б. (март 2003 г.). «Значение второй трансуретральной резекции в оценке пациентов с опухолями мочевого пузыря». Европейская урология. 43 (3): 241–5. Дои:10.1016 / с0302-2838 (03) 00040-х. PMID 12600426.
- ^ а б «Рекомендации ЕАУ: немышечно-инвазивный рак мочевого пузыря». Uroweb.
- ^ а б Замбони С., Баумейстер П., Маттей А., Мордасини Л., Антонелли А., Симеоне С., Москини М. (февраль 2019 г.). «Однократная послеоперационная инстилляция при немышечно-инвазивном раке мочевого пузыря: есть ли еще какие-либо показания?». Трансляционная андрология и урология. 8 (1): 76–84. Дои:10.21037 / тау.2018.08.20. ЧВК 6414349. PMID 30976571.
- ^ Витес Дж. А., Хендриксен К. (январь 2008 г.). «Внутрипузырная фармакотерапия при немышечно-инвазивном раке мочевого пузыря: критический анализ имеющихся в настоящее время лекарств, графиков лечения и долгосрочных результатов». Европейская урология. 53 (1): 45–52. Дои:10.1016 / j.eururo.2007.08.015. PMID 17719169.
- ^ Ди Стази С.М., Ридл С. (июнь 2009 г.). «Обновления во внутрипузырном электродвижущем введении митомицина-С при немышечно-инвазивном раке мочевого пузыря» (PDF). Всемирный журнал урологии. 27 (3): 325–30. Дои:10.1007 / s00345-009-0389-x. HDL:2108/6440. PMID 19234707. S2CID 24496739.
- ^ Кос Б., Васкес Дж. Л., Миклавчич Д., Герман Г. Г., Гель Дж. (2016). «Исследование механизмов действия электродвижущихся лекарств (EMDA)». PeerJ. 4 (e2309): e2309. Дои:10.7717 / peerj.2309. ЧВК 5012313. PMID 27635313.
- ^ Bahouth Z, Halachmi S, Moskovitz B, Nativ O (2016). «Роль гипертермии как лечения немышечно-инвазивного рака мочевого пузыря». Экспертный обзор противоопухолевой терапии. 16 (2): 189–98. Дои:10.1586/14737140.2016.1126515. PMID 26618756. S2CID 681090.
- ^ Александрофф А.Б., Джексон А.М., О'Доннелл М.А., Джеймс К. (май 1999). «Иммунотерапия БЦЖ рака мочевого пузыря: 20 лет спустя». Ланцет. 353 (9165): 1689–94. Дои:10.1016 / S0140-6736 (98) 07422-4. PMID 10335805. S2CID 19355109.
- ^ Ламм Д.Л., Блюменштейн Б.А., Кроуфорд Е.Д., Монти Дж.Э., Скардино П., Гроссман Н.Б. и др. (Октябрь 1991 г.). «Рандомизированное исследование внутрипузырного доксорубицина и иммунотерапии бациллой Кальметта-Герена для переходно-клеточной карциномы мочевого пузыря». Медицинский журнал Новой Англии. 325 (17): 1205–9. Дои:10.1056 / NEJM199110243251703. PMID 1922207.
- ^ Курода К., Браун Э.Дж., Телле В.Б., Рассел Д.Г., Рэтлифф Т.Л. (январь 1993 г.). «Характеристика интернализации бациллы Кальметта-Герена опухолевыми клетками мочевого пузыря человека». Журнал клинических исследований. 91 (1): 69–76. Дои:10.1172 / JCI116202. ЧВК 329996. PMID 8423234.
- ^ Рэтлифф Т.Л., Ричи Дж. К., Юань Дж. Дж., Андриоле Г. Л., Каталония, Висконсин (сентябрь 1993 г.). «Подмножества Т-клеток, необходимые для внутрипузырной иммунотерапии БЦЖ при раке мочевого пузыря». Журнал урологии. 150 (3): 1018–23. Дои:10.1016 / s0022-5347 (17) 35678-1. PMID 8102183.
- ^ Fuge O, Vasdev N, Allchorne P, Green JS (2015). «Иммунотерапия рака мочевого пузыря». Исследования и отчеты в урологии. 7: 65–79. Дои:10.2147 / RRU.S63447. ЧВК 4427258. PMID 26000263.
- ^ а б c d Камат А.М., Флэйг Т.В., Гроссман Н.Б., Конети Б., Ламм Д., О'Доннелл М.А. и др. (Апрель 2015 г.). «Документ о консенсусе экспертов: Заявление о консенсусе по наилучшей практике управления в отношении использования внутрипузырной иммунотерапии с БЦЖ при раке мочевого пузыря». Обзоры природы. Урология. 12 (4): 225–35. Дои:10.1038 / nrurol.2015.58. PMID 25800393.
- ^ Альхунаиди О., Злотта АР (2019). «Применение внутрипузырной БЦЖ при уротелиальном раке мочевого пузыря». ракмедицина. 13: 905. Дои:10.3332 / ecancer.2019.905. ЧВК 6411413. PMID 30915163.
- ^ Д'Андреа Д., Гонтеро П., Шариат С.Ф., Сория Ф. (февраль 2019 г.). "Внутрипузырная палочка Кальметта-Герена при раке мочевого пузыря: все ли штаммы равны?". Трансляционная андрология и урология. 8 (1): 85–93. Дои:10.21037 / тау.2018.08.19. ЧВК 6414340. PMID 30976572.
- ^ Macleod LC, Ngo TC, Gonzalgo ML (июль 2014 г.). «Осложнения внутрипузырной палочки кальметта-герена». Журнал Канадской урологической ассоциации. 8 (7–8): E540-4. Дои:10.5489 / cuaj.1411. ЧВК 4137021. PMID 25210559.
- ^ Шах С., Картер-Монро Н., Атта М.Г. (октябрь 2015 г.). «Гранулематозный интерстициальный нефрит». Клинический журнал почек. 8 (5): 516–23. Дои:10.1093 / ckj / sfv053. ЧВК 4581373. PMID 26413275.
- ^ Декастекер К., Остерлинк В. (2015). «Управление побочными эффектами интравезикальной терапии бациллами Кальметта-Герена». Исследования и отчеты в урологии. 7: 157–63. Дои:10.2147 / RRU.S63448. ЧВК 4630183. PMID 26605208.
- ^ Witjes JA (май 2006 г.). «Лечение неудач БЦЖ при поверхностном раке мочевого пузыря: обзор». Европейская урология. 49 (5): 790–7. Дои:10.1016 / j.eururo.2006.01.017. PMID 16464532.
- ^ Бабюк В., Остерлинк В., Сильвестр Р. и др. (2010). «Рекомендации по TaT1 (немышечно-инвазивному) раку мочевого пузыря». Европейская ассоциация урологов. В архиве из оригинала от 24 апреля 2010 г.
- ^ Панель обновления клинических рекомендаций по раку мочевого пузыря (2007). Рак мочевого пузыря: Руководство по лечению немышечного инвазивного рака мочевого пузыря: (стадии Ta, T1 и Tis): обновление 2007 г.. Американская урологическая ассоциация.[страница нужна ]
- ^ Hassler MR, Shariat SF, Soria F (май 2019 г.). «Спасательные терапевтические стратегии при неудаче бациллы Кальметта-Герена». Текущее мнение в урологии. 29 (3): 239–246. Дои:10.1097 / МОУ.0000000000000593. PMID 30762670. S2CID 73439134.
- ^ а б c d «Лечение неметастатического мышечно-инвазивного рака мочевого пузыря: Руководство AUA / ASCO / ASTRO / SUO (2017) - Американская урологическая ассоциация». www.auanet.org. Получено 20 ноября 2019.
- ^ Джохар Р.С., Хайн М.Х., Стегеманн А.П., Ахмед К., Агарвал П., Балбей М.Д. и др. (Июль 2013). «Осложнения после радикальной цистэктомии с помощью роботов: результаты Международного консорциума роботизированной цистэктомии». Европейская урология. 64 (1): 52–7. Дои:10.1016 / j.eururo.2013.01.010. PMID 23380164.
- ^ Шабсиг А., Корец Р., Вора К.С., Брукс С.М., Кронин А.М., Сэвидж С. и др. (Январь 2009 г.). «Определение ранней заболеваемости радикальной цистэктомией для пациентов с раком мочевого пузыря с использованием стандартизированной методологии отчетности». Европейская урология. 55 (1): 164–74. Дои:10.1016 / j.eururo.2008.07.031. PMID 18675501.
- ^ Moschini M, Simone G, Stenzl A, Gill IS, Catto J (апрель 2016 г.). «Критический обзор результатов радикальной цистэктомии: можно ли уменьшить осложнения радикальной цистэктомии с помощью хирургического объема и роботизированной хирургии?». Европейский фокус урологии. 2 (1): 19–29. Дои:10.1016 / j.euf.2016.03.001. PMID 28723446.
- ^ Серантола Й., Валерио М., Перссон Б., Йихлински П., Юнгквист О., Хубнер М. и др. (Декабрь 2013). «Рекомендации по периоперационному уходу после радикальной цистэктомии при раке мочевого пузыря: рекомендации общества по усиленному восстановлению после операции (ERAS (®))». Клиническое питание. 32 (6): 879–87. Дои:10.1016 / j.clnu.2013.09.014. PMID 24189391.
- ^ «UpToDate: неоадъювантная химиотерапия». www.uptodate.com.
- ^ Вейл, К. (июнь 2003 г.). «Неоадъювантная химиотерапия при инвазивном раке мочевого пузыря: систематический обзор и метаанализ». Ланцет. 361 (9373): 1927–34. Дои:10.1016 / с0140-6736 (03) 13580-5. PMID 12801735. S2CID 29233494.
- ^ Сотрудничество по метаанализу расширенного рака мочевого пузыря (ABC) (август 2005 г.). «Неоадъювантная химиотерапия при инвазивном раке мочевого пузыря: обновление систематического обзора и метаанализа данных отдельных пациентов, сотрудничество в метаанализе передового рака мочевого пузыря (ABC)». Европейская урология. 48 (2): 202–5, обсуждение 205–6. Дои:10.1016 / j.eururo.2005.04.006. PMID 15939524.
- ^ Гроссман Х.Б., Натале РБ, Танген К.М., Спейтс В.О., Фогельзанг, штат Нью-Джерси, Трамп Д.Л. и др. (Август 2003 г.). «Неоадъювантная химиотерапия плюс цистэктомия по сравнению с одной цистэктомией при местнораспространенном раке мочевого пузыря». Медицинский журнал Новой Англии. 349 (9): 859–66. Дои:10.1056 / NEJMoa022148. PMID 12944571.
- ^ а б Инь М., Джоши М., Мейджер Р.П., Гланц М., Холдер С., Харви Х.А. и др. (Июнь 2016). «Неоадъювантная химиотерапия при мышечно-инвазивном раке мочевого пузыря: систематический обзор и двухэтапный метаанализ». Онколог. 21 (6): 708–15. Дои:10.1634 / теонколог.2015-0440. ЧВК 4912364. PMID 27053504.
- ^ Ивата Т., Кимура С., Абуфарадж М., Яниш Ф., Каракевич П.И., Сибахер В. и др. (Октябрь 2019 г.). «Роль адъювантной лучевой терапии после операции по поводу уротелиальной карциномы верхних и нижних мочевых путей: систематический обзор». Урологическая онкология. 37 (10): 659–671. Дои:10.1016 / j.urolonc.2019.05.021. PMID 31255542.
- ^ а б c d «Схемы лечения рака мочевого пузыря». Советник по терапии рака. 1 января 2019 г.. Получено 26 ноября 2019.
- ^ "Своевременно". www.uptodate.com. Получено 26 ноября 2019.
- ^ а б c Ploussard G, Daneshmand S, Efstathiou JA, Herr HW, James ND, Rödel CM, et al. (Июль 2014 г.). «Критический анализ сохранения мочевого пузыря с помощью тримодальной терапии при мышечно-инвазивном раке мочевого пузыря: систематический обзор». Европейская урология. 66 (1): 120–37. Дои:10.1016 / j.eururo.2014.02.038. PMID 24613684.
- ^ Смелзер В. В., Остенфельд М. А., Хольцбайерляйн Дж. М., Ли Е. К.. Где мы находимся с сохранением мочевого пузыря при мышечно-инвазивном раке мочевого пузыря в 2017 году ?. Индиан Дж. Урол 2017; 33: 111–7 http://www.indianjurol.com/text.asp?2017/33/2/111/203415 В архиве 10 сентября 2017 г. Wayback Machine
- ^ Мирза А., Чоудхури А. (апрель 2016 г.). «Сохранение мочевого пузыря при мышечно-инвазивном раке мочевого пузыря». Рак мочевого пузыря. 2 (2): 151–163. Дои:10.3233 / BLC-150025. ЧВК 4927909. PMID 27376137.
- ^ «Химиотерапия рака мочевого пузыря». www.cancer.org. Получено 27 ноября 2019.
- ^ «Рекомендации ЕАУ: мышечно-инвазивный и метастатический рак мочевого пузыря». Uroweb.
- ^ Гальский М.Д., Хан Н.М., Розенберг Дж., Сонпавде Дж., Хатсон Т., Оу В.К. и др. (Июнь 2011 г.). «Лечение пациентов с метастатическим уротелиальным раком,« непригодным »для химиотерапии на основе цисплатина». Журнал клинической онкологии. 29 (17): 2432–8. Дои:10.1200 / JCO.2011.34.8433. PMID 21555688. S2CID 33263969.
- ^ а б Ким Б (2018). «Раздел VI. Химиотерапия при метастатическом раке мочевого пузыря». Рак мочевого пузыря. Академическая пресса. п. 527. ISBN 978-0-12-809939-1. Получено 27 ноября 2019.
- ^ Лайман Г.Х., Дейл Д.К., Кулакова Э., Поневерски М.С., Вольф Д.А., Кудерер Н.М. и др. (Октябрь 2013). «Влияние колониестимулирующего фактора гранулоцитов на интенсивность дозы химиотерапии и выживаемость при раке: систематический обзор и метаанализ рандомизированных контролируемых исследований». Анналы онкологии. 24 (10): 2475–84. Дои:10.1093 / annonc / mdt226. ЧВК 3841419. PMID 23788754.
- ^ Гиллиган Т.Д., Стил Г.С., Зитман А.Л., Кантофф П.В. (2003). Химиотерапия при метастатических заболеваниях.
- ^ Гальский М.Д., Чен Г.Дж., Оу В.К., Беллмант Дж., Рот Б.Дж., Петриоли Р. и др. (Февраль 2012 г.). «Сравнительная эффективность химиотерапии на основе цисплатина и карбоплатина для лечения запущенной уротелиальной карциномы». Анналы онкологии. 23 (2): 406–10. Дои:10.1093 / annonc / mdr156. PMID 21543626.
- ^ Шелли, доктор медицины, Кливес, Уилт, доктор медицинских наук, Мейсон (июль 2011 г.). «Химиотерапия гемцитабином для лечения метастатической карциномы мочевого пузыря». BJU International. 108 (2): 168–79. Дои:10.1111 / j.1464-410X.2011.10341.x. PMID 21718430. S2CID 26003400.
- ^ Aapro M, Abrahamsson PA, Body JJ, Coleman RE, Colomer R, Costa L, et al. (Март 2008 г.). «Руководство по использованию бисфосфонатов при солидных опухолях: рекомендации международной группы экспертов». Анналы онкологии. 19 (3): 420–32. Дои:10.1093 / annonc / mdm442. PMID 17906299.
- ^ Шридхар СС (май 2017 г.). «Развитие лечения прогрессирующего рака уротелия». Журнал онкологической практики. 13 (5): 309–315. Дои:10.1200 / JOP.2017.022137. PMID 28489981.
- ^ Геруллис Х., Ваврошек Ф., Кёне СН, Экке ТХ (январь 2017 г.). «Винфлунин в лечении запущенного рака уротелия: клинические данные и опыт». Терапевтические достижения в урологии. 9 (1): 28–35. Дои:10.1177/1756287216677903. ЧВК 5167074. PMID 28042310.
- ^ Oing C, Rink M, Oechsle K, Seidel C, von Amsberg G, Bokemeyer C (февраль 2016 г.). «Химиотерапия второй линии для прогрессирующей и метастатической уротелиальной карциномы: винфлунин и не только - всесторонний обзор современной литературы». Журнал урологии. 195 (2): 254–63. Дои:10.1016 / j.juro.2015.06.115. PMID 26410730.
- ^ Ким Б (2018). «Раздел VI. Химиотерапия при метастатическом раке мочевого пузыря». Рак мочевого пузыря. Академическая пресса. п. 530. ISBN 978-0-12-809939-1. Получено 27 ноября 2019.
- ^ «Эрдафитиниб эффективен против запущенного рака мочевого пузыря». Национальный институт рака. 9 августа 2019.
- ^ Конала В.М., Адапа С., Ароноу В.С. (февраль 2019 г.). «Иммунотерапия рака мочевого пузыря». Американский журнал терапии: 1. Дои:10.1097 / MJT.0000000000000934. PMID 30839322.
- ^ Кац Х, Васи Э, Альшареди М (сентябрь 2017 г.). «Ингибиторы контрольных точек: новая парадигма лечения уротелиального рака мочевого пузыря». Медицинская онкология. 34 (10): 170. Дои:10.1007 / s12032-017-1029-8. PMID 28864844. S2CID 22280860.
- ^ Heidenreich A, Albers P, Classen J, Graefen M, Gschwend J, Kotzerke J, et al. (2010). «Визуализирующие исследования у пациентов с метастатическим урогенитальным раком, проходящих системную терапию: рекомендации мультидисциплинарного консенсусного совещания Ассоциации урологической онкологии Немецкого онкологического общества». Urologia Internationalis. 85 (1): 1–10. Дои:10.1159/000318985. PMID 20693823.
- ^ Ллевелин Р. "Критерии оценки ответа при солидных опухолях | Справочная статья по радиологии | Radiopaedia.org". Радиопедия.
- ^ Сиддики М.Р., Грант С., Сэнфорд Т., Агарвал П.К. (август 2017 г.). «Текущие клинические испытания немышечно-инвазивного рака мочевого пузыря». Урологическая онкология. 35 (8): 516–527. Дои:10.1016 / j.urolonc.2017.06.043. ЧВК 5556973. PMID 28778250.
- ^ «Рак мочевого пузыря - Статистика». Cancer.Net. 25 июня 2012 г.
- ^ Кауфман Д.С., Шипли В.У., Фельдман А.С. (июль 2009 г.). "Рак мочевого пузыря". Ланцет. 374 (9685): 239–49. Дои:10.1016 / S0140-6736 (09) 60491-8. PMID 19520422. S2CID 40417997.
- ^ van der Heijden AG, Witjes JA (сентябрь 2009 г.). «Рецидив, прогрессирование и наблюдение при немышечно-инвазивном раке мочевого пузыря». Европейские добавки для урологии. 8 (7): 556–562. Дои:10.1016 / j.eursup.2009.06.010.
- ^ Тайсон, доктор медицины, Чанг С.С., Киган К.А. (2016). «Роль консолидирующей хирургической терапии у пациентов с местнораспространенным или регионально метастатическим раком мочевого пузыря». Мочевой пузырь. 3 (2). Дои:10.14440 / мочевой пузырь.2016.89 (неактивно 9 ноября 2020 г.). ЧВК 5336315. PMID 28261632.CS1 maint: DOI неактивен по состоянию на ноябрь 2020 г. (ссылка на сайт)
- ^ Чжан Л., Ву Б., Чжа З, Цюй В., Чжао Х, Юань Дж. (Июль 2019 г.). «Клинико-патологические факторы рака мочевого пузыря для специфических для рака исходов выживаемости после радикальной цистэктомии: систематический обзор и метаанализ». BMC Рак. 19 (1): 716. Дои:10.1186 / s12885-019-5924-6. ЧВК 6642549. PMID 31324162.
- ^ Ку Дж.Х., Кан М., Ким Х.С., Чжон С.В., Квак С., Ким Х.Х. (июнь 2015 г.). «Плотность лимфатических узлов как прогностическая переменная при лимфоузловом раке мочевого пузыря: метаанализ». BMC Рак. 15: 447. Дои:10.1186 / с12885-015-1448-х. ЧВК 4450458. PMID 26027955.
- ^ Ян Л.С., Шан Б.Л., Шан Л.Л., Чин П., Мюррей С., Ахмади Н., Саксена А. (сентябрь 2016 г.). «Систематический обзор и метаанализ результатов качества жизни после радикальной цистэктомии по поводу рака мочевого пузыря». Хирургическая онкология. 25 (3): 281–97. Дои:10.1016 / j.suronc.2016.05.027. PMID 27566035.
- ^ Сомани Б.К., Гимлин Д., Файерс П., Н'дов Дж. (Ноябрь 2009 г.). «Качество жизни и изображение тела для пациентов с раком мочевого пузыря, перенесших радикальную цистэктомию и отведение мочи - проспективное когортное исследование с систематическим обзором литературы». Урология. 74 (5): 1138–43. Дои:10.1016 / j.urology.2009.05.087. PMID 19773042.
- ^ Вартоломей Л., Ферро М, Мироне В., Шариат С.Ф., Вартоломей М.Д. (июль 2018 г.). «Систематический обзор: распространенность депрессии и тревоги у больных раком мочевого пузыря». Рак мочевого пузыря. 4 (3): 319–326. Дои:10.3233 / BLC-180181. ЧВК 6087432. PMID 30112443.
- ^ Дэвид Э (февраль 2017 г.). «Психиатрические расстройства ухудшают выживаемость при раке мочевого пузыря». www.healio.com. Получено 27 ноября 2019.
- ^ Корреа А.Ф., Смалдоне М.С. (август 2018 г.). «Меланхолия и рак: повествование о раке мочевого пузыря». Рак. 124 (15): 3080–3083. Дои:10.1002 / cncr.31402. PMID 29660788.
- ^ «Статистика рака мочевого пузыря». Всемирный фонд исследования рака. 22 августа 2018 г.. Получено 9 ноября 2019.
- ^ "Информационный бюллетень Греции" (PDF). Глобальная обсерватория рака. Получено 9 ноября 2019.
- ^ «Страновые оценки ВОЗ по заболеваниям и травмам». Всемирная организация здоровья. 2009. В архиве из оригинала 11 ноября 2009 г.. Получено 11 ноября 2009.
- ^ Рот, Грегори А .; Abate, Degu; Абате, Калкидан Хассен; Абай, Соломон М .; Аббафати, Кристиана; Аббаси, Нушин; Аббастабар, Хедаят; Абдаллах, Фоад; Абдела, Джемаль; Абделалим, Ахмед; Абдоллахпур, Ибрагим; Абдулкадер, Ризван Сулианкачи; Абебе, Хафтом Темесген; Абебе, Молла; Абебе, Зегей; Abejie, Ayenew Negesse; Abera, Semaw F .; Абиль, Олифан Зевди; Абраха, Хафтом Нигусе; Абрам, Аклилу Роба; Абу-Раддад, Лайт Джамал; Акромбесси, Манфред Марио Коку; Ачарья, Диларам; Adamu, Abdu A .; Adebayo, Oladimeji M .; Адедойн, Руфус Адесоджи; Адеканмби, Виктор; Adetokunboh, Olatunji O .; Адена, Бейене Мересса; и другие. (Ноябрь 2018 г.). «Глобальная, региональная и национальная возрастная и национальная смертность от 282 причин смерти в 195 странах и территориях, 1980–2017 годы: систематический анализ для исследования глобального бремени болезней 2017». Ланцет. 392 (10159): 1736–1788. Дои:10.1016 / S0140-6736 (18) 32203-7. ЧВК 6227606. PMID 30496103.
- ^ Лаккис Н.А., Адиб С.М., Хамаде Г.Н., Эль-Джарра Р.Т., Осман М.Х. (2018). «Рак мочевого пузыря в Ливане: заболеваемость и сравнение с региональными и западными странами». Борьба с раком. 25 (1): 1073274818789359. Дои:10.1177/1073274818789359. ЧВК 6055109. PMID 30027755.
- ^ а б Хемельт М., Ямамото Х., Ченг К.К., Зигерс М.П. (январь 2009 г.). «Влияние курения на мужской избыток рака мочевого пузыря: метаанализ и географический анализ». Международный журнал рака. 124 (2): 412–9. Дои:10.1002 / ijc.23856. PMID 18792102. S2CID 28518800.
- ^ «Ученые нашли одну причину, почему рак мочевого пузыря поражает больше мужчин». Медицинский центр Университета Рочестера. 20 апреля 2007 г. Архивировано с оригинал 11 января 2009 г.. Получено 20 апреля 2007.
- ^ Kim A, Kim MS, Ahn JH, Choi WS, Park HK, Kim HG, Paick SH (ноябрь 2019 г.). «Клиническое значение терапии ингибитором 5-α редуктазы и андрогенной депривации в заболеваемости, рецидивах и выживаемости рака мочевого пузыря: метаанализ и системный обзор». Стареющий мужчина: 1–8. Дои:10.1080/13685538.2019.1646238. PMID 31724468.
- ^ "Факты о Канаде" (PDF). Глобальная обсерватория рака. Получено 9 ноября 2019.
- ^ а б «Статистика рака мочевого пузыря - Канадское онкологическое общество». www.cancer.ca. Получено 2 декабря 2019.
- ^ "Китайские факты" (PDF). Глобальная обсерватория рака. Получено 9 ноября 2019.
- ^ Пан Ц., Гуань И, Ли Х, Чен В., Чжу Г. (июнь 2016 г.). «Урологический рак в Китае». Японский журнал клинической онкологии. 46 (6): 497–501. Дои:10.1093 / jjco / hyw034. PMID 27049022.
- ^ команда FPFIS (8 марта 2017 г.). «Эпидемиология рака мочевого пузыря в Европе». Научный центр ЕС - Европейская комиссия. Получено 2 декабря 2019.
- ^ "Информационный бюллетень Великобритании" (PDF). Глобальная обсерватория рака. Получено 9 ноября 2019.
- ^ Ward EM, Sherman RL, Henley SJ, Jemal A, Siegel DA, Feuer EJ, et al. (Декабрь 2019 г.). «Ежегодный отчет для нации о статусе рака у мужчин и женщин в возрасте 20-49 лет». Журнал Национального института рака. 111 (12): 1279–1297. Дои:10.1093 / jnci / djz106. ЧВК 6910179. PMID 31145458.
- ^ «Ключевые статистические данные по раку мочевого пузыря». www.cancer.org. Получено 28 ноября 2019.
- ^ "Общие сайты рака - Факты статистики рака". ВИДЯЩИЙ. Получено 28 ноября 2019.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
- Рак мочевого пузыря в Керли
- Клинически проверено информация о раке мочевого пузыря для пациентов из Cancer Research UK
- Cancer.Net: рак мочевого пузыря
- Калькулятор EORTC для стратификации риска немышечно-инвазивного рака мочевого пузыря
