Взаимодействие с незаменимыми жирными кислотами - Essential fatty acid interactions
Воздействие на людей ω-3 (омега-3) и ω-6 (омега-6) незаменимые жирные кислоты (EFA) лучше всего характеризуются взаимодействия.
Арахидоновая кислота (AA) представляет собой 20-углеродную ω-6 условно незаменимую жирную кислоту.[1] Он находится во главе «каскад арахидоновой кислоты» - более 20 различных сигнальные пути которые контролируют широкий спектр функций организма, но особенно те функции, которые включают воспаление, рост клеток и Центральная нервная система.[2] Большая часть AA в организме человека поступает с пищей. линолевая кислота (другая незаменимая жирная кислота, 18: 2 ω-6), полученная из орехи, семена, растительные масла и животные жиры.
При воспалительной реакции две другие группы пищевых незаменимых жирных кислот образуют каскады, которые параллельны каскаду арахидоновой кислоты и конкурируют с ним. EPA (20: 5 ω-3) обеспечивает наиболее важный конкурирующий каскад. Он поступает из жирная рыба, и масло водорослей или неэффективно полученное с пищей альфа-линоленовая кислота найдено, например, в грецкие орехи, конопляное масло и льняное масло. ДГЛА (20: 3 ω-6) обеспечивает третий, менее заметный каскад. Это происходит из диетического GLA (18: 3 ω-6) найдено, например, в масло огуречника. Эти два параллельных каскада смягчают воспалительные эффекты определенных эйкозаноиды сделано из АА.
Сегодня обычная диета в индустриальных странах содержит гораздо меньше ω-3 жирных кислот, чем диета столетней давности, и гораздо большее количество загрязнение воздуха ежедневно, что вызывает воспалительную реакцию. В диете столетней давности было гораздо меньше ω-3, чем в диете ранней охотники-собиратели но и гораздо меньше загрязнения, чем сегодня.[3] Мы также можем посмотреть на соотношение ω-3 и ω-6 при сравнении их рационов. Эти изменения сопровождались увеличением заболеваемости многими заболеваниями - так называемыми болезни цивилизации - с воспалительными процессами. Сейчас есть очень веские доказательства[4] что некоторые из этих заболеваний облегчаются за счет увеличения содержания ω-3 в рационе, а также убедительные доказательства для многих других. Есть также более предварительные данные, показывающие, что диетический ω-3 может облегчить симптомы при некоторых психических расстройствах.[5]
Номенклатура серии эйкозаноидов
Эйкозаноиды - это сигнальные молекулы, полученные из незаменимых жирных кислот (EFA); они являются основным путем, по которому EFA действуют в организме. Есть четыре класса эйкозаноидов и две или три серии внутри каждого класса. Прежде чем обсуждать действие эйкозаноидов, мы объясним номенклатуру серий.
В плазматические мембраны из клетки содержать фосфолипиды, которые состоят из гидрофильной фосфатной головки и двух гидрофобных жирная кислота хвосты. Некоторые из этих жирных кислот состоят из 20 атомов углерода. полиненасыщенный незаменимые жирные кислоты - AA, EPA или DGLA.[нужна цитата ] В ответ на множество воспалительных сигналов эти EFA отщепляются от фосфолипида и высвобождаются в виде свободных жирных кислот. Затем EFA насыщается кислородом (одним из двух путей), а затем модифицируется с образованием эйкозаноидов.[нужна цитата ] Циклооксигеназа (COX) окисление удаляет два C = C двойные связи, ведущий к TX, PG и PGI серии.Липоксигеназа окисление не удаляет двойные связи C = C и приводит к LK.[6]
После окисления эйкозаноиды дополнительно модифицируются, делая серии. Члены серии различаются ABC ... буквы, и нумеруются по количеству двойных связей, которое не меняется в пределах ряда. Например, действие циклооксигеназы на AA (с 4 двойными связями) приводит к тромбоксанам 2-го ряда (TXA2, TXB2...) каждая с двумя двойными связями. Действие циклооксигеназы на EPA (с 5 двойными связями) приводит к тромбоксанам 3-го ряда (TXA3, TXB3...) каждая с тремя двойными связями. Из этого шаблона есть исключения, некоторые из которых указывают стереохимия (PGF2α).
В таблице (1) показаны эти последовательности для AA (20: 4 ω-6). Последовательности для EPA (20: 5 ω-3) и DGLA (20: 3 ω-6) аналогичны.
| Диетический Незаменимая жирная кислота | Abbr | Формула атомы углерода: двойные связи ω | Серия продуктов Eicosanoid | ||
|---|---|---|---|---|---|
| TX PG PGI | LK | Последствия | |||
| Гамма-линоленовая кислота через Дигомо гамма линоленовая кислота | GLA DGLA | 18: 3ω6 20: 3ω6 | серия-1 | серия-3 | менее воспалительный |
| Арахидоновая кислота | AA | 20: 4ω6 | серия-2 | серия-4 | более воспалительный |
| Эйкозапентаеновая кислота | EPA | 20: 5ω3 | серия-3 | серия-5 | менее воспалительный |
Все простеноиды заменены простановые кислоты.Страница Простеноидов Центра Киберлипидов[7] иллюстрирует исходное соединение и кольца, связанные с каждой буквой серии.
В ИЮПАК и IUBMB используйте эквивалентный термин Икозаноид.[7]
Каскад арахидоновой кислоты при воспалении
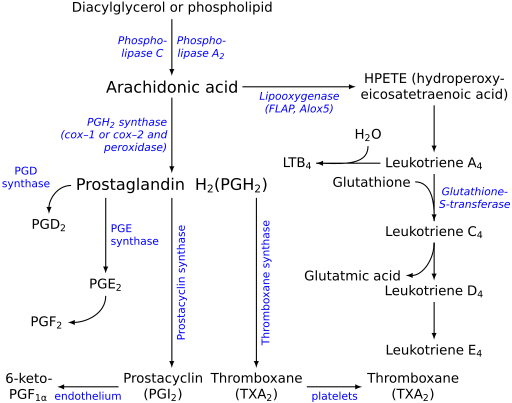
В каскаде арахидоновой кислоты диетическое линолевая кислота (18: 2 ω-6) ненасыщен и удлинен с образованием арахидоновой кислоты (а также других омега-6), этерифицированный в фосфолипид в клеточная мембрана.[8] Далее в ответ на многие воспалительные стимулы, такие как загрязнение воздуха, курение, пассивное курение, гидрогенизированные растительные масла и другие экзогенные токсины; фосфолипаза образуется и расщепляет этот фосфолипид, высвобождая АК в виде свободная жирная кислота.[нужна цитата ] Затем АК может быть насыщен кислородом и затем модифицирован с образованием эйкозаноиды – автокринный и паракринные агенты это связывает рецепторы на клетке или ее соседях, чтобы предупредить иммунную систему о повреждении клетки. В качестве альтернативы АА может диффундировать в ядро клетки и взаимодействовать с факторы транскрипции контролировать Транскрипция ДНК за цитокины или другие гормоны.
Механизмы действия эйкозаноидов ω-3

Эйкозаноиды из AA обычно способствуют воспалению. Те из GLA (через DGLA) и EPA обычно менее воспалительные, или неактивные, или даже противовоспалительные. (Это обобщение условно: эйкозаноид может оказывать провоспалительное действие в одной ткани и противовоспалительное действие в другой. Видеть обсуждение PGE2 в Колдере[9] или Тилли.[10])
На рисунке (2) показаны цепи синтеза ω-3 и -6, а также основные эйкозаноиды из AA, EPA и DGLA.
Диетический ω-3 и GLA противодействуют воспалительным эффектам эйкозаноидов AA тремя способами: вытеснение, конкурентное торможение и прямое противодействие.
Смещение
Диетический ω-3 снижает концентрацию АК в тканях. Исследования на животных показывают, что повышенный диетический ω-3 приводит к снижению содержания АК в мозге и других тканях.[11] Линоленовая кислота (18: 3 ω-3) способствует этому, смещая линолевая кислота (18: 2 ω-6) от удлинения и десатураза ферменты, продуцирующие АК. EPA подавляет фосфолипаза Высвобождение АА А2 из клеточной мембраны.[12] Другие механизмы, включающие транспорт EFAs, также могут играть роль.
Верно и обратное - высокое содержание линолевой кислоты в рационе снижает преобразование α-линоленовой кислоты в организме в EPA. Однако эффект не такой сильный; десатураза имеет более высокое сродство к α-линоленовой кислоте, чем к линолевой кислоте.[13]
Конкурентное торможение
DGLA и EPA конкурируют с AA за доступ к ферментам циклооксигеназы и липоксигеназы. Таким образом, присутствие DGLA и EPA в тканях снижает выход АА. эйкозаноиды. Например, диетическая GLA увеличивает тканевый DGLA и снижает TXB.2.[14][15] Точно так же EPA подавляет производство PG и TX серии 2.[9] Хотя DGLA не формирует LT, производная DGLA блокирует преобразование AA в LT.[16]
Противодействие
Некоторые эйкозаноиды, полученные из DGLA и EPA, противодействуют своим аналогам, полученным из АА. Например, DGLA дает PGE1, который сильно противодействует PGE2.[17] EPA дает антиагрегационный простациклин PGI3 [18] Он также дает лейокотриен LTB5 который нарушает действие LTB, полученного из АА4.[19]
Парадокс диетической GLA
Диетический окисленный линолевая кислота (LA, 18: 2 ω-6) воспалительный. В организме LA обесцвечивается с образованием GLA (18: 3 ω-6), но диетическая GLA обладает противовоспалительным действием. Некоторые наблюдения частично объясняют этот парадокс: LA конкурирует с α-линоленовая кислота, (ALA, 18: 3 ω-3) для Δ6-десатуразы и, таким образом, в конечном итоге ингибирует образование противовоспалительной EPA (20: 5 ω-3). Напротив, GLA не конкурирует за Δ6-десатуразу. Продукт удлинения GLA DGLA (20: 3 ω-6) конкурирует с 20: 4 ω-3 за Δ5-десатуразу, и можно было бы ожидать, что это вызовет воспаление GLA, но это не так, возможно, потому что этот шаг не ставка определения. Δ6-десатураза, по-видимому, действительно ограничивает скорость; 20: 4 ω-3 существенно не накапливается в липидах организма.
DGLA подавляет воспаление посредством конкурентного ингибирования и прямого противодействия (см. над.) Диетическая GLA приводит к резкому увеличению DGLA в мембранах белых кровяных телец, в отличие от LA. Это может отражать отсутствие десатуразы в лейкоцитах. Дополнение диетической GLA увеличивает сывороточный DGLA без увеличения сывороточного уровня AA.[17][20]
Вполне вероятно, что некоторая диетическая ГЛК в конечном итоге образует АК и способствует воспалению. Исследования на животных показывают, что эффект невелик.[15] Эмпирические наблюдения фактических эффектов GLA показывают, что противовоспалительные эффекты DGLA доминируют.[21]
Сложность путей
Пути передачи сигналов эйкозаноидов сложны, поэтому сложно охарактеризовать действие какого-либо конкретного эйкозаноида, например, PGE2 связывает четыре рецептора, получившие название EP1–4.Каждый кодируется отдельным геном, а некоторые существуют в нескольких изоформы.Каждый рецептор EP по очереди соединяется с G протеин.ЭР2, EP4 и одна изоформа EP3 рецепторы соединяются с GsЭто увеличивает внутриклеточное лагерь и обладает противовоспалительным действием.1 и другие EP3 изоформы соединяются с GqЭто приводит к увеличению внутриклеточного кальция и провоспалительно. Наконец, еще один EP3 пары изоформ к Gя, который одновременно снижает цАМФ и увеличивает кальций. Многие клетки иммунной системы экспрессируют несколько рецепторов, которые связывают эти явно противоположные пути.[10] Предположительно, производный ЭПК PGE3 имеет несколько иное влияние на эту систему, но не очень хорошо охарактеризовано.
Каскад арахидоновой кислоты в центральной нервной системе (ЦНС)
Даниэле Пиомелли Арахидоновая кислота[2]
Каскад арахидоновой кислоты в головном мозге протекает несколько иначе. Нейрогормоны, нейромодуляторы или нейротрансмиттеры действовать как первые посланники. Они активируют фосфолипидазу для высвобождения АК из нейрон клеточные мембраны как свободная жирная кислота.[нужна цитата ] В течение своей короткой жизни свободный АК может влиять на активность нейрона. ионные каналы и протеинкиназы. Или он может метаболизироваться с образованием эйкозаноидов, эпоксиэйкозатриеновые кислоты (EETs), нейропротектин D или различные эндоканнабиноиды (анандамид и его аналоги.)
Действие эйкозаноидов в головном мозге не так хорошо охарактеризовано, как при воспалении. Предполагается, что они действуют внутри нейрона как вторые посланники контроль пресинаптического торможения и активация протеинкиназа C. Они также действуют как паракринные медиаторы, воздействуя через синапсы на соседние клетки. Хотя подробностей о влиянии этих сигналов недостаточно, (Piomelli, 2000) комментирует
Нейроны в ЦНС организованы как взаимосвязанные группы функционально связанных клеток (например, в сенсорных системах). Диффузионный фактор, выделяемый нейроном в тканевая жидкость и способный взаимодействовать с мембранными рецепторами на соседних клетках, идеально подходит для «синхронизации» активности ансамбля взаимосвязанных нервных клеток. Кроме того, во время развития и в определенных формах обучения постсинаптические клетки могут секретировать регуляторные факторы, которые диффундируют обратно в пресинаптический компонент, определяя его выживание в качестве активного терминала, амплитуду его прорастания и его эффективность в секреции нейротрансмиттеров - феномен, известный как ретроградная регуляция. Было высказано предположение об участии метаболитов арахидоновой кислоты в ретроградной передаче сигналов и в других формах локальной модуляции нейрональной активности.
| Каскад арахидоновой кислоты | ||
|---|---|---|
| При воспалении | В мозгу | |
| Основное влияние на | Воспаление в ткани | Возбудимость нейронов |
| АА освобожден от | белые кровяные клетки | Нейроны |
| Триггеры для выпуска AA | Воспалительные раздражители | Нейротрансмиттеры, нейрогормоны и нейромодуляторы |
| Внутриклеточные эффекты на | Транскрипция ДНК цитокинов и др. медиаторы воспаления | Активность ионных каналов и белка киназы |
| Метаболизируется с образованием | Эйкозаноиды, резольвины, изофураны, изопростаны, липоксины, эпоксиэйкозатриеновые кислоты (EET) | Эйкозаноиды, нейропротектин D, EETs и некоторые эндоканнабиноиды |
Каскады EPA и DGLA также присутствуют в мозге, и их метаболиты эйкозаноидов были обнаружены. Способы, которыми они по-разному влияют на психические и нервные процессы, не так хорошо изучены, как эффекты при воспалении.
Дальнейшее обсуждение
На рисунке (2) показаны два пути от EPA к DHA, включая исключительные Шунт Спрекера.
5-LO действует на пятый углерод от карбоксильная группа.Другие липоксигеназы - 8-LO, 12-LO и 15-LO - производят другие эйкозаноидоподобные продукты. Чтобы действовать, 5-LO использует ядерную мембрану. фермент Белок, активирующий 5-липоксигеназу (ЗАСЛОНКА), сначала в гидропероксиэйкозатетраеновая кислота (HPETE), затем к первому лейокотриену, LTA.
Смотрите также
- Незаменимая жирная кислота
- Омега-3 жирные кислоты
- Омега-6 жирные кислоты
- Соотношение омега-3 и омега-6 в разных продуктах
- Эйкозаноид
- Докозаноид
Рекомендации
- ^ Cunnane SC (ноябрь 2003 г.). «Проблемы с незаменимыми жирными кислотами: время для новой парадигмы?». Прогресс в исследованиях липидов. 42 (6): 544–68. Дои:10.1016 / S0163-7827 (03) 00038-9. PMID 14559071.
- ^ а б Пиомелли, Даниэле (2000). "Арахидоновая кислота". Нейропсихофармакология: пятое поколение прогресса. Архивировано из оригинал на 2006-07-15. Получено 2006-03-03.
- ^ Симопулос А. (2001). «Эволюционные аспекты диеты и незаменимых жирных кислот». Жирные кислоты и липиды - новые открытия (PDF). Диета World Rev Nutr. Всемирный обзор питания и диетологии. 88. С. 18–27. Дои:10.1159/000059742. ISBN 978-3-8055-7182-1. PMID 11935953.
- ^ Национальный институт здоровья (1 августа 2005 г.). «Омега-3 жирные кислоты, рыбий жир, альфа-линоленовая кислота». Архивировано из оригинал 8 февраля 2006 г.. Получено 21 августа, 2010.
- ^ De Caterina, R .; Баста, Г. (2001). «Жирные кислоты n-3 и воспалительная реакция - биологический фон» (PDF). Добавки European Heart Journal. 3 (доп. D): D42. Дои:10.1016 / S1520-765X (01) 90118-X.
- ^ Киберлипид Центр. «Полиеновые жирные кислоты». Архивировано из оригинал 30 сентября 2018 г.. Получено 11 февраля, 2006.
- ^ а б Киберлипид Центр. «Простаноиды». Архивировано из оригинал 8 февраля 2007 г.. Получено 11 февраля, 2006.
- ^ Уилан Дж, Фриче К. (2013). "Линолевая кислота". Adv Nutr. 4 (3): 311–312. Дои:10.3945 / ан.113.003772. ЧВК 3650500. PMID 23674797.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ а б Колдер, Филип С. (сентябрь 2004 г.). «n-3 жирные кислоты и воспаление - новые повороты в старинной сказке». Архивировано из оригинал 16 марта 2006 г.. Получено 8 февраля, 2006.
- Приглашенная обзорная статья, Информационный бюллетень PUFA.
- ^ а б Тилли С., Коффман Т., Коллер Б. (2001). «Смешанные сообщения: модуляция воспаления и иммунных ответов простагландинами и тромбоксанами». J Clin Invest. 108 (1): 15–23. Дои:10.1172 / JCI13416. ЧВК 209346. PMID 11435451. Получено 2007-01-30.
- ^ Новости медицинских исследований (25 мая 2005 г.). «Уровни жирных кислот в мозге связаны с депрессией». Получено 10 февраля, 2006.
- Кто в свою очередь цитировал Грин П., Гиспан-Герман И., Ядид Г. (июнь 2005 г.). «Повышенная концентрация арахидоновой кислоты в мозге крыс Flinders Sensitive Line, животная модель депрессии». J. Lipid Res. 46 (6): 1093–6. Дои:10.1194 / мл. C500003-JLR200. PMID 15805551.
- ^ КП Су; SY Huang; CC Chiu; WW Шен (2003). «Омега-3 жирные кислоты при большом депрессивном расстройстве. Предварительный двойной слепой, плацебо-контролируемый?» (PDF). Архивировано из оригинал (PDF) 8 февраля 2005 г.. Получено 22 февраля, 2006.
- ^ Финни, SD; RS Odin; С.Б. Джонсон и Р.Т. Холман (1 марта 1990 г.). «Пониженное содержание арахидоната в сывороточных фосфолипидах и эфирах холестерина, связанное с вегетарианской диетой у людей». Американский журнал клинического питания. 51 (3): 385–392. Дои:10.1093 / ajcn / 51.3.385. PMID 2106775. Архивировано из оригинал 12 февраля 2007 г.. Получено 11 февраля, 2006.
- «[D] итетарная арахидоновая кислота обогащает свой циркулирующий пул у людей; однако 20: 5n-3 не так же реагирует на ограничения в питании».
- ^ Guivernau M, Meza N, Barja P, Roman O (ноябрь 1994 г.). «Клинические и экспериментальные исследования долгосрочного влияния пищевой гамма-линоленовой кислоты на липиды плазмы, агрегацию тромбоцитов, образование тромбоксана и продукцию простациклина». Простагландины, лейкотриены и незаменимые жирные кислоты. 51 (5): 311–6. Дои:10.1016/0952-3278(94)90002-7. PMID 7846101.
- GLA снижает триглицериды, LDL, увеличивает HDL, снижает TXB2 и другие воспалительные маркеры. Обзорная статья; исследования на людях и крысах.
- ^ а б Карлстад, доктор медицины, Демишель С.Дж., Литем В.Д., Петерсон МБ (ноябрь 1993 г.). «Влияние внутривенных липидных эмульсий, обогащенных гамма-линоленовой кислотой, на плазменные n-6 жирные кислоты и биосинтез простагландинов после ожогов и эндотоксиновых повреждений у крыс». Крит. Care Med. 21 (11): 1740–9. Дои:10.1097/00003246-199311000-00025. PMID 8222692. S2CID 36538810.
- Внутривенное введение гамма-линоленовой кислоты увеличивало уровень GLA в сыворотке, но не увеличивало процентное содержание арахидоновой кислоты в плазме (исследование на крысах), уменьшало TXB2.
- ^ Белч Дж. Дж., Хилл А (январь 2000 г.). «Масло примулы вечерней и масло бурачника при ревматологии». Являюсь. J. Clin. Нутр. 71 (1 приложение): 352С – 6С. Дои:10.1093 / ajcn / 71.1.352s. PMID 10617996.
- «Сам DGLA не может быть преобразован в LT, но может образовывать 15-гидроксильное производное, которое блокирует превращение арахидоновой кислоты в LT. Увеличение потребления DGLA может позволить DGLA действовать как конкурентный ингибитор PG 2-й серии и LT 4-й серии и, таким образом, подавить воспаление ».
- ^ а б Фань, Ян-И; Роберт С. Чапкин (9 сентября 1998 г.). «Важность диетической гамма-линоленовой кислоты для здоровья и питания человека». Журнал питания. 128 (9): 1411–1414. Дои:10.1093 / jn / 128.9.1411. PMID 9732298. Получено 2007-01-05.
- «[D] ietary GLA увеличивает содержание продукта своей элонгазы, дигомо-гамма линоленовой кислоты (DGLA), в клеточных мембранах без сопутствующих изменений арахидоновой кислоты (AA). Впоследствии, при стимуляции, DGLA может быть преобразован воспалительными клетками до 15 - (S) -гидрокси-8,11,13-эйкозатриеновая кислота и простагландин E1. Это примечательно, поскольку эти соединения обладают как противовоспалительными, так и антипролиферативными свойствами ».
- ^ Фишер С., Вебер П.С. (сентябрь 1985 г.). «Тромбоксан (TX) A3 и простагландин (PG) I3 образуются у человека после приема в пищу эйкозапентаеновой кислоты: идентификация и количественное определение с помощью капиллярной газовой хроматографии и масс-спектрометрии с электронным ударом». Биомед. Масс-спектрометрия. 12 (9): 470–6. Дои:10.1002 / bms.1200120905. PMID 2996649.
- ^ Прескотт С.М. (июнь 1984 г.). «Влияние эйкозапентаеновой кислоты на продукцию лейкотриена B нейтрофилами человека» (PDF). J. Biol. Chem. 259 (12): 7615–21. PMID 6330066.
- ^ Джонсон М.М., Свон Д.Д., Суретт М.Э. и др. (1997). «Пищевая добавка с гамма-линоленовой кислотой изменяет содержание жирных кислот и выработку эйкозаноидов у здоровых людей». J. Nutr. 127 (8): 1435–44. Дои:10.1093 / jn / 127.8.1435. PMID 9237935.
- ^ Стоун К.Дж., Уиллис А.Л., Харт В.М., Киртланд С.Дж., Кернофф ПБ, Макникол Г.П. (февраль 1979 г.). «Метаболизм дигомо-гамма-линоленовой кислоты в человеке». Липиды. 14 (2): 174–80. Дои:10.1007 / BF02533869. PMID 423720. S2CID 41372225.
