Шигатоксигенные и веротоксигенные Escherichia coli - Википедия - Shigatoxigenic and verotoxigenic Escherichia coli
| Шигатоксигенный и веротоксигенный Кишечная палочка | |
|---|---|
| Специальность | Инфекционное заболевание |
Шигатоксигенный кишечная палочка (СТЭК) и веротоксигенный Кишечная палочка (VTEC) являются штаммами бактерии кишечная палочка которые производят либо Шига токсин или же Шига-подобный токсин (веротоксин). Лишь небольшая часть штаммов вызывает болезни у людей.[1][неудачная проверка ] Те, которые делают, вместе известны как энтерогеморрагический Кишечная палочка (EHEC) и являются основными причинами болезни пищевого происхождения. Когда заражение люди, они часто вызывают гастроэнтерит, энтероколит, и кровавый понос (отсюда и название «энтерогеморрагический») и иногда вызывают тяжелые осложнение называется гемолитико-уремический синдром (HUS).[2] Группа и ее подгруппы известны по различные имена. Их отличают от других штаммов кишечных патогенных микроорганизмов. Кишечная палочка включая энтеротоксигенный Кишечная палочка (ETEC), энтеропатогенный Кишечная палочка (EPEC), энтероинвазивный Кишечная палочка (EIEC), энтероагрегантный Кишечная палочка (EAEC) и диффузно адгезивные Кишечная палочка (DAEC).[3]
Фон
Самый известный из этих штаммов - O157: H7, но штаммы, не относящиеся к O157, вызывают примерно 36000[нужна цитата ] болезней, 1000 госпитализаций и 30 смертей в США ежегодно.[4] Специалисты по безопасности пищевых продуктов признают штаммы "большой шестерки": O26; O45; O103; O111; O121; и O145.[4] А Вспышка 2011 г. в Германии был вызван другим STEC, O104: H4. Этот штамм обладает как энтероагрегативными, так и энтерогеморрагическими свойствами. Оба штамма O145 и O104 могут вызывать гемолитико-уремический синдром (ГУС); на первый штамм приходится от 2% до 51% известных случаев ГУС; примерно 56% таких случаев вызваны O145 и 14% - другими штаммами EHEC.
EHEC, вызывающие кровавую диарею, в 10% случаев приводят к ГУС. Клинические проявления постдиарейного ГУС включают: острая почечная недостаточность, микроангиопатическая гемолитическая анемия, и тромбоцитопения. Вероцитотоксин (шига-подобный токсин) может напрямую повреждать почечные и эндотелиальные клетки. Тромбоцитопения возникает, когда тромбоциты потребляются путем свертывания крови. Гемолитическая анемия возникает в результате внутрисосудистого фибрин отложение, повышенная хрупкость эритроцитов и фрагментация.[3]
Антибиотики имеют сомнительную ценность и не продемонстрировали явной клинической пользы. Антибиотики, нарушающие синтез ДНК, например фторхинолоны, как было показано, индуцируют бактериофаг, несущий Stx, и вызывают повышенное производство токсинов.[5] Попытки блокировать выработку токсинов с помощью антибактериальных средств, нацеленных на синтез рибосомного белка, концептуально более привлекательны. Плазменный обмен предлагает противоречивое, но, возможно, полезное лечение. Использование агенты, снижающие моторику (лекарства, подавляющие диарею за счет замедления прохождения кишечника) у детей младше 10 лет или у пожилых пациентов следует избегать, поскольку они повышают риск ГУС с инфекциями EHEC.[3]
Клиническая картина варьируется от легкой до неосложненной. понос до геморрагического колит при сильных болях в животе. Серотип O157: H7 может вызвать инфекционную дозу, содержащую 100 бактериальных клеток или меньше; другой штамм, такой как 104: H4, также вызвал вспышку в Германии в 2011 году. Инфекции чаще всего возникают в теплые месяцы и у детей в возрасте до пяти лет и обычно передаются от сырого мяса и непастеризованный молоко и сок. Первоначально у пациентов развивается некровавый понос после того, как бактерия прикрепляется к эпителий или терминал подвздошная кишка, слепая кишка, и двоеточие. Последующее производство токсинов опосредует кровавую диарею. У детей осложнением может быть гемолитико-уремический синдром, который затем использует цитотоксины для атаки клеток в кишечнике, так что бактерии могут просачиваться в кровь и вызывать повреждение эндотелия в таких местах, как почки, путем связывания с глоботриаозилцерамидом (Gb3).
Имена
Имена группы и ее подгрупп включают следующее.[6] Существует некоторое многозначность участвует. Неизменный синонимичность обозначается одинаковым цветом. Помимо этого, существует еще более широкая, но изменчивая синонимия. Первые два (фиолетовые) в самом узком смысл обычно рассматриваются как гиперонимы из остальных (красный и синий), хотя и менее точно использование красный и синий часто считались синонимами пурпурного. По крайней мере, одна ссылка указывает на то, что "EHEC" исключает "VTEC" и "STEC",[2] но это не соответствует общепринятому использованию, так как многие другие публикации объединяют все последнее с первым. Если определить токсин Шига как точный токсин из Шигелла дизентерия, вплоть до каждого последнего аминокислотного остатка, то можно просмотреть все кишечная палочка штаммы, которые продуцируют токсин, аналогичный VTEC, с все их токсинов SLT, нет ST; но столь же разумный взгляд на STEC как на производящий «тот же» токсин, что и Шигелла дизентерия (потому что разница незначительна для большинства целей) отличает STEC от VTEC. На практике выбор слов и категорий не так важен, как понимание клинической значимости. По мере развития микробиологии исторические вариации в номенклатуре (которые возникли из-за постепенного развития науки во многих местах) все больше уступают место признанию всех этих молекул «версиями одного и того же токсина», а не «разными токсинами».[7]:2–3
| Имя | Краткая форма |
|---|---|
| энтерогеморрагический Кишечная палочка | EHEC |
| гемолитико-уремический синдром - ассоциированный энтерогеморрагический Кишечная палочка | HUSEC |
| шига-токсин продуцирует Кишечная палочка | СТЭК |
| шигатоксигенный Кишечная палочка | СТЭК |
| шига-подобный токсин - продуцирующий Кишечная палочка | SLTEC |
| продуцирующий веротоксин Кишечная палочка | VTEC |
| веротоксигенный Кишечная палочка | VTEC |
| продуцирующий вероцитотоксин Кишечная палочка | VTEC |
| вероцитотоксигенный Кишечная палочка | VTEC |
Инфекционность и вирулентность
В заразительность или вирулентность штамма EHEC зависит от нескольких факторов, в том числе от наличия фукоза в среде восприятие этого сахара и активация EHEC остров патогенности.
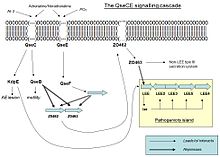
Регуляция острова патогенности
Эта статья может быть слишком техническим для большинства читателей, чтобы понять. Пожалуйста помогите улучшить это к Сделайте это понятным для неспециалистов, не снимая технических деталей. (Декабрь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
EHEC становится патогенным благодаря экспрессии локуса сглаживания энтероцитов (LEE), кодируемого на его острове патогенности. Однако, когда EHEC не находится в хозяине, это выражение является пустой тратой энергии и ресурсов, поэтому оно активируется только в том случае, если некоторые молекулы обнаруживаются в окружающей среде.
Когда QseC или QseE связываются с одной из их взаимодействующих сигнальных молекул, они аутофосфорилируют и переносят ее фосфат на регулятор ответа. QseC чувства адреналин, норадреналин и эндонуклеазой I-SceIII, кодируемой подвижным интроном группы I в митохондриальном гене COX1 (AI3); тогда как QseE чувствует адреналин, норадреналин, SO4 и PO4. Эти сигналы являются четким указанием бактериям на то, что они больше не свободны в окружающей среде, а в кишечнике.
В результате QseC фосфорилирует QseB (который активирует жгутики), KpdE (который активирует LEE) и QseF. QseE фосфорилирует QseF. Продукты QseBC и QseEF подавляют экспрессию FusK и FusR. FusK и FusR - два компонента системы, подавляющей транскрипцию генов LEE. FusK - это сенсорная киназа, которая способна ощущать многие сахара, в том числе фукозу. Когда фукоза присутствует в среде, FusK фосфорилирует FusR, который подавляет экспрессию LEE.
Таким образом, когда EHEC попадает в кишечник, возникает конкуренция между сигналами, поступающими от QseC и QseF, и сигналом, поступающим от FusK. Первые два хотели бы активировать вирулентность, но Фуск останавливает это, потому что слизистый слой, который является источником фукозы, изолирует энтероциты от бактерий, делая бесполезным синтез факторов вирулентности. Однако, когда концентрация фукозы снижается из-за того, что бактериальные клетки находят незащищенную область эпителия, тогда экспрессия генов LEE не будет подавляться FusR, и KpdE будет сильно их активировать. Таким образом, комбинированный эффект QseC / QseF и FusKR обеспечивает систему тонкой настройки экспрессии LEE, которая экономит энергию и позволяет механизмам вирулентности проявляться только тогда, когда шансы на успех выше.
Комплекс ФусКР
Этот комплекс, образованный двумя компонентами (FusK и FusR), выполняет в EHEC функцию обнаружения присутствия фукозы в окружающей среде и регулирования активации генов LEE. -FusK: кодируется геном z0462. Этот ген является сенсором гистидинкиназы. Он обнаруживает фукозу, а затем фосфорилирует ген Z0463, активируя ее. -FusR: кодируется геном z0463. Этот ген является репрессором генов LEE. Когда ген z0462 обнаруживает фукозу, фосфорилирует и активирует ген Z0463, который подавляет экспрессию le r, регулятора генов LEE. Если ген z0463 не активен, экспрессия гена ler не будет подавляться. Экспрессия ler активирует оставшиеся гены на острове патогенности, вызывая вирулентность. В то же время система FusKR ингибирует ген Z0461, транспортер фукозы.

Фукоза увеличивает активацию системы FusKR, которая ингибирует ген z0461, контролирующий метаболизм фукозы. Это механизм, который помогает избежать конкуренции за фукозу с другими штаммами Кишечная палочка которые обычно более эффективно используют фукозу в качестве источника углерода. Высокие концентрации фукозы в среде также увеличивают репрессию генов LEE.
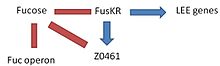
При низком уровне фукозы в окружающей среде система FusKR неактивна, а это означает, что ген z0461 транскрибируется, что увеличивает метаболизм фукозы. Кроме того, низкая концентрация фукозы является признаком незащищенного эпителия, поэтому репрессия генов ler исчезнет, и экспрессия генов LEE позволит атаковать соседние клетки.
Смотрите также
Рекомендации
- ^ Croxen MA, Law RJ, Scholz R, Keeney KM, Wlodarska M, Finlay BB (2013). «Последние достижения в понимании кишечной патогенной кишечной палочки». Обзоры клинической микробиологии. 26 (4): 822–80. Дои:10.1128 / CMR.00022-13. ЧВК 3811233. PMID 24092857.
- ^ а б Майнил, Дж (1999), «Шига / вероцитотоксины и шига / веротоксигенные Escherichia coli у животных», Vet Res, 30 (2–3): 235–57, PMID 10367357.
- ^ а б c Пэ, У Кюн; Ли, Юн Кён; Чо, Мин Сок; Ма, Сон Квон; Ким, Су Ван; Ким, Нам Хо; Чой, Ки Чул (30.06.2006). «Случай гемолитико-уремического синдрома, вызванного Escherichia coli O104: H4». Йонсей Мед Дж.. 47 (3): 437–439. Дои:10.3349 / ymj.2006.47.3.437. ЧВК 2688167. PMID 16807997. Два предложения были взяты из этого источника дословно.
- ^ а б Маллов, Зак (26 апреля 2010 г.). «Юристы борются с FSIS по поводу E. coli, не относящейся к O157». Новости безопасности пищевых продуктов. Получено 2 июн 2011.
- ^ Чжан, X; McDaniel, AD; Wolf, LE; Кеуш, GT; Уолдор, МК; Ачесон, DW (2000). «Хинолоновые антибиотики вызывают бактериофаги, кодирующие токсин Шига, выработку токсинов и гибель мышей». Журнал инфекционных болезней. 181 (2): 664–70. Дои:10.1086/315239. PMID 10669353.
- ^ Карч, Хельге; Tarr, Phillip I .; Беляшевская, Мартина (2005). «Энтерогеморрагический кишечная палочка в медицине человека ». Международный журнал медицинской микробиологии. 295 (6–7): 405–18. Дои:10.1016 / j.ijmm.2005.06.009. PMID 16238016.
- ^ Сильва, Кристофер Дж .; Брэндон, Дэвид Л .; Скиннер, Крейг Б.; Он, Сяохуа; и другие. (2017), «Глава 3: Структура токсинов шига и других токсинов AB5», Токсины шига: обзор структуры, механизма и обнаружения, Спрингер, ISBN 978-3319505800.
дальнейшее чтение
- Bardiau, M .; М. Сало и Дж. Дж. Майнил (2010). «Первоначальное присоединение EPEC, EHEC и VTEC к клеткам-хозяевам». Vet Res. 41 (5): 57. Дои:10.1051 / vetres / 2010029. ЧВК 2881418. PMID 20423697.
- Wong, A.R .; и другие. (2011). «Энтеропатогенные и энтерогеморрагические Escherichia coli: еще более разрушительные элементы». Мол Микробиол. 80 (6): 1420–38. Дои:10.1111 / j.1365-2958.2011.07661.x. PMID 21488979. S2CID 24606261.
- Тацуно, И. (2007). «[Присоединение энтерогеморрагической Escherichia coli O157: H7 к эпителиальным клеткам человека]». Нихон Сайкингаку Засши. 62 (2): 247–53. Дои:10.3412 / jsb.62.247. PMID 17575791.
- Kaper, J.B .; Дж. П. Натаро и Х. Л. Мобли (2004). «Патогенная кишечная палочка». Нат Рев Микробиол. 2 (2): 123–40. Дои:10.1038 / nrmicro818. PMID 15040260. S2CID 3343088.
- Garcia, A .; J.G. Фокс и Т. Бессер (2010). «Зоонозная энтерогеморрагическая кишечная палочка: перспектива единого здоровья». ИЛАР ДЖ. 51 (3): 221–32. Дои:10.1093 / ilar.51.3.221. PMID 21131723.
- Симидзу, Т. (2010). «[Экспрессия и внеклеточное высвобождение токсина шига при энтерогеморрагической кишечной палочке]». Нихон Сайкингаку Засши. 65 (2–4): 297–308. Дои:10.3412 / jsb.65.297. PMID 20505269.
внешняя ссылка
| Классификация |
|---|
