Азапроцин - Википедия - Azaprocin
 | |
| Клинические данные | |
|---|---|
| Код УВД |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| Химические и физические данные | |
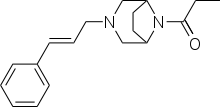
| Формула | C18ЧАС24N2О |
| Молярная масса | 284.403 г · моль−1 |
| 3D модель (JSmol ) | |
| Температура плавления | От 170 до 175 ° C (от 338 до 347 ° F) |
| |
| |
| | |
Азапроцин это препарат, который опиоид обезболивающее примерно в десять раз эффективнее морфий, а также быстрое начало и короткая продолжительность действия.[1][2][3] Он был открыт в 1963 году, но никогда не продавался.
Производное, замещенное в фенильном кольце п-нитрогруппой, более эффективно, чем исходное соединение, примерно в 25 раз сильнее, чем морфин.[4] Аналоги 2,6-диметилпиперазина с раскрытым кольцом также активны,[5] и большое семейство опиоидных анальгетиков, полученных из этой исходной структуры, было разработано за последние 40 лет.[6][7][8][9][10][11][12][13][14][15] Один аналог, АП-237, использовался в Китае для лечения боли, вызванной раком.
Рекомендации
- ^ Cignarella G, Occelli E, Cristiani G, Paduano L, Testa E (ноябрь 1963 г.). «Бициклические гомологи пиперазина. VI.1. Синтез и анальгетическая активность 3-замещенных 8-пропионил-3,8-диазабицикло [3.2.1] октанов». Журнал медицинской химии. 6 (6): 764–6. Дои:10.1021 / jm00342a030. PMID 14184943.
- ^ Cignarella G, Occelli E, Testa E (май 1965 г.). «Бициклические гомологи пиперазина. VII.1 Синтез и анальгетическая активность 3-аралкенил-8-пропионил-3,8-диазабицикло [3.2.1] октанов». Журнал медицинской химии. 8 (3): 326–31. Дои:10.1021 / jm00327a010. PMID 14323140.
- ^ Росселли дель Турко Б., Маффии Г. (февраль 1968 г.). «[Влияние обезболивающих на условное поведение крыс]». Боллеттино Чимико Фармацевтико. 107 (2): 120–6. PMID 5730115.
- ^ Cignarella G, Barlocco D, Tranquillini ME, Volterra A, Brunello N, Racagni G (май 1988 г.). «Взаимодействие 3,8-диазабицикло (3.2.1) октанов с мю- и дельта-опиоидными рецепторами». Сообщения о фармакологических исследованиях. 20 (5): 383–94. Дои:10.1016 / s0031-6989 (88) 80014-6. PMID 2843931.
- ^ Cignarella G, Testa E (май 1968 г.). «2,6-Диалкилпиперазины. IV. 1-Пропионил-4-замещенные цис-2,6-диметилпиперазины, структурно родственные анальгетическим 8-ацил-3,8-диазабицикло [3.2.1] октанам». Журнал медицинской химии. 11 (3): 592–4. Дои:10.1021 / jm00309a039. PMID 5656502.
- ^ Cignarella G, Barlocco D, Tranquillini ME, Volterra A, Brunello N, Racagni G (май 1988 г.). «Взаимодействие 3,8-диазабицикло (3.2.1) октанов с мю- и дельта-опиоидными рецепторами». Сообщения о фармакологических исследованиях. 20 (5): 383–94. Дои:10.1016 / s0031-6989 (88) 80014-6. PMID 2843931.
- ^ Barlocco D, Cignarella G, Greco G, Novellino E (октябрь 1993 г.). «Компьютерные взаимосвязи структура-сродство в наборе производных пиперазина и 3,8-диазабицикло [3.2.1] октана, связывающихся с мю-опиоидным рецептором». Журнал компьютерного молекулярного дизайна. 7 (5): 557–71. Bibcode:1993JCAMD ... 7..557B. Дои:10.1007 / bf00124362. PMID 8294946. S2CID 23360530.
- ^ Fadda P, Barlocco D, Tronci S, Cignarella G, Fratta W. (ноябрь 1997 г.). «Антиноцицептивное действие DBO 17 и DBO 11 у мышей: два производных 3,8 диазабицикло (3.2.1.) Октана с селективным сродством к опиоидным рецепторам мю». Архив фармакологии Наунин-Шмидеберг. 356 (5): 596–602. Дои:10.1007 / pl00005095. PMID 9402039. S2CID 40655683.
- ^ Barlocco D, Cignarella G, Vianello P, Villa S, Pinna GA, Fadda P, Fratta W. (1998). «Синтез и сродство к мю-опиоидным рецепторам новой серии нитрозамещенных производных 3,8-диазабицикло [3.2.1] октана». Farmaco. 53 (8–9): 557–62. Дои:10.1016 / s0014-827x (98) 00065-2. PMID 10081818.
- ^ Cignarella G, Barlocco D, Vianello P, Villa S, Pinna GA, Fadda P и др. (1998). «Бензоконденсированные производные как жесткие аналоги мю-опиоидных агонистов 3 (8) -циннамил-8 (3) -пропионил-3,8-диазабицикло [3.2.1] октанов: синтез, моделирование и сродство». Farmaco. 53 (10–11): 667–74. Дои:10.1016 / s0014-827x (98) 00084-6. PMID 10205853.
- ^ Вианелло П., Альбинати А., Пинна Г.А., Лавеккья А., Маринелли Л., Бореа П.А. и др. (Июнь 2000 г.). «Синтез, молекулярное моделирование и сродство к опиоидным рецепторам 9,10-диазатрицикло [4.2.1.1 (2,5)] деканов и 2,7-диазатрицикло [4.4.0. 0 (3,8)] деканов, структурно связанных с 3 , 8-диазабицикло [3.2.1] октаны ». Журнал медицинской химии. 43 (11): 2115–23. Дои:10.1021 / jm991140q. PMID 10841790.
- ^ Пинна Г.А., Муринедду Г., Курзу М.М., Вилла С., Вианелло П., Бореа П.А. и др. (Август 2000 г.). «Синтез, моделирование и сродство к мю-опиоидным рецепторам N-3 (9) -арилпропенил-N-9 (3) -пропионил-3,9-диазабицикла». Farmaco. 55 (8): 553–62. Дои:10.1016 / s0014-827x (00) 00036-7. PMID 11132733.
- ^ Pinna GA, Cignarella G, Loriga G, Murineddu G, Mussinu JM, Ruiu S и др. (Июнь 2002 г.). «N-3 (9) -арилпропенил-N-9 (3) -пропионил-3,9-диазабицикло [3.3.1] нонаны как агонисты мю-опиоидного рецептора. Влияние на мю-аффинность модификаций арилалкенильной цепи». Биоорганическая и медицинская химия. 10 (6): 1929–37. Дои:10.1016 / s0968-0896 (01) 00436-9. PMID 11937351.
- ^ Pinna GA, Cignarella G, Ruiu S, Loriga G, Murineddu G, Villa S и др. (Сентябрь 2003 г.). «Синтез новых диазатрициклодеканов (DTD). Влияние структурных изменений на С3 'аллильном конце и фенильном кольце коричной цепи на аффинность мю-рецептора и опиоидную антиноцицепцию». Биоорганическая и медицинская химия. 11 (18): 4015–26. Дои:10.1016 / s0968-0896 (03) 00373-0. PMID 12927864.
- ^ Loriga G, Manca I, Murineddu G, Chelucci G, Villa S, Gessi S и др. (Февраль 2006 г.). «Синтез 3,6-диазабицикло [3.1.1] гептанов в качестве новых лигандов для опиоидных рецепторов». Биоорганическая и медицинская химия. 14 (3): 676–91. Дои:10.1016 / j.bmc.2005.09.045. PMID 16243530.
