Селенол - Википедия - Selenol
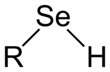
Селенолы находятся органические соединения которые содержат функциональная группа с возможностью подключения C–Se -ЧАС. Селенолы иногда также называют селеномеркаптаны и селенотиолы. Селенолы - один из основных классов селенорганические соединения. Самый известный член группы - аминокислота селеноцистеин.
Структура, сцепление, свойства
Селенолы структурно похожи на тиолы, но облигация C-Se примерно на 8% длиннее на 196 часов вечера. Угол C – Se – H приближается к 90 °. Связь включает почти чистые p-орбитали на Se, следовательно, углы около 90. Se – H энергия связи слабее связи S – H, следовательно, селенолы легко окисляются и служат донорами H-атома. Связь Se-H намного слабее, чем связь S-H, что отражено в их соответствующих энергия диссоциации связи (BDE). Для C6ЧАС5Se-H, БДЭ составляет 326 кДж / моль, а для C6ЧАС5S-H, БДЭ составляет 368 кДж / моль.[1]
Селеноловые кислоты примерно в 1000 раз сильнее тиолов: pKа CH3SeH составляет 5,2 против 8,3 для CH3SH. Депротонирование дает селенолят анион, RSe−, большинство из которых являются высоконуклеофильными и быстро окисляются воздухом.[2]
Температуры кипения селенолов обычно немного выше, чем у тиолов. Это можно объяснить возросшим значением более сильных соединение Ван-дер-Ваальса для более крупных атомов. Летучие селенолы имеют очень неприятный запах.
Приложения и возникновение
Селенолы имеют несколько коммерческих применений, ограниченных высокой токсичностью селена, а также чувствительностью связи Se – H. Их сопряженные основания, селенолаты, имеют ограниченное применение в органический синтез.

Биохимическая роль
Селенолы важны в определенных биологических процессах. Три фермента, обнаруженные у млекопитающих, содержат селенолы в своих активных центрах: глутатионпероксидаза, йодтиронин дейодиназа, и тиоредоксинредуктаза. Селенолы в этих белках являются частью незаменимая аминокислота селеноцистеин.[2] Селенолы действуют как восстановители, давая селененовая кислота производные (RSe – OH), которые, в свою очередь, повторно восстанавливаются тиолсодержащими ферментами. Метанселенол (обычно называемый «метилселенол») (CH3SeH), которые можно получить in vitro путем инкубации селенометионин с бактериальным метионин гамма-лиаза (МЕТаза) фермент путем биологического метилирования селенид-иона или in vivo путем восстановления метанселениновой кислоты (CH3SeO2H), был призван объяснить противораковую активность некоторых селенорганических соединений.[3][4][5] Прекурсоры метанселенола активно исследуются в профилактике и лечении рака. В этих исследованиях обнаружено, что метанселенол более биологически активен, чем этанселенол или 2-пропанезеленол.[6]
Подготовка
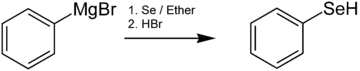
Селенолы обычно получают по реакции литийорганические реагенты или же Реактивы Гриньяра с элементарным Se. Например, бензолселенол порождается реакцией фенилмагний бромид селеном с последующим подкислением:[7]
Другой препаративный путь к селенолам включает алкилирование из селеномочевина с последующим гидролизом. Селенолы часто образуются путем восстановления диселенидов с последующим протонированием полученного селеноата:
- 2 RSeSeR + 2 LiHB (C2ЧАС5)3 → 2 RSeLi + 2 B (C2ЧАС5)3 + H2
- RSeLi + HCl → RSeH + LiCl
Диметилдиселенид можно легко восстановить в клетках до метанселенола.[8]
Реакции
Селенолы легко окисляются до диселенидов, соединений, содержащих связь Se-Se. Например, обработка бензолезеленола бромом дает дифенилдиселенид.
- 2 С6ЧАС5SeH + Br2 → (C6ЧАС5Se)2 + 2 HBr
В присутствии основания селенолы легко алкилируются с образованием селенидов. Эта связь иллюстрируется метилирование метанселенола, чтобы дать диметилселенид.
Безопасность
Селенорганические соединения (или любое соединение селена) являются кумулятивными ядами, несмотря на то, что следовые количества селена необходимы для здоровья.
Смотрите также
Рекомендации
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 0-8493-0487-3.
- ^ а б Wessjohann, L.A .; Schneider, A .; Аббас, М .; Брандт, В. «Селен в химии и биохимии в сравнении с серой» Biol. Chem., Vol. 388. С. 997–1006, 2007. Дои:10.1515 / BC.2007.138
- ^ Zeng, H .; Briske-Anderson, M .; Wu, M .; Мойер, М. П. Метилселенол, метаболит селена, играет общие и разные роли в пролиферации раковых клеток толстой кишки HCT116 и доброкачественных клеток толстой кишки NCM460, Питание и рак 2012, 64, 128–135. Дои: 10.1080/01635581.2012.630555
- ^ Fernandes, A.P .; Валленберг, М .; Гандин, В .; Misra1, S .; Marzano, C .; Rigobello, M. P .; Kumar, S .; Бьорнстедт, М. «Метилселенол, образованный спонтанным метилированием селенида, является более предпочтительным субстратом селена по сравнению с системами тиоредоксина и глутаредоксина», PLoS ONE 2012, 7, e50727. Дои:10.1371 / journal.pone.0050727
- ^ Ip, C .; Dong, Y .; Гантер, Х. Э. "Новые концепции в химиопрофилактике селеном". Метастаз рака Rev. 2002, 21, 281–289.
- ^ Zuazo, A .; Плано, Д .; Ansó, E .; Lizarraga, E .; Шрифт, M .; Ируджо, J.J.M. «Цитотоксическая и проапотическая активность производных имидоселенокарбамата зависит от высвобождения метилселенола», Chem. Res. Toxicol. 2012, 25, 2479–2489. Дои:10.1021 / tx300306t
- ^ Фостер, Д. Г. (1955). «Селенофенол». Органический синтез.; Коллективный объем, 3, п. 771
- ^ Gabel-Jensen, C .; Lunoe, K .; Гаммелгаард, Б. «Образование метилселенола, диметилселенида и диметилдиселенида в моделях метаболизма in vitro, определяемых методом ГХ-МС в свободном пространстве». Металломика 2010, 2, 167–173.