Моноклональные антитела - Monoclonal antibody
А моноклональное антитело (mAb или же моАб) является антитело сделан клонирование уникальный лейкоцит. Все последующие антитела, полученные таким образом, восходят к уникальной родительской клетке.
Моноклональный антитела могут иметь одновалентный близость, привязка только к тому же эпитоп (часть антиген который распознается антителом). В отличие, поликлональные антитела связываются с несколькими эпитопами и обычно образуются несколькими разными антителами, секретирующими плазматическая ячейка родословные. Биспецифические моноклональные антитела также могут быть созданы путем увеличения терапевтических мишеней одного моноклонального антитела до двух эпитопов.
Можно получить моноклональные антитела, которые специфически связываются практически с любым подходящим веществом; затем они могут служить для его обнаружения или очистки. Эта возможность стала важным инструментом в биохимия, молекулярная биология, и лекарство.
История
Роль моноклональных антител была впервые постулирована в начале 20 века. иммунолог Пол Эрлих, предложившего идею медицинского Зауберкугель, а "Магическая пуля ". Это было бы соединение, которое можно было бы сделать так, чтобы избирательно воздействовать на болезнетворный организм, что позволило бы токсину для этого организма доставляться вместе с ним. Он и Эли Мечников получил 1908 Нобелевская премия по физиологии и медицине для этой работы.
В 1970-х годах В-клеточный рак множественная миелома был известен. Было понятно, что все эти злокачественные B-клетки продуцируют один тип антител (a парапротеин ). Это использовалось для изучения структуры антител, но пока не было возможности получить идентичные антитела, специфичные для данного антиген.[3]:324
Производство моноклональных антител с участием гибридных клеток человека и мыши было впервые описано Джеррольд Швабер в 1973 г.[4] Эта работа по-прежнему широко цитируется среди тех, кто использует гибридомы.[5]
В 1975 г. Жорж Кёлер и Сезар Мильштейн удалось осуществить слияние линий миеломных клеток с В-клетки создавать гибридомы которые могли производить антитела, специфичные к известным антигенам, и которые были иммортализованы.[6] Они и Нильс Кай Йерн поделился Нобелевская премия по физиологии и медицине в 1984 г. за открытие.[6]
В 1988 г. Грег Винтер и его команда первыми разработали методы очеловечивать моноклональные антитела,[7] устранение реакций, которые вызывают у некоторых пациентов многие моноклональные антитела.
В 2018 г. Джеймс П. Эллисон и Тасуку Хондзё получил Нобелевскую премию по физиологии и медицине за открытие лечения рака путем подавления негативной иммунной регуляции с использованием моноклональных антител, предотвращающих ингибирующие связи.[8]
Производство




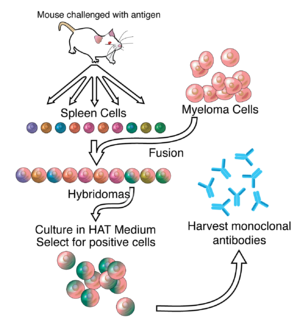
Развитие гибридомы
Большая часть работы по производству моноклональных антител уходит корнями в производство гибридом, которое включает идентификацию антигенспецифических клеток плазмы / плазмобластов (ASPC), которые продуцируют антитела, специфичные к интересующему антигену, и сплавление эти клетки с миелома клетки.[6] В-клетки кролика можно использовать для формирования гибридома кролика. Полиэтиленгликоль используется для слияния соседних плазматических мембран,[9] но вероятность успеха низкая, поэтому используется селективная среда, в которой могут расти только слитые клетки. Это возможно потому, что миеломные клетки утратили способность синтезировать гипоксантин-гуанин-фосфорибозилтрансфераза (HGPRT), фермент, необходимый для спасательный синтез нуклеиновых кислот. Отсутствие HGPRT не является проблемой для этих клеток, если только синтез пуринов de novo путь также нарушен. Воздействие на клетки аминоптерин (а фолиевая кислота аналог, подавляющий дигидрофолатредуктаза, DHFR), делает их неспособными использовать путь de novo и полностью ауксотрофный за нуклеиновые кислоты, поэтому для выживания требуются добавки.
Селективная питательная среда называется Шляпа средняя потому что он содержит гипоксантин, аминоптерин и тимидин. Эта среда является селективной для слитых (гибридома ) клетки. Неслитые миеломные клетки не могут расти, потому что в них отсутствует HGPRT, и поэтому они не могут реплицировать свою ДНК. Неслитые клетки селезенки не могут расти бесконечно из-за их ограниченной продолжительности жизни. Только слитые гибридные клетки, называемые гибридомами, способны бесконечно расти в среде, потому что партнер клетки селезенки поставляет HGPRT, а партнер миеломы имеет черты, которые делают его бессмертным (подобно раковой клетке).
Затем эту смесь клеток разбавляют и выращивают клоны из одиночных родительских клеток в лунках для микротитрования. Затем антитела, секретируемые различными клонами, исследуются на их способность связываться с антигеном (с помощью такого теста, как ELISA или антигенный микроматричный анализ) или иммуно-точечный блот. Затем выбирается наиболее продуктивный и стабильный клон для использования в будущем.
Гибридомы можно выращивать неограниченно долго в подходящей среде для культивирования клеток. Их также можно вводить мышам (в брюшная полость, окружающие кишечник). Там они производят опухоли, выделяющие богатую антителами жидкость, называемую асцит жидкость.
Среда должна быть обогащена во время in vitro отбор для дальнейшего содействия росту гибридомы. Это может быть достигнуто за счет использования слоя питающих фиброцитов или дополнительной среды, такой как бриклон. Можно использовать культуральные среды, кондиционированные макрофагами. Производство в культуре клеток обычно предпочтительнее, поскольку метод асцита болезнен для животного. Если существуют альтернативные методы, считается, что асцит. неэтичный.[10]
Новая технология разработки mAb
Недавно было разработано несколько технологий моноклональных антител,[11] Такие как фаговый дисплей,[12] культура единичных В-клеток,[13] амплификация отдельных клеток из различных популяций В-клеток[14][15][16][17][18] и технологии исследования одиночных плазматических клеток. В отличие от традиционной гибридомной технологии, новые технологии используют методы молекулярной биологии для амплификации тяжелых и легких цепей генов антител с помощью ПЦР и продуцирования в системах бактерий или млекопитающих с рекомбинантный технологии. Одно из преимуществ новых технологий применимо к нескольким животным, таким как кролик, лама, курица и другие обычные экспериментальные животные в лаборатории.
Очищение
После получения образца среды культивируемых гибридом или образца асцитной жидкости необходимо экстрагировать желаемые антитела. Загрязнители образцов клеточной культуры состоят в основном из компонентов среды, таких как факторы роста, гормоны и трансферрины. Напротив, in vivo образец может иметь антитела хозяина, протеазы, нуклеазы, нуклеиновые кислоты и вирусы. В обоих случаях другие выделения гибридом, такие как цитокины может присутствовать. Также может быть бактериальное заражение и, как следствие, эндотоксины которые секретируются бактериями. В зависимости от сложности среды, необходимой для культивирования клеток, и, следовательно, контаминантов, тот или иной метод (in vivo или же in vitro) может быть предпочтительнее.
Сначала образец кондиционируется или готовится к очистке. Клетки, клеточный дебрис, липиды и свернувшийся материал сначала удаляются, обычно центрифугированием с последующим фильтрация с фильтром 0,45 мкм. Эти большие частицы могут вызвать явление, называемое засорение мембраны на более поздних стадиях очистки. Кроме того, концентрация продукта в образце может быть недостаточной, особенно в случаях, когда желаемое антитело продуцируется линией клеток с низким уровнем секреции. Таким образом, образец концентрируется ультрафильтрация или же диализ.
Большинство заряженных примесей обычно анионы такие как нуклеиновые кислоты и эндотоксины. Их можно разделить ионообменная хроматография.[19] Либо катион обмен хроматография используется на достаточно низком уровне pH что желаемое антитело связывается с колонкой во время протекания анионов, или анионообменная хроматография используется при достаточно высоком pH, чтобы нужное антитело протекало через колонку, а анионы связывались с ней. Различные белки также могут быть разделены вместе с анионами на основе их изоэлектрическая точка (число Пи). В белках изоэлектрическая точка (pI) определяется как pH, при котором белок не имеет чистого заряда. Когда pH> pI, белок имеет чистый отрицательный заряд, а когда pH
Трансферрин вместо этого можно удалить эксклюзионная хроматография. Этот метод является одним из наиболее надежных методов хроматографии. Поскольку мы имеем дело с белками, такие свойства, как заряд и сродство, не согласованы и меняются в зависимости от pH, поскольку молекулы протонируются и депротонируются, в то время как размер остается относительно постоянным. Тем не менее, у него есть такие недостатки, как низкое разрешение, малая емкость и низкая элюирование раз.
Более быстрый одноэтапный метод разделения - это белок A / G аффинная хроматография. Антитело избирательно связывается с белком A / G, поэтому достигается высокий уровень чистоты (обычно> 80%). Однако этот метод может быть проблематичным для антител, которые легко повредить, поскольку обычно используются суровые условия. Низкий pH может разорвать связи и удалить антитело из колонки. Помимо возможного воздействия на продукт, низкий pH может вызвать утечку самого белка A / G из колонки и его появление в элюируемом образце. Доступны буферные системы для щадящей элюции, в которых используются высокие концентрации солей, чтобы избежать воздействия на чувствительные антитела низкого pH. Стоимость также является важным фактором при использовании этого метода, поскольку иммобилизованный белок A / G является более дорогой смолой.
Для достижения максимальной чистоты за одну стадию можно провести аффинную очистку с использованием антигена для обеспечения специфичности антитела. В этом методе антиген, используемый для создания антитела, ковалентно присоединяется к агароза поддерживать. Если антиген пептид, он обычно синтезируется с помощью терминала цистеин, что позволяет селективно прикрепляться к белку-носителю, например KLH во время разработки и для поддержки очистки. Затем содержащую антитело среду инкубируют с иммобилизованным антигеном либо партиями, либо по мере того, как антитело пропускают через колонку, где оно избирательно связывается и может удерживаться, пока примеси смываются. Затем используют элюирование буфером с низким pH или более мягким буфером для элюции с высоким содержанием соли для извлечения очищенного антитела из носителя.
Гетерогенность антител
Гетерогенность продукта является обычным явлением для моноклональных антител и других рекомбинантных биологических продуктов и обычно вводится либо в начале процесса экспрессии, либо ниже в процессе производства.[нужна цитата ]
Эти варианты обычно являются агрегатами, дезамидирование товары, гликозилирование варианты, окисленные боковые цепи аминокислот, а также амино- и карбоксильные концевые аминокислоты.[20] Эти, казалось бы, незначительные структурные изменения могут повлиять на доклиническую стабильность и оптимизацию процесса, а также на эффективность терапевтического продукта. биодоступность и иммуногенность. Общепринятый метод очистки технологических потоков моноклональных антител включает улавливание целевого продукта с помощью белок А, элюирование, подкисление для инактивации потенциальных вирусов млекопитающих с последующим ионная хроматография, сначала с анионные шарики а затем с катионными шариками.[нужна цитата ]
Вытесняющая хроматография использовался для идентификации и характеристики этих часто невидимых вариантов в количествах, подходящих для последующих схем доклинической оценки, таких как животные фармакокинетический исследования.[21][22] Знания, полученные на этапе доклинической разработки, имеют решающее значение для лучшего понимания качества продукции и обеспечивают основу для управления рисками и повышения гибкости регулирования. Недавнее Управление по санитарному надзору за качеством пищевых продуктов и медикаментов Качество по дизайну Инициатива пытается предоставить руководство по разработке и облегчить проектирование продуктов и процессов, которые максимизируют профиль эффективности и безопасности, одновременно повышая технологичность продукта.[23]
Рекомбинантный
Производство рекомбинантный моноклональные антитела включают репертуар клонирование, CRISPR / Cas9, или же фаговый дисплей /дрожжевой дисплей технологии.[24] Конструирование рекомбинантных антител включает производство антител с использованием вирусы или же дрожжи, а не мышей. Эти методы основаны на быстром клонировании генных сегментов иммуноглобулина для создания библиотек антител с немного разными аминокислота последовательности, из которых могут быть выбраны антитела с желаемой специфичностью.[25] Библиотеки фаговых антител представляют собой вариант библиотек фаговых антигенов.[26] Эти методы можно использовать для повышения специфичности, с которой антитела распознают антигены, их стабильности в различных условиях окружающей среды, их терапевтической эффективности и их детектируемости в диагностических приложениях.[27] Камеры ферментации использовались для крупномасштабного производства антител.
Химерные антитела
Хотя мышиные и человеческие антитела структурно схожи, различий между ними было достаточно, чтобы вызвать иммунный ответ, когда мышиный моноклональные антитела вводили людям, что привело к их быстрому удалению из крови, а также к системным воспалительным эффектам и выработке человеческие антимышиные антитела (ХАМА).
Рекомбинантная ДНК изучается с конца 1980-х годов для увеличения времени пребывания. В одном подходе ДНК мыши, кодирующая связывающую часть моноклонального антитела, была объединена с ДНК, продуцирующей антитела человека, в живых клетках. Выражение этого "химерный "или" гуманизированная "ДНК через культура клеток дали частично мышиные, частично человеческие антитела.[28][29]
Человеческие антитела

С момента открытия возможности образования моноклональных антител ученые нацелены на создание от корки до корки человеческие продукты для уменьшения побочных эффектов гуманизированных или химерных антител. Выявлено несколько успешных подходов: трансгенные мыши,[30] фаговый дисплей[12] и клонирование единичных В-клеток:[11]
По состоянию на ноябрь 2016 г. тринадцать из девятнадцати от корки до корки Терапевтические препараты человеческих моноклональных антител, представленные на рынке, были получены с использованием технологии трансгенных мышей.
К числу принимающих организаций, продающих трансгенные технологии, относятся:
- Медарекс - которая продавала платформу UltiMab. Medarex была приобретена в июле 2009 г. Бристоль Майерс Сквибб[31]
- Abgenix - продавец технологии Xenomouse. Abgenix была приобретена в апреле 2006 г. Amgen.[32]
- Regeneron Pharmaceuticals Технология VelocImmune.[33]
- Kymab - кто продает свою технологию Kymouse.[34]
- Откройте платформу OmniRat ™ и OmniMouse ™ компании Monoclonal Technology.[35]
- TRIANNI, Inc. - которые продают свои ТРИАННИ Платформа мыши.[36]
- Ablexis, LLC - которые продают свою платформу для мышей AlivaMab.[37]
Фаговый дисплей могут быть использованы для экспрессии вариабельных доменов антител на белках оболочки нитчатых фагов (Главный белок оболочки фага ).[38][39][40] Эти антитела фагового дисплея можно использовать для различных исследовательских целей.[41][42] ProAb было объявлено в декабре 1997 г.[43] и включал высокопроизводительный скрининг библиотек антител против пораженной и здоровой ткани, в то время как Проксимол использовал свободнорадикальную ферментативную реакцию для мечения молекул в непосредственной близости от данного белка.[44][45]
Моноклональные антитела одобрены для лечения рак, сердечно-сосудистые заболевания, воспалительные заболевания, дегенерация желтого пятна, отторжение трансплантата, рассеянный склероз и вирусная инфекция.
В августе 2006 г. Фармацевтические исследования и производители Америки сообщили, что у американских компаний было 160 различных моноклональных антител в клинических испытаниях или ожидающих одобрения Управление по контролю за продуктами и лекарствами.[46]
Расходы
Моноклональные антитела дороже в производстве, чем небольшие молекулы, из-за сложных процессов и общего размера молекул, и все это в дополнение к огромным расходам на исследования и разработки, связанным с предоставлением пациентам нового химического соединения. Цены на них позволяют производителям окупить, как правило, большие инвестиционные затраты, а там, где нет контроля над ценами, например в США, цены могут быть выше, если они обеспечивают большую ценность. Семь Питтсбургский университет исследователи пришли к выводу: «Годовая цена лечения с применением mAb в онкологии и гематологии примерно на 100 000 долларов выше, чем при других болезненных состояниях», сравнивая их на уровне пациента с ценами на сердечно-сосудистые или метаболические нарушения, иммунологию, инфекционные заболевания, аллергию и офтальмологию. .[47]
Приложения
Диагностические тесты
После того, как моноклональные антитела к данному веществу были произведены, их можно использовать для обнаружения присутствия этого вещества. Белки можно обнаружить с помощью Вестерн-блоттинг и иммуно точечный блот тесты. В иммуногистохимия моноклональные антитела можно использовать для обнаружения антигенов в фиксированных срезах ткани, и аналогично, иммунофлуоресценция может использоваться для обнаружения вещества либо в замороженном срезе ткани, либо в живых клетках.
Аналитическое и химическое использование
Антитела также можно использовать для очистки их целевых соединений от смесей, используя метод иммунопреципитация.
Терапевтическое использование
Терапевтические моноклональные антитела действуют посредством нескольких механизмов, таких как блокирование функций целевых молекул, индуцируя апоптоз в клетках, которые экспрессируют мишень, или путем модуляции сигнальных путей.[48][49]
Лечение рака
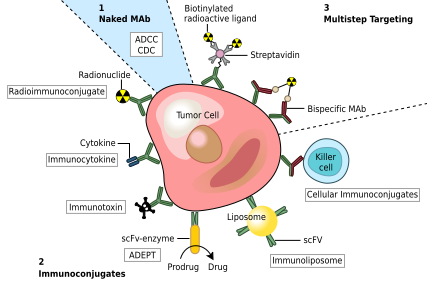
Одно возможное лечение рак включает моноклональные антитела, которые связываются только со специфическими для раковых клеток антигены и вызвать иммунная реакция против раковой клетки-мишени. Такие mAb можно модифицировать для доставки токсин, радиоизотоп, цитокин или другой активный конъюгат или для разработки биспецифические антитела которые могут связать их Fab регионы как нацеленный на антиген, так и на конъюгат или эффекторную клетку. Каждое интактное антитело может связываться с клеточными рецепторами или другими белками с помощью Fc регион.
МАТ, одобренные FDA для лечения рака, включают:[51]
Аутоиммунные заболевания
Моноклональные антитела, используемые для аутоиммунные заболевания включают инфликсимаб и адалимумаб, которые эффективны в ревматоидный артрит, болезнь Крона, язвенный колит и анкилозирующий спондилоартрит своей способностью связывать и подавлять TNF-α.[52] Базиликсимаб и даклизумаб подавлять Ил-2 на активированном Т-клетки и тем самым помочь предотвратить острую отказ трансплантации почек.[52] Омализумаб подавляет человека иммуноглобулин E (IgE) и полезен при лечении аллергических реакций средней и тяжелой степени. астма.
Примеры терапевтических моноклональных антител
Моноклональные антитела для исследовательских целей можно найти непосредственно у поставщиков антител или с помощью специальной поисковой системы, например CiteAb. Ниже приведены примеры клинически важных моноклональных антител.
| Главная категория | Тип | Заявление | Механизм / цель | Режим |
|---|---|---|---|---|
| Анти- воспалительный | инфликсимаб[52] | подавляет TNF-α | химерный | |
| адалимумаб | подавляет TNF-α | человек | ||
| базиликсимаб[52] |
| подавляет Ил-2 на активированном Т-клетки | химерный | |
| даклизумаб[52] |
| подавляет Ил-2 на активированном Т-клетки | очеловеченный | |
| омализумаб |
| подавляет человека иммуноглобулин E (IgE) | очеловеченный | |
| Противораковые | гемтузумаб[52] |
| нацелен на антиген миелоидной клеточной поверхности CD33 на лейкемия клетки | очеловеченный |
| алемтузумаб[52] | нацелен на антиген CD52 на Т- и В-лимфоциты | очеловеченный | ||
| ритуксимаб[52] |
| нацелены на фосфопротеин CD20 на В-лимфоциты | химерный | |
| трастузумаб |
| нацелен на HER2 / neu (erbB2) рецептор | очеловеченный | |
| нимотузумаб |
| EGFR ингибитор | очеловеченный | |
| цетуксимаб |
| EGFR ингибитор | химерный | |
| бевацизумаб & ранибизумаб |
| подавляет VEGF | очеловеченный | |
| Противораковые и противовирусные | бавитуксимаб[53] |
| иммунотерапия, цели фосфатидилсерин[53] | химерный |
| Другой | паливизумаб[52] |
| ингибирует слитый белок RSV (F) | очеловеченный |
| абциксимаб[52] |
| подавляет рецептор GpIIb / IIIa на тромбоциты | химерный |
Побочные эффекты
Несколько моноклональных антител, таких как Бевацизумаб и Цетуксимаб, может вызывать различные побочные эффекты.[54] Эти побочные эффекты можно разделить на общие и серьезные.[55]
Некоторые общие побочные эффекты включают:
Среди возможных серьезных побочных эффектов:
- Анафилаксия
- Кровотечение
- Артериальные и венозные тромбы
- Аутоиммунный тиреоидит
- Гипотиреоз
- Гепатит
- Сердечная недостаточность
- Рак
- Анемия
- Снижение лейкоцитов
- Стоматит
- Энтероколит
- Перфорация желудочно-кишечного тракта
- Мукозит[56]
Смотрите также
- Аффимер
- Миметик антител
- Аптамер
- Иммунотоксины, которые иногда используют моноклональные антитела в качестве механизма нацеливания
- Список моноклональных антител
- Терапия моноклональными антителами
- Номенклатура моноклональных антител
- Поликлональные антитела
- Журнал моноклональных антител
Рекомендации
- ^ «Цитохром P450 опосредованный лекарственный препарат и метаболизм канцерогенов с использованием моноклональных антител». home.ccr.cancer.gov. Получено 2018-04-02.
- ^ Гельбоин Х.В., Краус К.В., Гонсалес Ф.Дж., Ян Т.Дж. (ноябрь 1999 г.). «Ингибирующие моноклональные антитела к ферментам цитохрома P450 человека: новый путь для открытия лекарств». Тенденции в фармакологических науках. 20 (11): 432–8. Дои:10.1016 / S0165-6147 (99) 01382-6. PMID 10542439.
- ^ Tansey EM, Catterall PP (июль 1994 г.). «Моноклональные антитела: свидетельский семинар по современной истории медицины». История болезни. 38 (3): 322–7. Дои:10.1017 / s0025727300036632. ЧВК 1036884. PMID 7934322.
- ^ Швабер Дж, Коэн EP (август 1973 г.). «Гибридный клон соматических клеток человека x мыши, секретирующий иммуноглобулины обоих родительских типов». Природа. 244 (5416): 444–7. Дои:10.1038 / 244444a0. PMID 4200460. S2CID 4171375.
- ^ Камброзио А., Китинг П. (1992). «Между фактом и техникой: истоки гибридомной технологии». Журнал истории биологии. 25 (2): 175–230. Дои:10.1007 / BF00162840. PMID 11623041. S2CID 45615711.
- ^ а б c Marks, LV. «История Сезара Мильштейна и моноклональных антител». WhatisBiotechnology.org. Получено 23 сентября 2020.
- ^ Рихманн Л., Кларк М., Вальдманн Х., Винтер Г. (март 1988 г.). «Преобразование человеческих антител для терапии». Природа. 332 (6162): 323–7. Bibcode:1988Натура.332..323р. Дои:10.1038 / 332323a0. PMID 3127726. S2CID 4335569.
- ^ Altmann DM (ноябрь 2018 г.). «Работа, достойная Нобелевской премии: иммунология рака и использование иммунитета к неоантигенам опухоли». Иммунология. 155 (3): 283–284. Дои:10.1111 / imm.13008. ЧВК 6187215. PMID 30320408.
- ^ Ян J1, Шен MH. Слияние клеток, опосредованное полиэтиленгликолем. Методы Мол биол. 2006; 325: 59-66.
- ^ Комитет Национального исследовательского совета (США) по методам получения моноклональных антител. Рекомендация 1: Краткое содержание: Производство моноклональных антител. Вашингтон (округ Колумбия): National Academies Press (США); 1999 г. ISBN 978-0-309-07511-4
- ^ а б c Хо М (июнь 2018). "Первая редакционная статья: В поисках волшебных пуль". Антитела терапия. 1 (1): 1–5. Дои:10.1093 / abt / tby001. ЧВК 6086361. PMID 30101214.
- ^ а б Хо М., Фенг М., Фишер Р.Дж., Рейдер С., Пастан I (май 2011 г.). «Новое высокоаффинное человеческое моноклональное антитело к мезотелину». Международный журнал рака. 128 (9): 2020–30. Дои:10.1002 / ijc.25557. ЧВК 2978266. PMID 20635390.
- ^ Сибер С., Рос Ф., Тори И., Тифенталер Г., Калуза К., Лифке В. и др. (2014). «Надежная высокопроизводительная платформа для создания функциональных рекомбинантных моноклональных антител с использованием кроличьих В-клеток из периферической крови». PLOS ONE. 9 (2): e86184. Bibcode:2014PLoSO ... 986184S. Дои:10.1371 / journal.pone.0086184. ЧВК 3913575. PMID 24503933.
- ^ Wardemann H, Yurasov S, Schaefer A, Young JW, Meffre E, Nussenzweig MC (сентябрь 2003 г.). «Преобладающая продукция аутоантител ранними предшественниками В-клеток человека». Наука. 301 (5638): 1374–7. Bibcode:2003Наука ... 301.1374W. Дои:10.1126 / science.1086907. PMID 12920303. S2CID 43459065.
- ^ Koelsch K, Zheng NY, Zhang Q, Duty A, Helms C, Mathias MD и др. (Июнь 2007 г.). «Зрелые В-клетки класса, переведенные на IgD, обладают аутореактивностью у здоровых людей». Журнал клинических исследований. 117 (6): 1558–65. Дои:10.1172 / JCI27628. ЧВК 1866247. PMID 17510706.
- ^ Смит К., Гарман Л., Враммерт Дж., Чжэн Нью-Йорк, Капра Дж. Д., Ахмед Р., Уилсон П.С. (01.01.2009). «Быстрое образование полностью человеческих моноклональных антител, специфичных к вакцинационному антигену». Протоколы природы. 4 (3): 372–84. Дои:10.1038 / nprot.2009.3. ЧВК 2750034. PMID 19247287.
- ^ Duty JA, Szodoray P, Zheng NY, Koelsch KA, Zhang Q, Swiatkowski M и др. (Январь 2009 г.). «Функциональная анергия в субпопуляции наивных В-клеток от здоровых людей, которые экспрессируют аутореактивные рецепторы иммуноглобулинов». Журнал экспериментальной медицины. 206 (1): 139–51. Дои:10.1084 / jem.20080611. ЧВК 2626668. PMID 19103878.
- ^ Хуанг Дж., Дориа-Роуз Н.А., Лонго Н.С., Лауб Л., Линь С.Л., Тюрк Э. и др. (Октябрь 2013). «Выделение человеческих моноклональных антител из В-клеток периферической крови». Протоколы природы. 8 (10): 1907–15. Дои:10.1038 / nprot.2013.117. ЧВК 4844175. PMID 24030440.
- ^ Власак Дж., Ионеску Р. (декабрь 2008 г.). «Неоднородность моноклональных антител, выявленная зарядочувствительными методами». Текущая фармацевтическая биотехнология. 9 (6): 468–81. Дои:10.2174/138920108786786402. PMID 19075686.
- ^ Бек А., Вурч Т., Байи С., Корвайя Н. (май 2010 г.). «Стратегии и проблемы для следующего поколения терапевтических антител». Обзоры природы. Иммунология. 10 (5): 345–52. Дои:10.1038 / nri2747. PMID 20414207. S2CID 29689097.
- ^ Khawli LA, Goswami S, Hutchinson R, Kwong ZW, Yang J, Wang X и др. (2010). «Варианты заряда в IgG1: выделение, характеристика, свойства связывания in vitro и фармакокинетика у крыс». mAbs. 2 (6): 613–24. Дои:10.4161 / мабс.2.6.13333. ЧВК 3011216. PMID 20818176.
- ^ Чжан Т., Бурре Дж., Кано Т. (август 2011 г.). «Выделение и характеристика вариантов заряда терапевтических антител с использованием катионообменной хроматографии замещения». Журнал хроматографии А. 1218 (31): 5079–86. Дои:10.1016 / j.chroma.2011.05.061. PMID 21700290.
- ^ Ратор А.С., Винкль Х (январь 2009 г.). «Дизайн для биофармацевтических препаратов». Природа Биотехнологии. 27 (1): 26–34. Дои:10.1038 / nbt0109-26. PMID 19131992. S2CID 5523554.
- ^ van der Schoot JM, Fennemann FL, Valente M, Dolen Y, Hagemans IM, Becker AM и др. (Август 2019 г.). «Функциональная диверсификация антител, продуцируемых гибридомами, с помощью геномной инженерии CRISPR / HDR». Достижения науки. 5 (8): eaaw1822. Дои:10.1126 / sciadv.aaw1822. ЧВК 6713500. PMID 31489367.
- ^ Сигель Д.Л. (январь 2002 г.). «Технология рекомбинантных моноклональных антител». Transfusion Clinique et Biologique. 9 (1): 15–22. Дои:10.1016 / S1246-7820 (01) 00210-5. PMID 11889896.
- ^ "Доктор Георгий Печеник". Выпускники LMB. Лаборатория молекулярной биологии (ЛКБ) MRC. 17 сентября 2009 г. Архивировано с оригинал 23 декабря 2012 г.. Получено 17 ноября 2012.
- ^ Шмитц У., Ферсмольд А, Кауфманн П, Франк Х.Г. (2000). «Фаговый дисплей: молекулярный инструмент для генерации антител - обзор». Плацента. 21 Дополнение A (Дополнение A): S106-12. Дои:10.1053 / plac.1999.0511. PMID 10831134.
- ^ Булианна Г.Л., Ходзуми Н., Шульман М.Дж. (1984). «Производство функциональных химерных антител мыши / человека». Природа. 312 (5995): 643–6. Дои:10.1038 / 312643a0. PMID 6095115. S2CID 4311503.
- ^ Chadd HE, Chamow SM (апрель 2001 г.). «Технология терапевтической экспрессии антител». Текущее мнение в области биотехнологии. 12 (2): 188–94. Дои:10.1016 / S0958-1669 (00) 00198-1. PMID 11287236.
- ^ Лонберг Н., Хусар Д. (1995). «Человеческие антитела трансгенных мышей». Международные обзоры иммунологии. 13 (1): 65–93. Дои:10.3109/08830189509061738. PMID 7494109.
- ^ «Бристол-Майерс покупает компанию Medarex Drugmaker за 2,4 миллиарда долларов (Обновление 3)».
- ^ «Amgen завершает приобретение Abgenix; приобретение дает Amgen полное право собственности на панитумумаб и устраняет роялти деносумаба».
- ^ «Архивная копия». Архивировано из оригинал 29 июня 2009 г.. Получено 28 июля, 2009.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Патентованная платформа антител». Архивировано из оригинал на 2013-02-03. Получено 2013-01-17.
- ^ «Естественно оптимизированные человеческие антитела».
- ^ «Патентованная платформа антител».
- ^ «Патентованная платформа антител».
- ^ Маккафферти Дж., Гриффитс А.Д., Винтер Дж., Чисвелл Д.Д. (декабрь 1990 г.). «Фаговые антитела: нитчатый фаг, демонстрирующий вариабельные домены антител». Природа. 348 (6301): 552–4. Bibcode:1990Натура.348..552М. Дои:10.1038 / 348552a0. PMID 2247164. S2CID 4258014.
- ^ Marks JD, Hoogenboom HR, Bonnert TP, McCafferty J, Griffiths AD, Winter G (декабрь 1991 г.). «Обходная иммунизация. Человеческие антитела из библиотек V-генов, отображаемые на фаге». Журнал молекулярной биологии. 222 (3): 581–97. Дои:10.1016 / 0022-2836 (91) 90498-У. PMID 1748994.
- ^ Кармен С., Джермутус Л. (июль 2002 г.). «Концепции фагового дисплея антител». Брифинги по функциональной геномике и протеомике. 1 (2): 189–203. Дои:10.1093 / bfgp / 1.2.189. PMID 15239904.
- ^ Осборн Дж. К. (2002). «Выбор антител по методу близости (ProxiMol)». Фаговый дисплей антител. Методы Мол. Биол. 178. С. 201–5. Дои:10.1385/1-59259-240-6:201. ISBN 978-1-59259-240-1. PMID 11968489.
- ^ Abeloff MD, Armitage JO, Niederhuber JE, Kastan MB, McKenna G (2008). «Терапевтические антитела и иммунологические конъюгаты». Клиническая онкология Абелова (4-е изд.). Эльзевир.
- ^ «Кембриджская технология антител». Архивировано из оригинал 28 сентября 2011 г.
- ^ Осборн Дж. К., Дербишир Э. Дж., Воган Т. Дж., Филд А. В., Джонсон К. С. (январь 1998 г.). «Отбор следопытов: выделение новых антител in situ». Иммунотехнология. 3 (4): 293–302. Дои:10.1016 / S1380-2933 (97) 10007-0. PMID 9530562.
- ^ «Современное состояние протеомных технологий». Архивировано из оригинал на 2011-10-08. Получено 2009-07-28.
- ^ Отчеты PhRMA выявляют более 400 биотехнологических препаратов в разработке. Pharmaceutical Technology, 24 августа 2006 г. Дата обращения 4 сентября 2006 г.
- ^ Эрнандес И., Ботт С.В., Патель А.С., Вольф К.Г., Хосподар А.Р., Сампаткумар С., Шранк WH (февраль 2018 г.). «Цены на терапию моноклональными антителами: выше, если они используются для лечения рака?». Американский журнал управляемой помощи. 24 (2): 109–112. PMID 29461857.
- ^ Бредвелд (Февраль 2000 г.). «Лечебные моноклональные антитела». Ланцет. 355 (9205): 735–40. Дои:10.1016 / S0140-6736 (00) 01034-5. PMID 10703815. S2CID 43781004.
- ^ Австралийский врач, назначающий наказание (2006) «Терапия моноклональными антителами при незлокачественных заболеваниях». Австралийский врач. 29 (5): 130–133. Дои:10.18773 / austprescr.2006.079.
- ^ Изменено из Картер П. (ноябрь 2001 г.). «Повышение эффективности лечения рака на основе антител». Обзоры природы. Рак. 1 (2): 118–29. Дои:10.1038/35101072. PMID 11905803. S2CID 10169378.
- ^ Такимото СН, Кальво Э. (01 января 2005 г.) «Принципы онкологической фармакотерапии» in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (ред.) Лечение рака
- ^ а б c d е ж грамм час я j Позвонил в HP (2003). Фармакология. Эдинбург: Черчилль Ливингстон. стр. 241, где приведены примеры инфликсимаба, базиликсимаба, абциксимаба, даклизумаба, паливусамаба, гемтузумаба, алемтузумаба и ритуксимаба, а также механизма и режима. ISBN 978-0-443-07145-4.
- ^ а б Персонал, Adis Insight. Бавитуксимаб профиль Последнее обновление: 27 января 2016 г.
- ^ «Моноклональные антитела для лечения рака | Американское онкологическое общество». www.cancer.org. Получено 2018-04-19.
- ^ «Лекарства с моноклональными антителами от рака: как они работают». Клиника Майо. Получено 2018-04-19.
- ^ а б «Моноклональные антитела: список, типы, побочные эффекты и использование FDA (рак)». MedicineNet. Получено 2018-04-19.
дальнейшее чтение
- 2019 Исторический обзор моноклональных антител в журнале Nature
- Моноклональные антитела, из онлайн-учебника биологии Джона В. Кимбалла.
внешняя ссылка
- Моноклональные + антитела в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Антитопедия, виртуальный репозиторий с открытым доступом, публикующий данные и комментарии о любых антителах, доступных научному сообществу.
- Справочник по очистке антител
| Библиотечные ресурсы о Моноклональные антитела |