Немевалонатный путь - Non-mevalonate pathway
В немевалонатный путь—Также появляется как мевалонат-независимый путь и 2-C-метил-D-эритрит 4-фосфат / 1-дезокси-D-ксилулоза 5-фосфат (MEP / DOXP) путь- альтернативный метаболический путь для биосинтез предшественников изопреноидов изопентенилпирофосфат (IPP) и диметилаллил пирофосфат (DMAPP).[1][2][3] В настоящее время предпочтительным названием для этого пути является Путь MEP, поскольку MEP является первым совершенным метаболитом на пути к IPP.
Биосинтез изопреноидных предшественников
Классический мевалонатный путь или же HMG-CoA редуктаза Путь - это метаболический путь биосинтеза изопреноидных предшественников, присутствующих у большинства высших эукариот и некоторых бактерий.[нужна цитата ] Это важно для продукции IPP и DMAPP, которые служат основой для биосинтеза изопреноид (терпеноид) молекулы, используемые в таких разнообразных процессах, как белок пренилирование, клеточная мембрана обслуживание, синтез гормоны, заякоривание белка и N-гликозилирование.[нужна цитата ]
Бактерии, растения и апикомплекс простейшие -Такие как малярия паразиты - способны производить изопреноид прекурсоров, использующих альтернативный путь, путь MEP, который является немевалонатный путь. В случае растений и некоторых простейших биосинтез IPP / DMAPP происходит в пластида органеллы.[4] Растения синтезируют предшественники изопреноидов, используя мевалонатный путь в цитоплазме и путь MEP в своих хлоропластах. Бактерии, которые используют этот путь, включают важные патогены, такие как Микобактерии туберкулеза.[5]
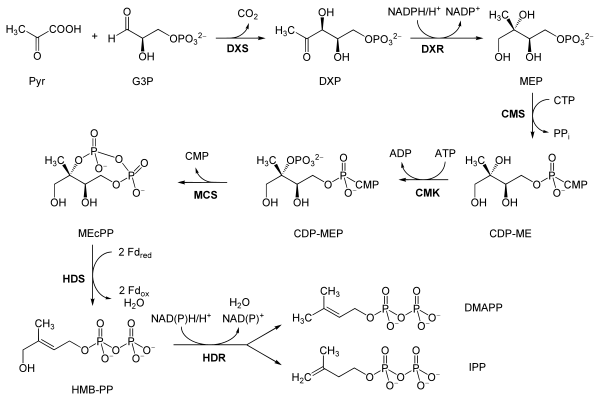
Реакции
Ниже приведены реакции немевалонатного пути, взятые в основном у Eisenreich и его сотрудников, за исключением тех случаев, когда жирные метки являются дополнительными местными сокращениями, помогающими связать таблицу со схемой выше:[7][6]
| Реагенты | Фермент | Товар | |
| Пируват (Pyr) и глицеральдегид-3-фосфат (G3P) | DOXP-синтаза (Dxs; DXP) | 1-дезокси-D-ксилулоза 5-фосфат (DOXP; DXP) |  |
| DOXP (DXP) | DXP редуктоизомераза (Dxr, IspC; DXR) | 2-C-метилэритритол 4-фосфат (MEP) |  |
| MEP | 2-C-метил-D-эритритол-4-фосфатцитидилилтрансфераза (YgbP, IspD; CMS) | 4-дифосфоцитидил-2-C-метилэритритол (CDP-ME) |  |
| CDP-ME | 4-дифосфоцитидил-2-C-метил-D-эритритолкиназа (YchB, IspE; CMK) | 4-дифосфоцитидил-2-C-метил-D-эритритол 2-фосфат (CDP-MEP) | |
| CDP-MEP | 2-C-метил-D-эритритол-2,4-циклодифосфатсинтаза (YgbB, IspF; MCS) | 2-C-метил-D-эритритол 2,4-циклодифосфат (MEcPP) |  |
| MEcPP | HMB-PP синтаза (GcpE, IspG; HDS) | (E) -4-Гидрокси-3-метил-бут-2-енилпирофосфат (HMB-PP) |  |
| HMB-PP | HMB-PP редуктаза (LytB, IspH; HDR) | Изопентенил пирофосфат (IPP) и Диметилаллил пирофосфат (DMAP) |   |
Исследование ингибирования и других путей
DXP редуктоизомераза (также известный как DXR, DOXP редуктоизомераза, IspC, MEP-синтаза), является ключевым ферментом в пути MEP. Это может быть запрещено натуральный продукт фосмидомицин, который изучается в качестве отправной точки для разработки антибактериального или противомалярийного препарата-кандидата.[8][9][10]
Промежуточный, HMB-PP, является естественным активатором человеческого Vγ9 / Vδ2 Т-клетки, основная популяция γδ Т-клеток в периферической крови и клетки, которые «играют решающую роль в иммунном ответе на микробные патогены».[11]
Рекомендации
- ^ Rohmer M; Ромер, Мишель (1999). «Открытие независимого от мевалоната пути биосинтеза изопреноидов у бактерий, водорослей и высших растений». Nat Prod Rep. 16 (5): 565–574. Дои:10.1039 / a709175c. PMID 10584331.
- ^ В. Эйзенрайх; А. Бахер; Д. Аригони; Ф. Рохдич (2004). «Обзор биосинтеза изопреноидов через немевалонатный путь». Клеточные и молекулярные науки о жизни. 61 (12): 1401–1426. Дои:10.1007 / s00018-004-3381-z. PMID 15197467.
- ^ Хантер, WN (2007). "Немевалонатный путь биосинтеза изопреноидных предшественников". Журнал биологической химии. 282 (30): 21573–21577. Дои:10.1074 / jbc.R700005200. PMID 17442674.
- ^ Лихтенталер Х (1999). «Путь 1-дезокси-D-ксилулозо-5-фосфата биосинтеза изопреноидов в растениях». Анну Рев Завод Физиол Растение Мол Биол. 50: 47–65. Дои:10.1146 / annurev.arplant.50.1.47. PMID 15012203.
- ^ Wiemer, AJ; Сяо, Швейцария; Вимер, Д.Ф. (2010). «Изопреноидный метаболизм как терапевтическая мишень для грамотрицательных патогенов». Актуальные темы медицинской химии. 10 (18): 1858–1871. Дои:10.2174/156802610793176602. PMID 20615187.
- ^ а б Цидвай Т., Джамал Ф, Хан М.Ю., Шарма Б. (2014). «Изучение лекарственных мишеней в пути биосинтеза изопреноидов для Plasmodium falciparum». Biochemistry Research International. 2014: 657189. Дои:10.1155/2014/657189. ЧВК 4017727. PMID 24864210.CS1 maint: использует параметр авторов (связь)
- ^ а б Eisenreich W, Bacher A, Arigoni D, Rohdich F (2004). «Биосинтез изопреноидов немевалонатным путем». Клетка. Мол. Life Sci. 61 (12): 1401–26. Дои:10.1007 / s00018-004-3381-z. PMID 15197467.
- ^ Хейл И., О'Нил П.М., Берри Н.Г., Одом А. и Шарма Р. (2012). «Путь MEP и разработка ингибиторов как потенциальных противоинфекционных агентов». Med. Chem. Сообщество. 3 (4): 418–433. Дои:10.1039 / C2MD00298A.CS1 maint: использует параметр авторов (связь)
- ^ Джомаа Х., Визнер Дж., Сандербранд С. и др. (1999). «Ингибиторы немевалонатного пути биосинтеза изопреноидов в качестве противомалярийных препаратов». Наука (отчет о первичном исследовании)
| формат =требует| url =(помощь). 285 (5433): 1573–6. Дои:10.1126 / science.285.5433.1573. PMID 10477522. - ^ К. Зингле; Л. Кунц; Д. Трич; К. Гросдеманж-Бильярд; М. Ромер (2010). «Изопреноидный биосинтез через метилэритритолфосфатный путь: структурные вариации вокруг фосфонатного якоря и спейсера фосмидомицина, мощного ингибитора дезоксиксилулозофосфатредуктоизомеразы». J. Org. Chem. (отчет о первичном исследовании)
| формат =требует| url =(помощь). 75 (10): 3203–3207. Дои:10.1021 / jo9024732. PMID 20429517. - ^ Эберл М., Хинтц М., Райхенберг А., Коллас А.К., Визнер Дж., Джомаа Х. (2003). «Микробный изопреноидный биосинтез и активация человеческих γδ Т-клеток». FEBS Lett. 544 (1–3): 4–10. Дои:10.1016 / S0014-5793 (03) 00483-6. PMID 12782281.
дальнейшее чтение
- Хейл И., О'Нил П.М., Берри Н.Г., Одом А. и Шарма Р. (2012). «Путь MEP и разработка ингибиторов как потенциальных противоинфекционных агентов». Med. Chem. Сообщество. 3 (4): 418–433. Дои:10.1039 / C2MD00298A.CS1 maint: использует параметр авторов (связь) RSC рассмотрение; использует номенклатуру MAP-синтазы.
- Цидвай Т., Джамал Ф, Хан М.Ю., Шарма Б. (2014). «Изучение лекарственных мишеней в пути биосинтеза изопреноидов для Plasmodium falciparum». Biochemistry Research International. 2014: 657189. Дои:10.1155/2014/657189. ЧВК 4017727. PMID 24864210.CS1 maint: использует параметр авторов (связь)

