Диен - Википедия - Diene
В органическая химия а диен (/ˈdаɪ.яп/ DY-een ) (диолефин (/dаɪˈoʊлəжɪп/ dy-ОЙ-lə-fin ) или же алкадиен) это ковалентное соединение который содержит два двойные связи, обычно среди углерод атомы.[1] Таким образом, они содержат два алкene единиц, со стандартным префиксом ди из систематическая номенклатура. Как субъединица более сложных молекул, диены встречаются в природных и синтетических химических веществах и используются в органический синтез. Конъюгированный диены широко используются как мономеры в полимер промышленность. Полиненасыщенные жиры представляют интерес для питание.
Классы
Диены можно разделить на три класса, в зависимости от относительного расположения двойных связей:[1]
- Кумулятивные диены имеют двойные связи, разделяющие общий атом. Результат более конкретно называется аллен.
- Конъюгированные диены имеют сопряженный двойные связи, разделенные одной одинарной связью. Конъюгированные диены более стабильны, чем другие диены из-за резонанса.
- Несопряженные диены имеют двойные связи, разделенные двумя или более одинарными связями. Обычно они менее стабильны, чем изомерный сопряженные диены. Это также может быть известно как изолированный диен.

Согласно Золотая книга По определению, «диен» может включать один или несколько гетероатомы которые заменяют ненасыщенные атомы углерода, давая структуры, которые можно было бы более конкретно назвать гетеродиены.[1]
Соединения, содержащие более двух двойных связей, называются полиены. Полиены и диены имеют много общих свойств.
Синтез диенов
В промышленных масштабах бутадиен получают термическое растрескивание из бутаны. В аналогичном неизбирательном процессе дициклопентадиен получается из каменноугольные смолы.
В лаборатории используются более целенаправленные и более тонкие процессы, такие как дегидрогалогенирование и конденсаты. Мириады методы были разработаны, такие как Реакция Уайтинга. Семейства несопряженных диенов происходят от олигомеризация и димеризация сопряженных диенов. Например, 1,5-циклооктадиен и винилциклогексен получают димеризацией 1,3-бутадиен.
Диен-содержащий жирные кислоты находятся биосинтезированный из ацетил-КоА.
α, ω-Диены имеют формулу (CH2)п(CH = CH2)2. Их готовят промышленным способом этенолиз циклических диенов. Например, 1,5-гексадиен и 1,9-декадиен, полезные сшивающие агенты и синтетические промежуточные продукты, получают из 1,5-циклооктадиен и циклооктен, соответственно. Катализатор получен из Re2О7 на глиноземе.[2]
Реакционная способность и использование
Полимеризация
Наиболее часто встречающаяся реакция алкенов, включая диены, - это полимеризация. 1,3-Бутадиен является предшественником резинка используется в шинах, и изопрен является предшественником натуральная резина. Хлоропрен родственный, но это синтетический мономер.
Циклоприсоединения
Важной реакцией на сопряженные диены является Реакция Дильса – Альдера. Многие специализированные диены были разработаны для использования этой реакционной способности для синтеза натуральные продукты (например., Диена Данишефского ).
Другие реакции присоединения
К конъюгированным диенам добавляют такие реагенты, как бром и водород по путям 1,2-присоединения и 1,4-присоединения. Добавление полярных реагентов может создавать сложные архитектуры:[3]
Реакции метатезиса
Несопряженные диены являются субстратами для метатезис, замыкающий кольцо реакции. Для этих реакций требуется металл катализатор:
Кислотность
Положение рядом с двойной связью кислый потому что в результате аллил анион стабилизируется резонансом. Этот эффект становится более выраженным по мере того, как больше алкенов участвует в создании большей стабильности. Например, депротонирование в положении 3 1,4-диена или положении 5 1,3-диена дает пентадиенил анион. Еще больший эффект наблюдается, если анион ароматический, например, депротонирование циклопентадиен дать циклопентадиенил анион.
Как лиганды
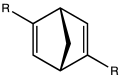
Диены широко используют хелатирующие лиганды в металлоорганическая химия. В некоторых случаях они служат в качестве лигандов-заполнителей, удаляясь во время каталитического цикла. Например, циклооктадиеновые («трески») лиганды в бис (циклооктадиен) никель (0) лабильны. В некоторых случаях диены являются лигандами-наблюдателями, остающимися скоординированными на протяжении всего каталитического цикла и влияющими на распределение продуктов. Хиральный также описаны диены.[5] Другие диеновые комплексы включают (бутадиен) трикарбонил железа, циклобутадиен, трикарбонил железа, и циклооктадиен димер хлорида родия.
Рекомендации
- ^ а б c ИЮПАК, Сборник химической терминологии 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "диены ". Дои:10.1351 / goldbook.D01699
- ^ Лайонел Делод, Альфред Ф. Ноэлс (2005). «Метатезис». Энциклопедия химической технологии Кирка-Отмера. Вайнхайм: Wiley-VCH. Дои:10.1002 / 0471238961.metanoel.a01. ISBN 0471238961.CS1 maint: использует параметр авторов (связь)
- ^ Роджер Бишоп. «9-Тиабицикло [3.3.1] нонан-2,6-дион». Органический синтез.; Коллективный объем, 9, п. 692Диас, Дэвид Диас; Конверсо, Антонелла; Шарплесс, К. Барри; Финн, М. Г. (2006). «2,6-Дихлор-9-тиабицикло [3.3.1] нонан: многограммное отображение азидных и цианидных компонентов на универсальной основе». Молекулы. 11 (4): 212–218. Дои:10.3390/11040212. ЧВК 6148556. PMID 17962753.
- ^ Хаяси Т., Уэяма К., Токунага Н., Ёсида К. (2003). "Хиральный хелатирующий диен как новый тип хирального лиганда для катализаторов переходных металлов: его получение и использование для катализируемого родием асимметричного 1,4-присоединения". Варенье. Chem. Soc. 125 (38): 11508–11509. Дои:10.1021 / ja037367z. PMID 13129348.
- ^ Рио Шинтани, Тамио Хаяси, "Хиральные диеновые лиганды для асимметричного катализа" Олдрич Чимика Acta 2009, вып. 42, номер 2, с. 31-38.


![2,6-Дихлор-9-тиабицикло [3.3.1] нонан, синтез и реакции](http://upload.wikimedia.org/wikipedia/commons/thumb/a/ab/CODSCl2.png/450px-CODSCl2.png)
