Винорелбин - Vinorelbine
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Навельбин |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a695013 |
| Беременность категория |
|
| Маршруты администрация | внутривенный, устно[1] |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 43 ± 14% (перорально)[2] |
| Связывание с белками | От 79 до 91% |
| Метаболизм | печень (CYP3A4 -опосредованно) |
| Устранение период полураспада | От 27,7 до 43,6 часов |
| Экскреция | Фекальный (46%) и почка (18%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
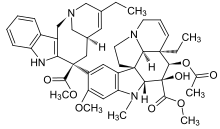
| Формула | C45ЧАС54N4О8 |
| Молярная масса | 778.947 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Винорелбин (NVB), продается под торговой маркой Навельбин среди прочего, это химиотерапевтические препараты используется для лечения ряда видов рака.[3] Это включает в себя рак молочной железы и немелкоклеточный рак легкого.[3] Это дается инъекция в вену или через рот.[3][1]
Общие побочные эффекты включают: подавление костного мозга, боль в месте инъекции, рвота, чувство усталости, онемение и диарея.[3] Другие серьезные побочные эффекты включают: одышка.[3] Использовать во время беременность может навредить ребенку.[3] Винорелбин находится в алкалоид барвинка семейство лекарств.[1] Считается, что он действует, нарушая нормальную функцию микротрубочки и тем самым остановив деление клеток.[3]
Винорелбин был одобрен для медицинского применения в США в 1994 году.[3] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[4]
Медицинское использование
Винорелбин одобрен для лечения немелкоклеточного рака легкого.[5][6] Он используется не по прямому назначению для лечения других видов рака, таких как метастатический рак груди. Он также активен в рабдомиосаркома.[7]
Побочные эффекты
Винорелбин имеет ряд побочных эффектов, которые могут ограничивать его использование:
Периферическая невропатия, вызванная химиотерапией (прогрессирующее, стойкое и часто необратимое покалывание, онемение, сильная боль и гиперчувствительность к холоду, начинающиеся с кистей и стоп, а иногда и с вовлечением рук и ног[8]), пониженная сопротивляемость инфекциям, синякам или кровотечению, анемия, запор, рвота, понос, тошнота, усталость и общее чувство слабости (астения ), воспаление вены, в которую он был введен (флебит ). Редко тяжелый гипонатриемия виден.
Реже наблюдаются выпадение волос и аллергическая реакция.
Фармакология
Противоопухолевая активность обусловлена ингибированием митоза за счет взаимодействия с тубулином.[9]
История
Винорелбин изобрел фармацевт Пьер Потье и его команда из CNRS в Франция в 1980-х годах и получил лицензию на отделение онкологии Pierre Fabre Group. Препарат был одобрен во Франции в 1989 году под торговой маркой Навельбин для лечения немелкоклеточных заболеваний. рак легких. Он получил разрешение лечить метастатический рак груди в 1991 г. Винорелбин получил одобрение Соединенные Штаты Управление по контролю за продуктами и лекарствами (FDA) в декабре 1994 г. при финансовой поддержке Burroughs Wellcome Company. Группа Pierre Fabre теперь продает Навельбин в США, где в феврале 2003 года этот препарат стал генериком.
В большинстве европейских стран винорелбин одобрен для лечения немелкоклеточного рака легких и рака груди. В США он одобрен только для лечения немелкоклеточного рака легкого.
Источники
Барвинок мадагаскарский Катарантус розовый L. является источником ряда важных натуральных продуктов, в том числе катарантин и виндолин[10] и алкалоиды барвинка из них производит: лейрозин и химиотерапия агенты винбластин и винкристин, все это можно получить с завода.[11][12][5][13] Новее полусинтетический химиотерапевтическое средство винорелбин, которое используется при лечении немелкоклеточный рак легкого[5][6] и, как известно, не встречается в природе. Однако его можно приготовить как из виндолина, так и из катарантина.[5][14] или из лейрозина,[15] в обоих случаях путем синтеза ангидровинбластин. Путь лейрозина использует Реагент Наджента – Раджана Бабу в высоко хемоселективной деоксигенации лейрозина.[16][15] Затем ангидровинбластин последовательно реагирует с N-бромосукцинимид и трифторуксусная кислота с последующим тетрафторборат серебра чтобы получить винорелбин.[14]

Оральный состав
Пероральный состав был продан и зарегистрирован в большинстве европейских стран. Он имеет такую же эффективность, что и препарат для внутривенного введения, но позволяет избежать токсического воздействия на вену при инфузии и его легче принимать.[требуется медицинская цитата ] Устная форма не одобрена в США и Австралии.[требуется медицинская цитата ]
Рекомендации
- ^ а б c Британский национальный формуляр: BNF 69 (69 изд.). Британская медицинская ассоциация. 2015. стр. 594. ISBN 9780857111562.
- ^ Марти М., Фумоле П., Аденис А., Руссо И., Мерруш И., Робине Дж., Сенак I, Пуоццо С. (2001). «Исследование фармакокинетики перорального винорелбина и абсолютной биодоступности у пациентов с солидными опухолями». Энн Онкол. 12 (11): 1643–9. Дои:10.1023 / А: 1013180903805. PMID 11822766.
- ^ а б c d е ж грамм час «Винорелбин тартрат». Американское общество фармацевтов систем здравоохранения. В архиве из оригинала 21 декабря 2016 г.. Получено 8 декабря 2016.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ а б c d Кеглевич, Петер; Хазаи, Ласло; Калаус, Дьёрдь; Сантай, Чаба (2012). «Модификации основных скелетов винбластина и винкристина». Молекулы. 17 (5): 5893–5914. Дои:10.3390 / молекулы17055893. ЧВК 6268133. PMID 22609781.
- ^ а б Фаллер, Брайан А.; Панди, Трайлокья Н. (2011). «Безопасность и эффективность винорелбина в лечении немелкоклеточного рака легкого». Понимание клинической медицины: онкология. 5: 131–144. Дои:10.4137 / CMO.S5074. ЧВК 3117629. PMID 21695100.
- ^ Казанова, Микела; Феррари, Андреа; Спреафико, Филиппо; Теренциани, Моника; Массимино, Маура; Лукш, Роберто; Чефало, Грациелла; Поластри, Даниэла; Маркон, Илария; Беллани, Франка Фоссати (2002). «Винорелбин в ранее леченных запущенных детских саркомах: доказательства активности при рабдомиосаркоме». Рак. 94 (12): 3263–3268. Дои:10.1002 / cncr.10600. PMID 12115359. S2CID 21824468.
- ^ дель Пино BM. Периферическая нейропатия, вызванная химиотерапией. Бюллетень NCI Cancer Bulletin. 23 февраля 2010 г. [в архиве 2011-12-11];7(4):6.
- ^ Jordan, M. A .; Уилсон, Л. (2004). «Микротрубочки как мишень для противоопухолевых препаратов». Обзоры природы Рак. 4 (4): 253–265. Дои:10.1038 / nrc1317. PMID 15057285. S2CID 10228718.
- ^ Хирата, К .; Миямото, К .; Миура, Ю. (1994). "Катарантус розовый L. (Барвинок): Производство виндолина и катарантина в культурах с множественными побегами ». В Bajaj, Ю. П. С. (ред.). Биотехнология в сельском и лесном хозяйстве 26. Лекарственные и ароматические растения. VI. Springer-Verlag. стр.46–55. ISBN 9783540563914.
- ^ Гансойер, Андреас; Юстисия, Хосе; Фань, Чун-Ан; Воргулл, Деннис; Пистерт, Фредерик (2007). «Восстановительное образование связи C — C после раскрытия эпоксида посредством переноса электрона». В Крише, Майкл Дж. (ред.). Катализируемое металлом образование восстановительных связей C — C: отход от предварительно приготовленных металлоорганических реагентов. Темы современной химии. 279. Springer Science & Business Media. С. 25–52. Дои:10.1007/128_2007_130. ISBN 9783540728795. В архиве из оригинала от 01.08.2017.
- ^ Купер, Раймонд; Дикин, Джеффри Джон (2016). «Дар Африки миру». Ботанические чудеса: химия растений, изменивших мир. CRC Press. С. 46–51. ISBN 9781498704304. В архиве из оригинала от 01.08.2017.
- ^ Равинья, Энрике (2011). «Алкалоиды барвинка». Эволюция открытия лекарств: от традиционных лекарств к современным лекарствам. Джон Уайли и сыновья. С. 157–159. ISBN 9783527326693. В архиве из оригинала от 01.08.2017.
- ^ а б Нго, Куок Ань; Русси, Фанни; Кормье, Энтони; Торет, Сильвиана; Кноссов, Марсель; Генар, Даниэль; Герит, Франсуаза (2009). «Синтез и биологическая оценка Алкалоиды барвинка и гибриды фомопсина ". Журнал медицинской химии. 52 (1): 134–142. Дои:10.1021 / jm801064y. PMID 19072542.
- ^ а б Хардуэн, Кристоф; Дорис, Эрик; Руссо, Бернар; Миосковски, Чарльз (2002). «Краткий синтез ангидровинбластина из лейрозина». Органические буквы. 4 (7): 1151–1153. Дои:10.1021 / ol025560c. PMID 11922805.
- ^ Морсилло, Сара П .; Мигель, Делия; Campaña, Araceli G .; Сьенфуэгос, Луис Альварес де; Юстисия, Хосе; Куерва, Хуан М. (2014). "Недавние применения Cp2TiCl в синтезе природных продуктов ». Границы органической химии. 1 (1): 15–33. Дои:10.1039 / c3qo00024a.
внешняя ссылка
- «Винорелбин». Портал информации о наркотиках. Национальная медицинская библиотека США.
