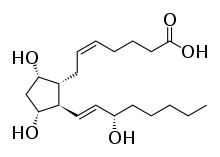
Простагландин F2альфа - Prostaglandin F2alpha
 | |
| Клинические данные | |
|---|---|
| Другие имена | Амогландин, Кронибен, Циклозин, Динифертин, Энзапрост, Гландин, PGF2α, Панацелан, Простамодин |
| AHFS /Drugs.com | Международные названия лекарств |
| Маршруты администрация | Внутривенно (не может использоваться для стимулирования родов), потому что не может использоваться в шейке матки, внутриамниотический (чтобы вызвать аборт) |
| Код УВД | |
| Фармакокинетический данные | |
| Устранение период полураспада | От 3 до 6 часов в амниотическая жидкость, менее 1 минуты в плазма крови |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.209.720 |
| Химические и физические данные | |
| Формула | C20ЧАС34О5 |
| Молярная масса | 354.487 г · моль−1 |
| 3D модель (JSmol ) | |
| Растворимость в воде | 200 мг / мл (20 ° С) |
| |
| |
| | |
Простагландин F2α (PGF2α в простаноид номенклатура), фармацевтически называемые карбопрост простагландин природного происхождения, используемый в медицине для вызвать роды и как абортивное средство.[1]
У домашних млекопитающих он вырабатывается маткой при стимуляции окситоцин в том случае, если имплантация в лютеиновую фазу не производилась. Он действует на желтое тело вызывать лютеолиз, образуя corpus albicans и остановка выработки прогестерона. Действие PGF2α зависит от количества рецепторов на мембране желтого тела.
PGF2α изоформа 8-изо-PGF2α был обнаружен в значительно увеличенных количествах у пациентов с эндометриоз, таким образом, являясь потенциальным причинным звеном окислительного стресса, связанного с эндометриозом.[2]
Механизм действия
PGF2α действует путем привязки к рецептор простагландина F2α. Он высвобождается в ответ на повышение уровня окситоцина в матке и стимулирует как лютеолитическую активность, так и высвобождение окситоцина.[3] Потому что PGF2α связан с повышением уровня окситоцина в матке, есть данные, что PGF2α и окситоцин образуют петлю положительной обратной связи, способствующую деградации желтого тела.[4] PGF2α и окситоцин также подавляют производство прогестерон, гормон, который способствует развитию желтого тела. И наоборот, более высокие уровни прогестерона подавляют выработку PGF.2α и окситоцин, поскольку эффекты гормонов противоположны друг другу.
Фармацевтическое использование
При введении в тело или амниотический мешок PGF2α может вызвать роды или аборт в зависимости от используемой концентрации. В малых дозах (1–4 мг / сут) PGF2α действует, чтобы стимулировать сокращение мышц матки, что помогает в процессе родов. Однако в течение первого триместра и в более высоких концентрациях (40 мг / день)[5] PGF2α может вызвать аборт из-за разрушения желтого тела, которое питает плод в утробе матери. Поскольку к этому времени плод не жизнеспособен вне матки, недостаток пищи приводит к истощению и прерыванию плода через день или два.
Синтез
Промышленный синтез
В 2012 году краткий и высокостереоселективный общий синтез PGF2α был описан.[6] Синтез требует всего семи шагов, что является огромным улучшением первоначального 17-шагового синтеза Кори и Ченга,[7] и использует 2,5-диметокситетрагидрофуран в качестве исходного реагента, с S-пролин как асимметричный катализатор.
Биосинтез
В организме PGF2α синтезируется в несколько отдельных этапов. Первый, Фосфолипаза А2 (PLA2) способствует превращению фосфолипидов в Арахидоновая кислота, каркас, из которого формируются все простагландины.[8] Затем арахидоновая кислота реагирует с двумя Циклооксигеназа (ЦОГ) рецепторы, ЦОГ-1 и ЦОГ-2 с образованием простагландина H2, промежуточный. Наконец, соединение вступает в реакцию с альдозоредуктазой (AKR1B1 ) для формирования PGF2α.[8]
Аналоги
Следующие лекарства аналоги простагландина F2α:
Рекомендации
- ^ Индекс Merck: энциклопедия химикатов, лекарств и биологических препаратов. О'Нил, Мариадель Дж., Королевское химическое общество (Великобритания) (15-е изд.). Кембридж, Великобритания: Королевское химическое общество. 2013. ISBN 978-1849736701. OCLC 824530529.CS1 maint: другие (связь)
- ^ Шарма I, Дхаливал Л.К., Саха СК, Сангван С., Дхаван В. (июнь 2010 г.). «Роль 8-изопростагландина F2alpha и 25-гидроксихолестерина в патофизиологии эндометриоза». Фертильность и бесплодие. 94 (1): 63–70. Дои:10.1016 / j.fertnstert.2009.01.141. PMID 19324352.
- ^ Самуэльссон Б., Голдайн М., Гранстрем Э., Хамберг М., Хаммарстрём С., Мальмстен С. (1978). «Простагландины и тромбоксаны». Ежегодный обзор биохимии. 47: 997–1029. Дои:10.1146 / annurev.bi.47.070178.005025. PMID 209733.
- ^ Хупер С.Б., Уоткинс В.Б., Торберн Г.Д. (декабрь 1986 г.). «Концентрации окситоцина, нейрофизина, связанного с окситоцином, и простагландина F2 альфа в маточно-яичниковой вене беременных и небеременных овец» (PDF). Эндокринология. 119 (6): 2590–7. Дои:10.1210 / эндо-119-6-2590. PMID 3465529.
- ^ «Расширенная информация для пациентов с инъекциями динопроста трометамина». Truvn Health Analytics Inc. 2016. Получено 2 ноября, 2017.
- ^ Култхард Г., Эрб В., Аггарвал В.К. (сентябрь 2012 г.). «Стереоконтролируемый органокаталитический синтез простагландина PGF2α в семь этапов». Природа. 489 (7415): 278–81. Bibcode:2012Натура 489..278С. Дои:10.1038 / природа11411. PMID 22895192.
- ^ Кори EJ, Ченг XM (1995). Логика химического синтеза. Вайли.
- ^ а б Fortier MA, Krishnaswamy K, Danyod G, Boucher-Kovalik S, Chapdalaine P (август 2008 г.). «Постгеномный комплексный взгляд на простагландины в репродукции: последствия для других систем организма». Журнал физиологии и фармакологии. 59 Дополнение 1: 65–89. PMID 18802217.
