Стероидный гормон - Steroid hormone
| Стероидный гормон | |
|---|---|
| Класс препарата | |
 | |
| Идентификаторы класса | |
| Синонимы | Стероид надпочечников; Гонадный стероид |
| Использовать | Разные |
| Биологическая мишень | Рецепторы стероидных гормонов |
| Химический класс | Стероидный; Нестероидный |
| В Викиданных | |
А стероидный гормон это стероидный препарат что действует как гормон. Стероидные гормоны можно разделить на два класса: кортикостероиды (обычно производится в кора надпочечников, следовательно кортико-) и половые стероиды (обычно производится в гонады или же плацента ). Внутри этих двух классов пять типов в соответствии с рецепторы к которым они привязаны: глюкокортикоиды и минералокортикоиды (оба кортикостероиды) и андрогены, эстрогены, и прогестагены (половые стероиды). Витамин Д производные представляют собой шестую близкородственную гормональную систему с гомологичными рецепторами. Они обладают некоторыми характеристиками настоящих стероидов: рецепторные лиганды.
Стероидные гормоны помогают контролировать обмен веществ, воспаление, иммунные функции, солевой и водный баланс, развитие половые признаки и способность противостоять болезням и травмам. Период, термин стероидный препарат описывает как гормоны, вырабатываемые организмом, так и искусственно производимые лекарства, которые дублируют действие природных стероидов.[1][2][3]
Синтез

Природные стероидные гормоны обычно синтезируются из холестерин в гонады и надпочечники. Эти формы гормонов липиды. Они могут проходить через клеточную мембрану, поскольку они жирорастворимы,[5] а затем привязать к рецепторы стероидных гормонов (который может быть ядерным или цитозольным в зависимости от стероидного гормона), чтобы вызвать изменения внутри клетки. Стероидные гормоны обычно переносятся в крови и связаны с конкретным носителем. белки Такие как глобулин, связывающий половые гормоны или же кортикостероид-связывающий глобулин. Дальнейшие преобразования и катаболизм происходят в печени, в других «периферических» тканях и в тканях-мишенях.
| Секс | Половой гормон | Репродуктивный фаза | Кровь дебит | Гонад скорость секреции | Метаболический скорость оформления | Референсный диапазон (уровни сыворотки) | |
|---|---|---|---|---|---|---|---|
| SI единицы | Не-SI единицы | ||||||
| Мужчины | Андростендион | – | 2,8 мг / день | 1,6 мг / день | 2200 л / сутки | 2,8-7,3 нмоль / л | 80–210 нг / дл |
| Тестостерон | – | 6,5 мг / день | 6,2 мг / день | 950 л / сутки | 6,9–34,7 нмоль / л | 200–1000 нг / дл | |
| Estrone | – | 150 мкг / день | 110 мкг / день | 2050 л / сутки | 37–250 пмоль / л | 10–70 пг / мл | |
| Эстрадиол | – | 60 мкг / день | 50 мкг / день | 1600 л / сутки | <37–210 пмоль / л | 10–57 пг / мл | |
| Эстрона сульфат | – | 80 мкг / день | Незначительный | 167 л / сутки | 600–2500 пмоль / л | 200–900 пг / мл | |
| Женщины | Андростендион | – | 3,2 мг / день | 2,8 мг / день | 2000 л / сутки | 3,1–12,2 нмоль / л | 89–350 нг / дл |
| Тестостерон | – | 190 мкг / день | 60 мкг / день | 500 л / сутки | 0,7–2,8 нмоль / л | 20–81 нг / дл | |
| Estrone | Фолликулярная фаза | 110 мкг / день | 80 мкг / день | 2200 л / сутки | 110–400 пмоль / л | 30–110 пг / мл | |
| Лютеиновой фазы | 260 мкг / день | 150 мкг / день | 2200 л / сутки | 310–660 пмоль / л | 80–180 пг / мл | ||
| Постменопауза | 40 мкг / день | Незначительный | 1610 л / сутки | 22–230 пмоль / л | 6–60 пг / мл | ||
| Эстрадиол | Фолликулярная фаза | 90 мкг / день | 80 мкг / день | 1200 л / сутки | <37–360 пмоль / л | 10–98 пг / мл | |
| Лютеиновой фазы | 250 мкг / день | 240 мкг / день | 1200 л / сутки | 699–1250 пмоль / л | 190–341 пг / мл | ||
| Постменопауза | 6 мкг / день | Незначительный | 910 л / сутки | <37–140 пмоль / л | 10–38 пг / мл | ||
| Эстрона сульфат | Фолликулярная фаза | 100 мкг / день | Незначительный | 146 л / сутки | 700–3600 пмоль / л | 250–1300 пг / мл | |
| Лютеиновой фазы | 180 мкг / день | Незначительный | 146 л / сутки | 1100–7300 пмоль / л | 400–2600 пг / мл | ||
| Прогестерон | Фолликулярная фаза | 2 мг / день | 1,7 мг / день | 2100 л / сутки | 0,3–3 нмоль / л | 0,1–0,9 нг / мл | |
| Лютеиновой фазы | 25 мг / день | 24 мг / день | 2100 л / сутки | 19–45 нмоль / л | 6–14 нг / мл | ||
Примечания и источники Примечания: "The концентрация Количество стероида в кровотоке определяется скоростью, с которой он секретируется железами, скоростью метаболизма предшественника или прегормонов в стероид и скоростью, с которой он извлекается тканями и метаболизируется. В скорость секреции стероида относится к общей секреции соединения железой за единицу времени. Скорость секреции оценивалась путем отбора проб венозного стока из железы с течением времени и вычитания концентрации артериальных и периферических венозных гормонов. В скорость метаболического клиренса стероида определяется как объем крови, который полностью очищен от гормона за единицу времени. В дебит стероидного гормона относится к поступлению в кровь соединения из всех возможных источников, включая секрецию желез и превращение прогормонов в интересующий стероид. В устойчивом состоянии количество гормона, поступающего в кровь из всех источников, будет равно скорости, с которой он очищается (скорость метаболического клиренса), умноженной на концентрацию в крови (скорость продукции = скорость метаболического клиренса × концентрация). Если метаболизм прогормона вносит небольшой вклад в циркулирующий пул стероидов, то скорость производства будет приблизительно соответствовать скорости секреции ». Источники: См. Шаблон. | |||||||
Синтетические стероиды и стерины
Также было изобретено множество синтетических стероидов и стеринов. Большинство из них - стероиды, но некоторые нестероидный молекулы могут взаимодействовать со стероидными рецепторами из-за сходства формы. Некоторые синтетические стероиды слабее или сильнее натуральных стероидов, рецепторы которых они активируют.[6]
Некоторые примеры синтетических стероидных гормонов:
- Глюкокортикоиды: алклометазон, преднизон, дексаметазон, триамцинолон, кортизон
- Минералокортикоид: флудрокортизон
- Витамин Д: дигидротахистерин
- Андрогены: оксандролон, оксаболон, тестостерон, нандролон (также известные как анаболические андрогенные стероиды или просто анаболические стероиды )
- Эстрогены: диэтилстильбестрол (DES) и эстрадиол
- Прогестины: норэтистерон, медроксипрогестерона ацетат, гидроксипрогестерона капроат.
Некоторые антагонисты стероидов:
- Андрогены: ципротерона ацетат
- Прогестины: мифепристон, гестринон
Транспорт

Стероидные гормоны транспортируются через кровь, связываясь с белками-носителями - белками сыворотки, которые связывают их и повышают растворимость гормонов в воде. Некоторые примеры глобулин, связывающий половые гормоны (SHBG), кортикостероид-связывающий глобулин, и альбумин.[7] Большинство исследований говорят, что гормоны могут влиять на клетки, только если они не связаны белками сыворотки. Чтобы быть активными, стероидные гормоны должны освободиться от своих солюбилизирующих кровь белков и либо связываться с внеклеточными рецепторами, либо пассивно пересекать клеточную мембрану и связываться с ними. ядерные рецепторы. Эта идея известна как гипотеза свободных гормонов. Эта идея показана на рисунке 1 справа.
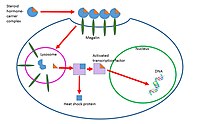
Одно исследование показало, что эти комплексы стероид-носитель связываются мегалин, мембранный рецептор, а затем попадают в клетки через эндоцитоз. Один из возможных путей состоит в том, что, оказавшись внутри клетки, эти комплексы попадают в лизосому, где белок-носитель разрушается, а стероидный гормон высвобождается в цитоплазму клетки-мишени. Затем гормон следует геномному пути действия. Этот процесс показан на рисунке 2 справа.[8] Роль эндоцитоза в транспорте стероидных гормонов недостаточно изучена и находится в стадии дальнейшего изучения.
Чтобы стероидные гормоны пересекали липидный бислой клеток, они должны преодолевать энергетические барьеры, которые препятствовали бы их входу или выходу из мембраны. Свободная энергия Гиббса здесь важная концепция. Эти гормоны, все производные холестерина, имеют гидрофильные функциональные группы на обоих концах и гидрофобные углеродные скелеты. Когда стероидные гормоны проникают в мембраны, существуют барьеры свободной энергии, когда функциональные группы входят в гидрофобную внутреннюю часть мембраны, но для гидрофобного ядра этих гормонов энергетически выгодно проникать в липидные бислои. Эти энергетические барьеры и колодцы перевернуты для гормонов, выходящих из мембран. Стероидные гормоны легко проникают и покидают мембрану в физиологических условиях. Экспериментально было показано, что они пересекают мембраны со скоростью около 20 мкм / с, в зависимости от гормона.[9]
Хотя гормонам энергетически выгоднее находиться в мембране, чем в ECF или ICF, они действительно покидают мембрану, когда попадают в нее. Это важное соображение, потому что холестерин - предшественник всех стероидных гормонов - не покидает мембрану, как только он внедрился внутрь. Разница между холестерином и этими гормонами заключается в том, что холестерин находится в гораздо большей отрицательной свободной энергии Гибба, находящейся внутри мембраны, по сравнению с этими гормонами. Это связано с тем, что алифатический хвост на холестерине очень благоприятно взаимодействует с внутренней частью липидных бислоев.[9]
Механизмы действия и эффекты
Существует множество различных механизмов, посредством которых стероидные гормоны влияют на их клетки-мишени. Все эти различные пути могут быть классифицированы как имеющие геномный эффект или негеномный эффект. Геномные пути являются медленными и приводят к изменению уровней транскрипции определенных белков в клетке; негеномные пути намного быстрее.
Геномные пути
Первыми идентифицированными механизмами действия стероидных гормонов были геномные эффекты.[10] По этому пути свободные гормоны сначала проходят через клеточную мембрану, потому что они жирорастворимы.[5] В цитоплазме стероид может подвергаться или не подвергаться фермент -опосредованное изменение, такое как восстановление, гидроксилирование или ароматизация. Затем стероид связывается с определенным рецептор стероидного гормона, также известный как ядерный рецептор, который представляет собой крупный металлопротеин. При связывании стероидов многие виды стероидных рецепторов димеризовать: две субъединицы рецептора объединяются, чтобы сформировать одну функциональную ДНК -связывающая единица, способная проникать в ядро клетки. Попав в ядро, комплекс стероид-рецептор-лиганд связывается со специфическими ДНК последовательности и индуцирует транскрипцию своей мишени гены.[2][11][12][10]
Негеномные пути
Поскольку негеномные пути включают любой механизм, который не является геномным эффектом, существуют различные негеномные пути. Однако все эти пути опосредуются каким-либо типом рецептор стероидного гормона находится на плазматической мембране.[13] Стероидные гормоны влияют на ионные каналы, переносчики, рецепторы, сопряженные с G-белком (GPCR) и текучесть мембран.[9] Из них наиболее распространены белки, связанные с GPCR. Для получения дополнительной информации об этих белках и метаболических путях посетите рецептор стероидного гормона страница.
Смотрите также
Рекомендации
- ^ Фондер Дж. У., Крозовски З., Майлс К., Сато А., Шеппард К. Э., Янг М. (1997). «Минералокортикоидные рецепторы, соли и гипертония». Недавнее Prog Horm Res. 52: 247–260. PMID 9238855.
- ^ а б Гупта ББП, Лалчхандама К. (2002). «Молекулярные механизмы действия глюкокортикоидов» (PDF). Текущая наука. 83 (9): 1103–1111.
- ^ Фрай CA (2009). «Стероиды, репродуктивная эндокринная функция и аффект. Обзор». Минерва Гинекол. 61 (6): 541–562. PMID 19942840.
- ^ Хэггстрем, Микаэль; Ричфилд, Дэвид (2014). «Схема путей стероидогенеза человека». WikiJournal of Медицина. 1 (1). Дои:10.15347 / wjm / 2014.005. ISSN 2002-4436.
- ^ а б Линда Дж. Хеффнер; Дэнни Дж. Шуст (2010). Репродуктивная система: краткий обзор. Джон Уайли и сыновья. стр.16 –. ISBN 978-1-4051-9452-5. Получено 28 ноября 2010.
- ^ Нахар Л., Саркер С.Д., Тернер А.Б. (2007). «Обзор синтетических и природных димеров стероидов: 1997-2006». Curr Med Chem. 14 (12): 1349–1370. Дои:10.2174/092986707780597880. PMID 17504217.
- ^ Адамс Дж. С. (2005). ""Привязано к работе: пересмотр гипотезы свободных гормонов. Клетка. 122 (5): 647–9. Дои:10.1016 / j.cell.2005.08.024. PMID 16143095.
- ^ Хаммес А (2005). «Роль эндоцитоза в клеточном поглощении половых стероидов». Клетка. 122 (5): 751–62. Дои:10.1016 / j.cell.2005.06.032.
- ^ а б c Орен I (2004). «Свободная диффузия стероидных гормонов через биомембраны: симплексный поиск с неявными расчетами модели растворителя». Биофизический журнал. 87 (2): 768–79. Дои:10.1529 / biophysj.103.035527. ЧВК 1304487.
- ^ а б Руссо Г. (2013). «Пятьдесят лет назад: поиск рецепторов стероидных гормонов». Молекулярная и клеточная эндокринология. 375 (1–2): 10–3. Дои:10.1016 / j.mce.2013.05.005. PMID 23684885.
- ^ Мур Флорида, Эванс SJ (1995). «Стероидные гормоны используют негеномные механизмы для управления функциями и поведением мозга: обзор доказательств». Развитие мозга. 54 (4): 41–50. Дои:10.1159/000006610. PMID 10516403.
- ^ Marcinkowska E, Wiedłocha A (2002). «Передача стероидного сигнала, активированная на клеточной мембране: от растений к животным». Акта Биохим Пол. 49 (9): 735–745. PMID 12422243.
- ^ Ван Ц., Лю И, Цао Дж. М. (2014). «Рецепторы, связанные с G-белком: экстраядерные медиаторы для негеномного действия стероидов». Международный журнал молекулярных наук. 15 (9): 15412–25. Дои:10.3390 / ijms150915412. ЧВК 4200746. PMID 25257522.
дальнейшее чтение
- Брук CG (1999). «Механизм полового созревания». Horm. Res. 51 Дополнение 3 (3): 52–4. Дои:10.1159/000053162. PMID 10592444.
- Холмс С.Дж., Шале С.М. (1996). «Роль гормона роста и половых стероидов в достижении и поддержании нормальной костной массы». Horm. Res. 45 (1–2): 86–93. Дои:10.1159/000184765. PMID 8742125.
- Оттоленги К., Уда М., Криспони Л., Омари С., Цао А., Форабоско А., Шлессингер Д. (январь 2007 г.). «Определение и стабильность пола». BioEssays. 29 (1): 15–25. Дои:10.1002 / bies.20515. PMID 17187356.
- Couse JF, Korach KS (июнь 1998 г.). «Изучение роли половых стероидов посредством исследований мышей с дефицитом рецепторов». J. Mol. Med. 76 (7): 497–511. Дои:10.1007 / s001090050244. PMID 9660168.
- МакИвен Б.С. (1992). «Стероидные гормоны: влияние на развитие и функции мозга». Horm. Res. 37 Дополнение 3 (3): 1–10. Дои:10.1159/000182393. PMID 1330863.
- Саймонс (август 2008 г.). «физиологическое и фармакологическое действие стероидных гормонов». BioEssays. 30 (8): 744–56. Дои:10.1002 / bies.20792. ЧВК 2742386. PMID 18623071.
- Han, Thang S .; Уокер, Брайан Р .; Арльт, Вибке; Росс, Ричард Дж. (17 декабря 2013 г.). «Лечение и результаты здоровья взрослых с врожденной гиперплазией надпочечников». Обзоры природы Эндокринология. 10 (2): 115–124. Дои:10.1038 / nrendo.2013.239. PMID 24342885 Рисунок 2: Путь стероидогенеза надпочечников.
