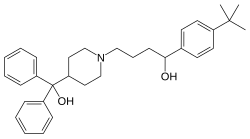
Терфенадин - Terfenadine
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Селдейн, Трилудан, Телдане |
| AHFS /Drugs.com | Информация для потребителей Multum |
| MedlinePlus | a600034 |
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Связывание с белками | 70% |
| Метаболизм | Печеночный (CYP3A4 ) |
| Метаболиты | Фексофенадин |
| Устранение период полураспада | 3,5 часа |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.051.537 |
| Химические и физические данные | |
| Формула | C32ЧАС41NО2 |
| Молярная масса | 471.685 г · моль−1 |
| 3D модель (JSmol ) | |
| Хиральность | Рацемическая смесь |
| |
| |
| | |
Терфенадин является антигистаминный препарат ранее использовался для лечения аллергический условия. Он был выведен на рынок Хёхст Марион Руссель (сейчас же Санофи-Авентис ) и продавалась под различными торговыми марками, в том числе Seldane в Соединенные Штаты, Трилудан в объединенное Королевство, и Teldane в Австралия.[1] Он был заменен фексофенадин в 1990-е годы из-за риска определенного типа нарушения электрических ритмов сердца (в частности, аритмия сердца вызванный QT интервал продление) и был снят с рынков по всему миру.[2]:53
Фармакология
Терфенадин действует как периферически-селективный антигистаминный препарат, или же антагонист из гистамин ЧАС1 рецептор. Это пролекарство, как правило, полностью метаболизируется к активной форме фексофенадин в печень посредством фермент цитохром P450 3A4. Из-за почти полного метаболизма в печени сразу после выхода из кишечника, терфенадин обычно не измеряется в плазме. Однако сам Терфенадин кардиотоксический в более высоких дозах, в то время как его основные активный метаболит не является. Терфенадин, помимо своего антигистаминного действия, также действует как блокатор калиевых каналов (Kv11.1 кодируется геном hERG ). Поскольку его активный метаболит не является блокатором калиевых каналов, кардиотоксичность не связана с фексофенадин.[3] Внезапная токсичность возможна даже после многих лет без проблем в результате взаимодействия с другими лекарствами, такими как эритромицин или продукты, такие как грейпфрут. Добавление или увеличение дозировки этих ингибиторов CYP3A4 затрудняет метаболизм и выведение терфенадина из организма. В более высоких концентрациях в плазме это может привести к токсическому воздействию на сердечный ритм (например, вентрикулярная тахикардия и torsades de pointes ).
История
В Соединенных Штатах Seldane был выпущен на рынок в 1985 году как первый неседативный антигистаминный препарат для лечения аллергический ринит.[1][4] В июне 1990 года доказательства серьезных желудочковых аритмий у тех, кто принимал Селдейн, побудили FDA опубликовать отчет о факторы риска связана с сопутствующий использование препарата с макролид антибиотики и кетоконазол.[1] Два месяца спустя FDA потребовало, чтобы производитель разослал письмо всем врачам, предупреждая их о проблеме; в июле 1992 г. существующие меры предосторожности были повышены до предупреждение о черном ящике[1] и эта проблема привлекла внимание средств массовой информации в сообщениях о том, что люди с заболеваниями печени или принимавшие кетоконазол, противогрибковое средство или антибиотик эритромицин, мог пострадать аритмия сердца если бы они также взяли Селдейна.[4]
В январе 1997 года, в том же месяце, когда США Управление по контролю за продуктами и лекарствами (FDA) ранее одобрила генерическую версию Seldane, произведенную Корпорация IVAX в Майами FDA рекомендовало удалить с рынка терфенадин-содержащие препараты, а врачи рассмотрят альтернативные лекарства для своих пациентов.[4] Seldane (и Seldane-D, терфенадин в сочетании с деконгестантом) псевдоэфедрин ) были удалены с рынка США их производителем в конце 1997 года после одобрения FDA препарата Allegra-D (фексофенадин / псевдоэфедрин).[5] Лекарства, содержащие терфенадин, были впоследствии удалены с канадского рынка в 1999 г.[6] и больше не продаются по рецепту в Великобритании.[7]
Рекомендации
- ^ а б c d Томпсон Д., Остер Г. (май 1996 г.). «Применение терфенадина и противопоказанных препаратов». JAMA. Американская медицинская ассоциация. 275 (17): 1339–41. Дои:10.1001 / jama.275.17.1339. PMID 8614120.
- ^ Горак Ф (2010). «Антиаллергические и вазоактивные препараты от аллергического ринита, глава 4». В Pawankar R, Holgate ST, Rosenwasser LJ (ред.). Границы аллергии: терапия и профилактика. Allergy Frontiers. 5. Springer Science & Business Media. ISBN 978-4-431-99362-9.
- ^ Рой М., Дюмен Р., Браун А.М. (август 1996 г.). "HERG, первичная желудочковая мишень человека не вызывающего седативного эффекта антигистаминного терфенадина". Тираж. Американская Ассоциация Сердца. 94 (4): 817–23. Дои:10.1161 / 01.cir.94.4.817. PMID 8772706.
- ^ а б c Розенталь (14 января 1997 г.). "FDA может остановить Селдейна". Los Angeles Daily News. TheFreeLibrary.com. Получено 2010-11-11 - через AP.
- ^ «FDA одобряет Allegra-D, производителя, чтобы вывести Seldane с рынка». Управление по контролю за продуктами и лекарствами. Архивировано из оригинал на 2008-02-23. Получено 2010-11-11.
- ^ «Статус терфенадин-содержащих препаратов в Канаде». Министерство здравоохранения Канады. 23 апреля 2004 г. Архивировано с оригинал 13 июля 2006 г.
- ^ «Терфенадин - тетрадь общей практики». GPnotebook.co.uk. Oxbridge Solutions Lt.
