Закон Гей-Люссака - Википедия - Gay-Lussacs law
| Часть серии по | ||||
| Механика сплошной среды | ||||
|---|---|---|---|---|
Законы
| ||||
Закон гея (правильнее называть Закон Амонтона) утверждает, что давление данной массы газа напрямую зависит от абсолютной температуры газа, когда объем поддерживается постоянным.[1]
Математически это можно записать так: .
Гей-Люссак ошибочно признан за Закон давления, который установил, что давление заключенного газа прямо пропорционально его температуре и который он сформулировал первым (ок. 1809 г.).[2] Ему также иногда приписывают[3][4][5] будучи первым, кто опубликовал убедительные доказательства, показывающие взаимосвязь между давлением и температурой фиксированной массы газа, сохраняемой в постоянном объеме.[4]
Эти законы также известны как Закон давления или Закон Амонтона и Закон Дальтона соответственно.[3][4][5][6]
Закон объединения объемов
Закон объединения объемов гласит, что когда газы реагируют вместе, они делают это в объеме, который имеет простое целочисленное отношение, при условии, что температура и давление реагирующих газов и их продуктов остаются постоянными.
Соотношение между объемами реагирующих газов и газообразных продуктов можно выразить простым целые числа.
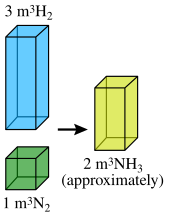
Например, Гей-Люссак обнаружил, что два объема водорода и один объем кислорода будут реагировать с образованием двух объемов газообразной воды. На основании результатов Гей-Люссака, Амедео Авогадро предположил, что при одинаковых температуре и давлении равные объемы газа содержат равное количество молекул (Закон Авогадро ). Эта гипотеза означала, что ранее заявленный результат
- 2 объема водорода + 1 объем кислорода = 2 объема газообразной воды
можно также выразить как
- 2 молекулы водорода + 1 молекула кислорода = 2 молекулы воды.
Это также можно выразить другим способом, например, 100 мл водорода объединяются с 50 мл кислорода, чтобы получить 100 мл водяного пара: водород (100 мл) + кислород (50 мл) = вода (100 мл)
Таким образом, объемы водорода и кислорода, которые объединяются (т.е. 100 мл и 50 мл), имеют простое соотношение 2: 1.
Закон объединения газов был обнародован Жозеф Луи Гей-Люссак в 1808 г.[7][8] Однако гипотеза Авогадро не была принята химиками до тех пор, пока итальянский химик Станислао Канниццаро смог убедить Первый международный химический конгресс в 1860 г.[9]
Закон давление-температура
Этот закон часто называют Закон Гей-Люссака давления – температурымежду 1800 и 1802 годами открыли взаимосвязь между давлением и температурой фиксированной массы газа, сохраняемой в постоянном объеме.[10][11][12] Гей Люссак обнаружил это при создании «воздушного термометра».
Давление газа фиксированного масса и исправлено объем является прямо пропорциональный до абсолютной температуры газа.

Если температура газа увеличивается, то увеличивается и его давление, если масса и объем газа остаются постоянными. Этот закон имеет особенно простую математическую форму, если температура измеряется по абсолютной шкале, например, в кельвины. Тогда закон можно математически выразить как
или же
куда:
- п это давление газа,
- Т это температура газа (измеряется в кельвины ),
- k это постоянный.
Этот закон верен, потому что температура является мерой среднего кинетическая энергия вещества; по мере увеличения кинетической энергии газа его частицы быстрее сталкиваются со стенками контейнера, тем самым создавая повышенное давление.
Для сравнения одного и того же вещества при двух различных наборах условий закон можно записать как:
Поскольку Амонтон открыл закон заранее, имя Гей-Люссака теперь в химии обычно ассоциируется с законом объединения объемов, обсуждаемым в разделе выше. Некоторые вводные учебники по физике все еще определяют зависимость давления от температуры как закон Гей-Люссака.[13][14][15] Гей-Люссак в первую очередь исследовал взаимосвязь между объемом и температурой и опубликовал ее в 1802 году, но его работа действительно охватывала некоторое сравнение между давлением и температурой.[16] Учитывая относительную технологию, доступную обоим мужчинам, Амонтон мог работать только с воздухом в качестве газа, тогда как Гей-Люссак мог экспериментировать с несколькими типами общих газов, такими как кислород, азот и водород.[17] Гей-Люссак приписал свои открытия Жак Шарль потому что он использовал большую часть неопубликованных данных Чарльза с 1787 года, поэтому закон стал известен как Закон Чарльза или закон Шарля и Гей-Люссака.[18]
Закон Гей-Люссака (Амонтона), Закон Чарльза, и Закон Бойля сформировать комбинированный газовый закон. Эти три закона газа в сочетании с Закон Авогадро можно обобщить закон идеального газа.
Расширение газов
Гей-Люссак использовал формулу, полученную из ΔV / V = αΔT, чтобы определить скорость расширения α для газов. Для воздуха он нашел относительное расширение ΔV / V = 37,50% и получил значение α = 37,50% / 100 ° C = 1 / 266,66 ° C, которое указывает на то, что значение абсолютный ноль была примерно 266,66 ° C ниже 0 ° C.[19] Значение скорости расширения α приблизительно одинаково для всех газов, и это также иногда называют законом Гей-Люссака.
Смотрите также
- Закон Авогадро - Соотношение между объемом и количеством молей газа при постоянной температуре и давлении.
- Закон Бойля - Соотношение между давлением и объемом в газе при постоянной температуре
- Закон Чарльза - Связь между объемом и температурой газа при постоянном давлении
- Закон о комбинированном газе - Сочетание газовых законов Шарля, Бойля и Гей-Люссака.
Рекомендации
- ^ "Закон Гей-Люссака". LibreTexts. 2016-06-27. Получено 5 декабря 2018.
- ^ Лагассе, Поль (2016), "Жозеф Луи Гей-Люссак", Колумбийская электронная энциклопедия (6-е издание, 2-е изд.), Колумбийский университет, ISBN 978-0787650155[страница нужна ]
- ^ а б Палмер, WP (1991), «Филателия, преподавание естественных наук и история науки» (PDF), Лабораторный разговор, 35 (1): 30–31
- ^ а б c Холброу, Швейцария; Амато, JC (2011), «Что Гей-Люссак нам не сказал», Являюсь. J. Phys., 79 (1): 17, Bibcode:2011AmJPh..79 ... 17H, Дои:10.1119/1.3485034
- ^ а б Спургин, CB (1987), "эксперименты Гей-Люссака по расширению газа и традиционное неверное учение закона Чарльза.'", Анналы науки, 44 (5): 489–505, Дои:10.1080/00033798700200321
- ^ Crosland MP (1961), "Истоки закона Гей-Люссака об объединении объемов газов", Анналы науки, 17 (1): 1, Дои:10.1080/00033796100202521
- ^ Гей-Люссак (1809) "Mémoire sur la combinaison des gazeuses, les unes avec les autres" (Воспоминания о соединении газообразных веществ друг с другом), Mémoires de la Société d'Arcueil 2: 207–234. Доступно на английском языке по адресу: Колледж Ле Мойн.
- ^ "Жозеф-Луи Гей-Люссак". chemistryexplained.com.
- ^ Хартли Гарольд (1966). «Станислао Канниццаро, F.R.S. (1826–1910) и Первая Международная химическая конференция в Карлсруэ». Примечания и отчеты Лондонского королевского общества. 21 (1): 56–63. Дои:10.1098 / рснр.1966.0006. S2CID 58453894.
- ^ Барнетт, Мартин К. (август 1941 г.), «Краткая история термометрии», Журнал химического образования, 18 (8): 358, Bibcode:1941JChEd..18..358B, Дои:10.1021 / ed018p358. Извлекать.
- ^ "История газовых законов Талла". Архивировано из оригинал на 2010-09-08. Получено 2010-07-16.
- ^ Видеть:
- Амонтонс Г. (представлен в 1699 г., опубликован в 1732 г.) "Moyens de substitute product l'action du feu à la force des hommes et des chevaux pour mouvoir les machines" (Способы удобной замены силы людей и лошадей действием огня для приведения в действие машин), Mémoires de l’Académie des Sciences de Paris, 112–126; особенно см. стр. 113–117.
- Амонтонс Г. (представлен в 1702 г., опубликован в 1743 г.) "Discours sur quelques propriétés de l'Air, & le moyen d'en connoître la température dans tous les climats de la Terre" (Рассуждение о некоторых свойствах воздуха и о способах определения температуры во всех климатах Земли), Mémoires de l’Académie des Sciences de Paris, 155–174.
- См. Также: Fontenelle, B. B. (1743) "Sur une nouvelle proprieté de l'air, et une nouvelle construction de Thermométre" (О новом свойстве воздуха и новой конструкции термометра), Histoire de l'Academie Royale des Sciences, 1–8.
- ^ Типпенс, Пол Э. (2007). Физика, 7 изд. Макгроу-Хилл. 386–387.
- ^ Купер, Кристал (11 февраля 2010 г.). «Закон Гей-Люссака». Bright Hub Engineering. Извлекаются из http://www.brighthubengineering.com/hvac/26213-gay-lussacs-law/ 8 июля 2013 г.
- ^ Верма, К. - Cengage Physical Chemistry Часть 1 - Раздел 5.6.3
- ^ Кросланд, Морис П. (2004). Гей-Люссак: ученый и буржуа. Издательство Кембриджского университета. 119–120.
- ^ Азимов, Исаак (1966). Понимание физики - движение, звук и тепло. Уокер и Ко. 191–192.
- ^ Гей-Люссак (1802 г.), "Recherches sur la dilatation des gaz et des vapeurs" (Исследования по расширению газов и паров), Annales de Chimie 43: 137–175. На странице 157 Гей-Люссак упоминает неопубликованные находки Шарля: «Avant d'aller plus loin, je dois prévenir que quoique j'eusse reconnu un grand nombre de fois que les gaz oxigène, azote, hydrogène et acide carbonique, et l 'air atmosphérique se dilatent également depuis 0 ° jusqu'a 80 °, le cit. Charles avait remarqué depuis 15 ans la même propriété dans ces gaz; mais n'avant jamais publié ses résultats, c'est par le plus grand hasard que je je les ai connus. " (Прежде чем продолжить, я должен сообщить [вам], что, хотя я много раз осознавал, что газы кислород, азот, водород и углекислота [т.е. углекислый газ] и атмосферный воздух также расширяются от 0 ° до 80 °, гражданин Чарльз заметил 15 лет назад то же свойство в этих газах; но, так и не опубликовав свои результаты, я по чистой случайности знал о них.) Доступно на английском языке по адресу: Колледж Ле Мойн.
- ^ Гей-Люссак (1802 г.). "Recherches sur la dilatation des gaz et des vapeurs". Annales de chimie, ou, Recueil de mémoires Concerant la chimie (На французском).
дальнейшее чтение
- Castka, Джозеф Ф .; Меткалф, Х. Кларк; Дэвис, Раймонд Э .; Уильямс, Джон Э. (2002). Современная химия. Холт, Райнхарт и Уинстон. ISBN 978-0-03-056537-3.
- Гуч, Ян (2003). Полное руководство идиота по химии. Альфа, Penguin Group Inc. ISBN 978-1-59257-101-7.
- Маскетта, Джозеф А. (1998). Как подготовиться к SAT II Chemistry. Баррона. ISBN 978-0-7641-0331-5.