Придопидин - Pridopidine
 | |
| Имена | |
|---|---|
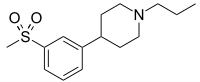
| Название ИЮПАК 4- (3- (Метилсульфонил) фенил) -1-пропилпиперидин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.240.998 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C15ЧАС23NО2S | |
| Молярная масса | 281.41 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Придопидин (ранее Huntexil, ACR16, также ASP2314) представляет собой низкомолекулярный кандидат для исследования биодоступных перорально биодоступных веществ. Это очень селективный Рецептор сигма-1 (S1R) агонист.[1][2] S1R регулирует ключевые клеточные процессы, относящиеся к нейродегенеративным заболеваниям, такие как гомеостаз кальция, динамика цитоскелета, восстановление здоровья митохондрий и высвобождение нейротрофических факторов. S1R участвует в клеточной дифференцировке, нейропластичности, нейропротекции и когнитивном функционировании мозга.
Придопидин положительно влияет на регулируемые S1R пути по нейродегенеративным показаниям и показаниям нервного развития, включая защиту от повреждения аксонов и нейронов, восстановление нарушений позвоночника, усиление секреции BDNF и восстановление функции митохондрий.
Ранее считалось, что приодопин является антагонистом D2R, но это оказалось неверным.[3]
Придопидин находится на поздней стадии разработки Prilenia Therapeutics. Ранее он принадлежал Teva Pharmaceutical Industries кто приобрел права на продукт у его первоначального разработчика NeuroSearch в 2012.
Придопидин - первый препарат, показавший статистически значимое влияние на поддержание функциональной способности при БХ,[4] как измеряется общей функциональной емкостью (TFC). Этот эффект был наиболее заметным у пациентов с ранней стадией HD.[5]
В то время как в низких дозах Придопидин влияет на S1R, в более высоких дозах он взаимодействует с другими мишенями, включая дофамин D3, адренергический α2C и серотонинергический 5-HT1A, которые являются установленными терапевтическими мишенями для дискинезии, вызванной болезнью Паркинсона леводопой (PD-LID). Это вероятный механизм явного эффекта, наблюдаемого в «золотом стандарте» модели приматов, не относящихся к человеку, для PD-LID - макак, пораженных MPTP.[6] Эта модель считается очень успешной в клинических испытаниях фазы 2.
Придопидин в настоящее время находится в клинической фазе 2 для PD-LID,[7] и был недавно выбран[8][9] принять участие в испытании новой платформы для БАС, проведенном Центром Шона М. Хили и AMG по БАС при Массачусетской больнице общего профиля.
Рекомендации
- ^ Джонстон, Том Х .; Гева, Михал; Штайнер, Лилах; Орбах, Арик; Папапетропулос, Спирос; Савола, Джуха-Матти; Рейнольдс, Ян Дж .; Рэйвенскрофт, Паула; Хилл, Майкл (май 2019 г.). «Придопидин, готовое к клиническому применению соединение, снижает дискинезию, вызванную 3,4-дигидроксифенилаланином, у паркинсонических макак». Двигательные расстройства. 34 (5): 708–716. Дои:10.1002 / mds.27565. ISSN 1531-8257. PMID 30575996.
- ^ Сахлхольм, Кристоффер; Sijbesma, Jurgen W.A .; Маас, Брам; Квизера, Шанталь; Марчеллино, Даниэль; Рамакришнан, Ниша К .; Dierckx, Rudi A. J. O .; Elsinga, Philip H .; ван Ваард, Арен (сентябрь 2015 г.). «Придопидин селективно захватывает сигма-1, а не рецепторы допамина D2 в поведенчески активных дозах». Психофармакология. 232 (18): 3443–3453. Дои:10.1007 / s00213-015-3997-8. ISSN 1432-2072. ЧВК 4537502. PMID 26159455.
- ^ Сахлхольм, Кристоффер; Sijbesma, Jurgen W. A .; Маас, Брам; Квизера, Шанталь; Марчеллино, Даниэль; Рамакришнан, Ниша К .; Dierckx, Rudi A. J. O .; Elsinga, Philip H .; ван Ваард, Арен (сентябрь 2015 г.). «Придопидин селективно захватывает сигма-1, а не рецепторы допамина D2 в поведенчески активных дозах». Психофармакология. 232 (18): 3443–3453. Дои:10.1007 / s00213-015-3997-8. ISSN 1432-2072. ЧВК 4537502. PMID 26159455.
- ^ «Пациенты Хантингтона могут увидеть отсрочку функционального снижения при приеме придопидина». Новости болезни Хантингтона. 2017-04-20. Получено 2019-09-21.
- ^ «Испытание показало, что препарат Тева может замедлить болезнь Хантингтона». en.globes.co.il (на иврите). 2016-09-19. Получено 2019-09-21.
- ^ Джонстон, Том Х .; Гева, Михал; Штайнер, Лилах; Орбах, Арик; Папапетропулос, Спирос; Савола, Джуха-Матти; Рейнольдс, Ян Дж .; Рэйвенскрофт, Паула; Хилл, Майкл (май 2019 г.). «Придопидин, готовое к клиническому применению соединение, снижает дискинезию, вызванную 3,4-дигидроксифенилаланином, у паркинсонических макак». Двигательные расстройства. 34 (5): 708–716. Дои:10.1002 / mds.27565. ISSN 1531-8257. PMID 30575996.
- ^ «Исследование по оценке безопасности и эффективности придопидина по сравнению с плацебо в лечении дискинезии, вызванной леводопой, у пациентов с болезнью Паркинсона - Просмотр полного текста - ClinicalTrials.gov». Clinicaltrials.gov. Получено 2019-09-21.
- ^ «Шон М. Хили и Центр AMG по БАС в Mass General запускают первое испытание платформы БАС с 5 многообещающими препаратами». Массачусетская больница общего профиля. Получено 2019-09-21.
- ^ «Придопидин выбран для участия в первом испытании платформы ALS». www.businesswire.com. 2019-09-18. Получено 2019-09-21.
