Хонокиол - Honokiol
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2- (4-гидрокси-3-проп-2-енилфенил) - 4-проп-2-енилфенол | |
| Другие имена houpa, hnk | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.122.079 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС18О2 | |
| Молярная масса | 266,334 г / моль |
| Внешность | Белое твердое вещество |
| умеренно (25 ° C) | |
| Родственные соединения | |
Связанный бифенолы | диэтилстильбестрол, дигидроксиэвгенол |
Родственные соединения | магнолол. 4-O-Methylhonokiol |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хонокиол это лигнан изолированные от коры, семенные шишки и листья деревьев, принадлежащих к роду Магнолия. Он был признан одним из химические соединения в некоторых традиционных восточных лекарственных травах вместе с магнолол, 4-O-метилхонокиол, и обоватол.
Биология
Хонокиол был извлечен из ряда видов Магнолия родом из многих регионов земного шара. Магнолия крупноцветковая, который является родным для юга Америки, а также таких мексиканских видов, как Магнолия дейбата были обнаружены источники хонокиола.[1] Традиционно в азиатской медицине Магнолия biondii, Магнолия обратнояйская, и Магнолия лекарственная обычно используются.[2] Само соединение имеет пряный запах.
Из-за своих физических свойств хонокиол может легко пересекать гематоэнцефалический барьер и гематоэнцефалический барьер.[1][3] В результате гонокиол является потенциально сильнодействующим препаратом с высоким содержанием биодоступность.
Химия
Структура
Хонокиол относится к классу бифенолов неолигнанов. Как полифенол он относительно невелик и может взаимодействовать с белками клеточной мембраны посредством межмолекулярных взаимодействий, таких как водородная связь, гидрофобные взаимодействия, или же ароматный Пи-орбитальная ковалентность.[1] Он гидрофобен и легко растворяется в липидах. Конструктивно похож на пропофол.[1]
Очищение
Есть несколько методов очистки и выделения хонокиола. В природе хонокиол существует в виде структурного изомера. магнолол, который отличается от хонокиола только положением одного гидроксильная группа. Из-за очень схожих свойств магнолола и гонокиола очистка часто ограничивается ВЭЖХ или же электромиграция. Однако методы, разработанные в 2006 г. сотрудниками лаборатории г. Джек Л. Арбайзер, воспользовались близостью фенольных гидроксильных групп в магнололе, которые образуют защищаемый диол, чтобы создать магнолол ацетонид (Рисунок 1), с последующей простой очисткой через флэш-хроматография над кремнезем.[4]
Рисунок 1

Кроме того, метод быстрого разделения был опубликован в Журнал хроматографии А в 2007 году. В процессе используются высокопроизводительные высокоскоростные противоточная хроматография (HSCCC высокой емкости).[5] С помощью этого метода хонокиол можно отделить и очистить до чистоты выше 98% с высоким выходом менее чем за час.
История
Традиционная медицина

Экстракты из коры или семенных шишек Магнолия дерево широко использовалось в традиционной медицине Китая, Кореи и Японии.[2]
Кора магнолии традиционно использовалась в восточной медицине как болеутоляющее, а также для лечения тревожности и расстройств настроения.[2][6] В традиционная китайская медицина, кора магнолии называется Houpu и чаще всего берется от двух видов, Магнолия обратнояйская и Магнолия лекарственная.[7] Некоторые китайские традиционные формулы, содержащие хоупу, включают Banxia Houpu Tang (半夏 厚朴 丸), Xiao Zhengai Tang, Ping Wei San (平胃散) и Shenmi Tang.[2] Японский Кампо формулы включают Hange-koboku-to (半夏 厚朴 湯) и Sai-boku-to (柴 朴 湯).[2][6]

Западные медицинские исследования
Эта секция нужно больше медицинские справки за проверка или слишком сильно полагается на основные источники. (Июнь 2014 г.) |
Хонокиол - это плейотропное соединение, что означает, что он может воздействовать на организм несколькими путями. Такое разнообразие взаимодействий делает его жизнеспособным средством лечения ряда состояний в Центральная нервная система, сердечно-сосудистая система, и желудочно-кишечный тракт. Было показано, что он также обладает противоопухолевым, противовоспалительным и антиоксидантным действием.[1][8][9]
Побочные эффекты и противопоказания
Исследования показали довольно ограниченный профиль побочных эффектов гонокиола, и он, по-видимому, довольно хорошо переносится. Однако его антитромботические эффекты могут вызвать кровотечение, особенно у пациентов с состояниями, которые могут подвергнуть их более высокому риску, например гемофилия или же Болезнь фон Виллебранда.[1] Кроме того, пациенты, уже принимающие антикоагулянты следует поговорить со своим врачом, прежде чем принимать добавки хонокиола. Хонокиол также нейротоксичен при высоких концентрациях. В исследовании 2002 года исследователи вызывали гибель клеток кортикальных нейронов плода крысы путем непосредственного нанесения 100 мкМ in vitro.[10]
Фармакология
Противоопухолевые действия
Хонокиол про-апоптотический эффекты в меланома, саркома, миелома, лейкемия, мочевой пузырь, легкое, предстательная железа, плоскоклеточный рак полости рта,[11] в мультиформных клетках глиобластома [12] и рак толстой кишки Сотовые линии.[13][14][15][16] Хонокиол подавляет фосфорилирование Акт, стр44 / 42 митоген-активированная протеинкиназа (MAPK) и src. Кроме того, хонокиол регулирует ядерный фактор каппа B (NF-κB) путь активации, вышестоящий эффектор фактор роста эндотелия сосудов (VEGF), MCL1, и циклооксигеназа 2 (COX-2), все существенныеангиогенный и факторы выживания. Хонокиол индуцирует каспаззависимую апоптоз TRAIL-опосредованным образом и усиливает проапоптотические эффекты доксорубицин и другие этопозиды. Проапоптотические эффекты хонокиола настолько сильны, что он преодолевает даже известные лекарственно-устойчивые новообразования, такие как множественная миелома и хронические заболевания. В-клеточный лейкоз. Хонокиол также действует на PI3K /mTOR пути в опухолевых клетках при сохранении активности пути в Т-клетки.[17]
Нейротрофическая активность
Было показано, что хонокиол способствует нейрит нарост и иметь нейропротекторный эффекты в крыса корковый нейроны. Кроме того, гонокиол увеличивает свободную цитоплазматическую Ca2+ в нейронах коры головного мозга крыс.[10] Хонокиол является слабым лигандом каннабиноидного рецептора CB2, но было показано, что встречающееся в природе производное 4-O-метилхонокиола является сильным и селективным обратным агонистом каннабиноидного рецептора CB2 и обладает антиостеокластический последствия.[18]
Антитромботическая активность
Хонокиол подавляет агрегацию тромбоцитов у кроликов дозозависимым образом и защищает культивируемый RAEC от окисления низкой плотности. липопротеин травма, повреждение. Хонокиол значительно увеличивает простациклин метаболит 6-кето-PGF1альфа, потенциально ключевой фактор в антитромботической активности хонокиола.[19]
Противовоспалительная активность
Исследования, изучающие гонокиол как защитную терапию против очаговая церебральная ишемия-реперфузия травмы выявили ряд противовоспалительных путей. Нейтрофил проникновение в поврежденные ткани может вызвать дальнейшие повреждения и проблемы с заживлением. В in vitro исследования, хонокиол снижен fMLP (N-формилметионил-лейцилфенилаланин) и PMA (форбол-12-миристат-13-ацетат ) индуцировала прочную адгезию нейтрофилов, которая является неотъемлемым этапом инфильтрации.[1][20] Хонокиол подавляет ROS продукция нейтрофилов.[20] Хонокиол также блокирует выработку воспалительного фактора в глиальные клетки через запрет на NF-κB активация.[21][22] Считается, что этот механизм подавляет производство НЕТ, фактор некроза опухоли-α (TNF-α ), и RANTES /CCL5.[21]
Антиоксидантная активность
Хонокиол также был предложен в качестве антиоксидант. Состав защищает от перекисное окисление липидов путем вмешательства в производство и миграцию ROS.[20] Накопление АФК внеклеточно вызывает макромолекулярное повреждение, в то время как внутриклеточное накопление может вызывать цитокин активация.
Подавление цитотоксичности
Один из способов, которым гонокиол действует как нейропротектор, - это клеточная регуляция и последующее ингибирование цитотоксичности. Для достижения этого ингибирования используются два механизма: ГАМК.А Модуляция и Ca2+ Торможение. Ингибирование цитотоксичности может быть нейропротективным механизмом хонокиола. Также было показано, что хонокиол подавляет повторяющуюся стрельбу, блокируя глутамат.[23]
ГАМКА модуляция
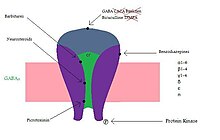
Считается, что хонокиол действует на ГАМКА рецепторы аналогично бензодиазепины и Z-препараты. Однако было показано, что хонокиол вызывает анксиолиз с меньшим количеством моторных или когнитивных побочных эффектов, чем ГАМК.А агонисты рецепторов, такие как флуразепам и диазепам. Было показано, что хонокиол, вероятно, имеет более высокую селективность в отношении различных ГАМК.А подтипы рецепторов и магнолол, и гонокиол показали более высокую эффективность при действии на рецепторы, содержащие субъединицы δ.[1] ГАМКА рецепторы контролируют лиганд-зависимый Cl− каналы, которые могут помочь увеличить пороги судорожных припадков за счет притока анионов хлорида. Гонокиол также может влиять на синтез ГАМК. В исследовании, в котором мыши получали семь ежедневных инъекций гонокиола, исследователи наблюдали значительное увеличение гиппокамп уровни глутаматдекарбоксилаза (GAD) (67) предшественник ГАМК.[24]
Ca2+ торможение
Высокая концентрация Са2+ побуждает эксайтотоксичность который считается основным механизмом двигательных расстройств, таких как ALS, болезнь Паркинсона и судорожные расстройства, такие как эпилепсия. Хонокиол разрушает интерфейсы постсинаптического белка плотности (PSD95 ) и нейрональной синтазы оксида азота (nNOS ).[1] Связь PSD95 и nNOS с рецептором NMDA вызывает конформационные изменения, ответственные за внутриклеточный приток Са2+ что, в свою очередь, может быть путем нейротоксичности. Перегрузка кальцием также может вызвать повреждение из-за чрезмерной активации ферментов, стимулируемых кальцием. Хонокиол может снизить приток кальция за счет ингибирования fMLP, AlF.4−, и тапсигаргин G-белок пути.[20]
Противовирусная активность
Было показано, что хонокиол подавляет вирус гепатита С (HCV) инфекция in vitro.[25] Обладает слабой активностью in vitro против Вирус иммунодефицита человека (ВИЧ-1).[4]
Метаболическая активность
Было показано, что хонокиол нормализует уровень глюкозы в крови и предотвращает увеличение массы тела у мышей с диабетом, действуя как агонист PPARgamma.[26]
Фармакокинетика
В фармакокинетика хонокиола были исследованы на крысах и мышах; однако необходимы дальнейшие исследования на людях.[27] Внутривенное введение 5-10 мг / кг на моделях грызунов показало период полувыведения из плазмы около 40-60 минут, в то время как внутрибрюшинные инъекции 250 мг / кг имели период полувыведения из плазмы около 4-6 часов с максимальной концентрацией в плазме между 20–30 минут.[1][28]
Способы доставки
Хонокиол чаще всего принимают внутрь. Есть ряд доступных добавок, содержащих хонокиол. Чай из магнолии, приготовленный из коры дерева, также является распространенным методом доставки хонокиола.[нужна цитата ] И коренные американцы, и японская медицина используют полоскания с чаем для лечения зубной боли и боли в горле.[29] Поскольку гонокиол очень гидрофобен, он должен быть растворен в липиде для многих способов доставки. Во многих текущих исследованиях на животных соединение растворяется в липидном смягчающем средстве и доставляется через внутрибрюшинная инъекция. Продолжается[когда? ] работа над разработкой липосомальных эмульсий для внутривенного введения.[27]
Рекомендации
- ^ а б c d е ж грамм час я j Вудбери, Анна; Ю, Шань Пин; Вэй, Линг; Гарсия, Пол (2013). «Нейромодулирующие эффекты хонокиола: обзор». Границы неврологии. 265 (7): 4111–5. Дои:10.3389 / fneur.2013.00130. PMID 2406271.
- ^ а б c d е Ли, Юнг-Юнг; Ли, Йут Мо; Ли, Чонг-Кил; Юнг, Джэ Гён; Хан, Санг Бэ; Хун, Джин Тэ (2011). «Терапевтическое применение соединений семейства магнолий». Фармакология и терапия. 130 (2): 157–76. Дои:10.1016 / j.pharmthera.2011.01.010. PMID 21277893.
- ^ Ван, Сяньхуо; Дуань, Синмэй; Ян, Гуанли; Чжан, Хао; Дэн, Чунъян; Вэнь Цзяолинь; Ван, Нин; Пэн, Ченг; Чжао, Ся; Вэй, Юйцюань; Чен, Лицзюань; Вэй, Юйцюань; Чен, Лицзюань (2011). «Хонокиол скрещивает BBB и BCSFB и ингибирует рост опухоли головного мозга на модели интрацеребральной глиосаркомы 9L крысы и модели глиомы ксенотрансплантата U251 человека». PLOS ONE. 6 (4): e18490. Bibcode:2011PLoSO ... 618490W. Дои:10.1371 / journal.pone.0018490. ЧВК 3084695. PMID 21559510.
- ^ а б Амблард, Франк; Делинский, Дэвид; Арбисер, Джек Л .; Схинаци, Раймонд Ф. (2006). «Простая очистка хонокиола и его противовирусные и цитотоксические свойства». Журнал медицинской химии. 49 (11): 3426–7. Дои:10,1021 / jm060268m. ЧВК 3195338. PMID 16722664.
- ^ Чен, Лицзюань; Чжан, Цян; Ян, Гуанли; Фан, Линью; Тан, Джеймс; Гаррард, Ян; Игнатова, Светлана; Фишер, Дерек; Сазерленд, Ян А. (2007). «Быстрая очистка и масштабирование гонокиола и магнолола с использованием высокопроизводительной высокоскоростной противоточной хроматографии». Журнал хроматографии А. 1142 (2): 115–22. Дои:10.1016 / j.chroma.2006.09.098. PMID 17222860.
- ^ а б Саррис, Джером; Макинтайр, Эрика; Кэмфилд, Дэвид А. (2013). «Лекарства на растительной основе от тревожных расстройств, часть 1». Препараты ЦНС. 27 (3): 207–19. Дои:10.1007 / s40263-013-0044-3. HDL:11343/216777. PMID 23436255. S2CID 207485984.
- ^ Маруяма, Юдзи; Kuribara, H .; Morita, M .; Юдзурихара, М .; Вайнтрауб, С. (1998). «Идентификация магнолола и хонокиола в качестве анксиолитических агентов в экстрактах сайбоку-то, восточного фитотерапевта». Журнал натуральных продуктов. 61 (1): 135–138. Дои:10.1021 / np9702446. PMID 9461663.
- ^ Fried, Levi E .; Арбисер, Джек Л. (2009). «Хонокиол, многофункциональное антиангиогенное и противоопухолевое средство». Антиоксиданты и редокс-сигналы. 11 (5): 1139–48. Дои:10.1089 / ars.2009.2440. ЧВК 2842137. PMID 19203212.
- ^ Герра-Арайса, Кристиан; Альварес-Мехиа, Ана Лаура; Санчес-Торрес, Стефани; Фарфан-Гарсия, Юнис; Мондрагон-Лозано, Родриго; Пинто-Алмазан, Родольфо; Сальгадо-Себальос, Хермелинда (2013). «Влияние природных экзогенных антиоксидантов на старение и нейродегенеративные заболевания». Свободные радикальные исследования. 47 (6–7): 451–62. Дои:10.3109/10715762.2013.795649. PMID 23594291. S2CID 30716241.
- ^ а б Фукуяма, Ёсиясу; Накаде, Коске; Миношима, Юка; Ёкояма, Рицуко; Чжай, Хайфэн; Мицумото, Ясухидэ (2002). «Нейротрофическая активность хонокиола на культурах корковых нейронов плода крысы». Письма по биоорганической и медицинской химии. 12 (8): 1163–1166. Дои:10.1016 / S0960-894X (02) 00112-9. PMID 11934579.
- ^ Чен, Си-руи; Лу, Руи; Дэн, Хун-ся; Ляо, штат Джорджия; Чжоу, Мин; Ли, Сяо-юй; Цзи, Нин (2011). «Хонокиол: многообещающий природный агент с небольшой молекулярной массой для ингибирования роста клеток плоскоклеточного рака полости рта». Международный журнал оральной науки. 3 (1): 34–42. Дои:10.4248 / IJOS11014. ЧВК 3469873. PMID 21449214.
- ^ Chang, K. H .; Ян М.Д. (ноябрь 2013 г.). «Хонокиол-индуцированный апоптоз и аутофагия в мультиформных клетках глиобластомы». Письма об онкологии. 6 (5): 1435–1438. Дои:10.3892 / ол.2013.1548. ЧВК 3813738. PMID 24179537.
- ^ Шигемура, Кацуми; Арбисер, Джек Л .; Сунь, Ши-Юн; Зайзафун, Маджд; Johnstone, Peter A.S .; Фудзисава, Масато; Гото, Акинобу; Векслер, Бабетта; Zhau, Haiyen E .; Чанг, Леланд В.К. (2007). «Хонокиол, натуральный растительный продукт, подавляет метастатический рост клеток рака простаты человека». Рак. 109 (7): 1279–89. Дои:10.1002 / cncr.22551. PMID 17326044. S2CID 22184445.
- ^ Ishitsuka, K .; Хидешима, Т; Хамасаки, М; Raje, N; Кумар, S; Hideshima, H; Сираиси, Н. Ясуи, Н; Роккаро, AM; Richardson, P; Подар, К; Ле Гуй, S; Чаухан, D; Тамура, К; Арбисер, Дж; Андерсон, KC (2005). «Хонокиол преодолевает обычную лекарственную устойчивость множественной миеломы человека за счет индукции каспазозависимого и независимого апоптоза». Кровь. 106 (5): 1794–800. Дои:10.1182 / кровь-2005-01-0346. ЧВК 1895215. PMID 15870175.
- ^ Battle, T. E .; Арбисер, Дж; Франк, Д.А. (2005). «Натуральный продукт гонокиол индуцирует каспазозависимый апоптоз в клетках В-клеточного хронического лимфоцитарного лейкоза (B-CLL)». Кровь. 106 (2): 690–7. Дои:10.1182 / кровь-2004-11-4273. PMID 15802533.
- ^ Бай, X .; Cerimele, F; Ушио-Фукаи, М; Waqas, M; Кэмпбелл, премьер-министр; Говиндараджан, Б; Der, CJ; Битва, Т; Франк, DA; Е, К; Мурад, Э; Дубиль, Вт; Soff, G; Арбисер, JL (2003). «Хонокиол, натуральный продукт с небольшой молекулярной массой, подавляет ангиогенез in vitro и рост опухоли in vivo». Журнал биологической химии. 278 (37): 35501–7. Дои:10.1074 / jbc.M302967200. PMID 12816951.
- ^ Крейн, Кортни; Паннер, Амит; Пайпер, Рассел; Арбисер, Джек; Парса, Эндрю (2009). «Хонокиол-опосредованное ингибирование пути PI3K / mTOR: потенциальная стратегия преодоления иммунорезистентности в глиоме, карциноме груди и простаты без воздействия на функцию Т-клеток». Журнал иммунотерапии. 32 (6): 585–592. Дои:10.1097 / CJI.0b013e3181a8efe6. ЧВК 3795513. PMID 19483651.
- ^ Шуэли, Вольфганг; Паредес, Хуан Мануэль Виверос; Клейер, Йонас; Хюфнер, Антье; Анави-Гоффер, Шарон; Радунер, Стефан; Альтманн, Карл-Хайнц; Герч, Юрг (2011). "Механизмы ингибирования остеокластогенеза новым классом обратных агонистов каннабиноидного рецептора CB2 бифенильного типа". Химия и биология. 18 (8): 1053–64. Дои:10.1016 / j.chembiol.2011.05.012. PMID 21867920.
- ^ Ху, Он; Чжан Сяо-сюэ; Ван, Инь-е; Чен, Ши-Чжун (2005). «Хонокиол подавляет артериальный тромбоз за счет защиты эндотелиальных клеток и стимуляции простациклина». Acta Pharmacologica Sinica. 26 (9): 1063–8. Дои:10.1111 / j.1745-7254.2005.00164.x. PMID 16115372.
- ^ а б c d Лиу, Го-Тонг; Шен, Юй-Чан; Чен, Чи-Фу; Цао, Чэн-Мин; Цай, Шен-Коу (2003). «Хонокиол защищает мозг крысы от очаговой церебральной ишемии-реперфузионного повреждения, подавляя инфильтрацию нейтрофилов и производство активных форм кислорода». Исследование мозга. 992 (2): 159–166. Дои:10.1016 / j.brainres.2003.08.026. PMID 14625055. S2CID 44974515.
- ^ а б Чжан, Пэн; Лю, Сяоянь; Чжу, Яньцзюнь; Чен, Шичжун; Чжоу, Демин; Ван, Инье (2012). «Хонокиол подавляет воспалительную реакцию во время реперфузии ишемии мозга, подавляя активацию NF-κB и выработку цитокинов глиальными клетками». Письма о неврологии. 534: 123–7. Дои:10.1016 / j.neulet.2012.11.052. PMID 23262090. S2CID 10051483.
- ^ Чао, Луи Куопин; Ляо, Пей-Чун; Хо, Чен-Лунг; Ван, Юджин И-Чен; Чуанг, Чао-Чин; Чиу, Хуан-Вэнь; Хунг, Ланг-Банг; Хуа, Куо-Фэн (2010). «Противовоспалительные биоактивные вещества хонокиола за счет ингибирования протеинкиназы C, митоген-активированной протеинкиназы и пути NF-κB для снижения LPS-индуцированной экспрессии TNFα и NO». Журнал сельскохозяйственной и пищевой химии. 58 (6): 3472–8. Дои:10.1021 / jf904207m. PMID 20192217.
- ^ Линь И-Руу; Чен, Хвэй-Сянь; Ко, Чиен-Синь; Чан, Мин-Хуан (2006). «Нейропротекторная активность гонокиола и магнолола при повреждении гранулярных клеток мозжечка». Европейский журнал фармакологии. 537 (1–3): 64–9. Дои:10.1016 / j.ejphar.2006.03.035. PMID 16631734.
- ^ Ку, Тянь-Сюн; Ли, И-Цзин; Ван, Су-Джейн; Фань, Чен-Хуа; Тянь, Лу-Тай (2011). «Влияние хонокиола на активность GAD (65) и GAD (67) в коре и гиппокампе мышей». Фитомедицина. 18 (13): 1126–9. Дои:10.1016 / j.phymed.2011.03.007. PMID 21561750.
- ^ Lan, KH; Ван, Инь-Вэнь; Ли, Вэй-Пин; Лан, Кенг-Ли; Ценг, Су-Хан; Хунг, Ли-Ронг; Йен, Санг-Хюэ; Линь, Хан-Чи; Ли, Шоу-Донг (2012). «Множественные эффекты хонокиола на жизненный цикл вируса гепатита С». Liver International. 32 (6): 989–97. Дои:10.1111 / j.1478-3231.2011.02621.x. PMID 22098176. S2CID 22428079.
- ^ Атанасов, Атанас Г .; Wang, Jian N .; Гу, Ши П .; Бу, Цзин; Kramer, Matthias P .; Баумгартнер, Лиза; Фахрудин, Нананг; Ладурнер, Анджела; Малайнер, Клеменс; Вуоринен, Анна; Ноха, Стефан М .; Швайгер, Стефан; Роллингер, Джудит М .; Шустер, Даниэла; Ступпнер, Германн; Дирш, Верена М .; Хейсс, Эльке Х. (2013). «Хонокиол: природный агонист PPARγ, не являющийся адипогенным». Biochimica et Biophysica Acta (BBA) - Общие предметы. 1830 (10): 4813–4819. Дои:10.1016 / j.bbagen.2013.06.021. ЧВК 3790966. PMID 23811337.
- ^ а б Чжэн, Дж; Тан, Y; Вс, М; Чжао, Y; Ли, Q; Чжоу, Дж; Ван, Y (2013). «Характеристика, фармакокинетика, тканевое распределение и противоопухолевая активность субмикронных липидных эмульсий гонокиола у мышей с опухолевой нагрузкой». Die Pharmazie. 68 (1): 41–6. PMID 23444779.
- ^ Цай, Дун-Ху; Чжоу, Ченг-Джен; Ченг, Фу-Чжоу; Чен, Чи-Фу (1994). «Фармакокинетика гонокиола после внутривенного введения крысам оценивается с помощью высокоэффективной жидкостной хроматографии». Журнал хроматографии B. 655 (1): 41–5. Дои:10.1016 / 0378-4347 (94) 00031-х. PMID 8061832.
- ^ Шимер, Портер (2004). Секреты исцеления коренных американцев: травы, лекарства и методы, восстанавливающие дух. стр.83–4. ISBN 978-1-57912-392-5.
внешняя ссылка
- Исцелить магнолии, Журнал Эмори, Весна 2004 г.
