Флуоренол - Fluorenol
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 9ЧАС-Флуорен-9-ол | |
| Другие имена 9-гидроксифлуорен | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.015.345 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C13ЧАС10О | |
| Молярная масса | 182,22 г / моль |
| Внешность | Беловатый кристаллический порошок |
| Плотность | 1,151 г / мл |
| Температура плавления | От 152 до 155 ° C (от 306 до 311 ° F, от 425 до 428 K) |
| Практически нерастворим [2] | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
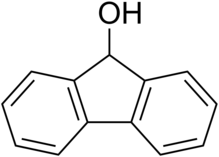
Флуоренол является алкоголь производная от флуорен. В наиболее значимом изомере, флуорен-9-оле или 9-гидроксифлуорене, гидроксильная группа расположен на мостиковом углероде между двумя бензольными кольцами. Гидроксифлуорен можно превратить в флуоренон путем окисления. Это твердое вещество бело-кремового цвета при комнатной температуре.
Токсичность
Флуоренол токсичен для водных организмов, включая водоросли, бактерии и ракообразных.[3] Флуоренол был запатентован как инсектицид в 1939 г.,[4] и является альгицид против зеленых водорослей Дуналиелла биокулата.[5]
Его токсичность и канцерогенность у человека неизвестны.[5]
Евгероический
Исследование, опубликованное Цефалон описывая исследования по разработке преемника евгероический модафинил сообщили, что соответствующее производное флуоренола на 39% более эффективно, чем модафинил, удерживало мышей в сознании в течение 4-часового периода.[6] Однако после дальнейшего исследования было установлено, что эугероическая активность аналога флуоренола, вероятно, связана с активный метаболит, который они идентифицируют как сам флуоренол.[6] Флуоренол слабый ингибитор обратного захвата дофамина с ИС50 из 9 мкМ, заметно на 59% слабее модафинила (IC50 = 3,70 мкМ),[6] потенциально делает его еще менее ответственным за зависимость.[7] Он также не проявил склонности к цитохром P450 2C19, в отличие от модафинила.[6]
Смотрите также
Рекомендации
- ^ 9-гидроксифлуорен, chemicalland21.com
- ^ Запись 9H-флуорен-9-ол в базе данных веществ GESTIS Институт охраны труда и здоровья, доступ 5 ноября 2008 г.
- ^ Шепич, Эстер; Бричель, Михаил; Лесковшек, Гермина (2003). «Токсичность флуорантена и его метаболитов биодеградации для водных организмов». Атмосфера. 52 (7): 1125–33. Дои:10.1016 / S0045-6535 (03) 00321-7. PMID 12820993.
- ^ Патент США 2197249: Инсектицид.
- ^ а б MSDS В архиве 2016-03-04 в Wayback Machine
- ^ а б c d Dunn, D .; Hostetler, G .; Iqbal, M .; Марси, В. Р .; Lin, Y.G .; Джонс, Б.; Aimone, L.D .; Gruner, J .; Атор, М. А .; Bacon, E. R .; Чаттерджи, С. (2012). «Агенты, способствующие пробуждению: поиск модафинила следующего поколения, извлеченные уроки: Часть III». Письма по биоорганической и медицинской химии. 22 (11): 3751–3753. Дои:10.1016 / j.bmcl.2012.04.031. PMID 22546675.
- ^ Мудрый, Р. А. (1996). «Нейробиология наркозависимости». Текущее мнение в нейробиологии. 6 (2): 243–51. Дои:10.1016 / S0959-4388 (96) 80079-1. PMID 8725967.

