РТИ-31 - Википедия - RTI-31
 | |
| Идентификаторы | |
|---|---|
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
| Формула | C16ЧАС20ClNО2 |
| Молярная масса | 293.79 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
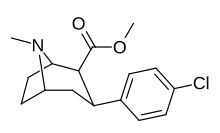
(-) - 2β-Карбометокси-3β- (4'-хлорфенил) тропан (РТИ-4229-31) является синтетическим аналог из кокаин что действует как стимулятор.[1] Полусинтез этого соединения зависит от доступности исходного материала кокаина. Согласно статье,[1] RTI-31 в 64 раза сильнее кокаина с точки зрения его способности вызывать самостоятельное введение у обезьян. ВЫИГРАТЬ 35428 был в 6 раз слабее РТИ-31, тогда как РТИ-51 был в 2,6 раза слабее РТИ-31.
Еще одним преимуществом, помимо эффективности этого соединения, является то, что продолжительность его действия больше, чем у кокаина. Поэтому его можно рассматривать в контексте как терапию на основе агонистов для лечения кокаиновой зависимости, хотя на самом деле это РТИ-336 с учетом этого вступили в клинические испытания. RTI-31 уже сам по себе является полностью психоактивным, что означает, что дальнейшие химические манипуляции следует рассматривать как вариант, который не является строго необходимым. RTI-336 фактически производится с использованием RTI-31 в качестве исходного материала. RTI-31 не является полностью избирательным DRI в том смысле, что он также имеет заметное сродство к блокировке SERT и NET. RTI-31 можно легко «очистить», как это делается, например, путем замены сложного карбометоксиэфира более стерически закрытым заместителем, как это делается для RTI-113.
Связывание и селективность поглощения
На основе поглощения тритированного биогенного моноамина радиоиндикаторы Это можно подтвердить, наблюдая за цифрами в прилагаемой таблице, что RTI-31 является относительно сбалансированным ингибитором обратного захвата по отношению D / N / S.
Аффинность связывающего лиганда для различных переносчиков несколько искажена в пользу DAT; в данных может быть некоторая предвзятость. Причиной этого может быть то, что WIN35428 относительно легче заменить из DAT, чем пароксетин из SERT, из-за более высокой константа привязки бывшего соединения.
Также нужно иметь в виду идею распущенности перевозчиков.[2] Возможно, что уровни NE повышены, по крайней мере частично, за счет блокады DAT.
РТИ-31 лежит где-то посередине стола между тропарилом на одном конце и РТИ-55 с другой. Это не так избирательно, как РТИ-113 для DAT, но более избирательно, чем Дихлоропан для этого транспортера. RTI-31 также обладает некоторой активностью агониста мускаринового ацетилхолина.
| МАТ IC50 (и Kя ) для простых фенилтропаны с 1R, 2S, 3S стереохимия.[3] | ||||||
| Сложный | [3ЧАС]CFT | [3ЧАС]DA | [3ЧАС]Низоксетин | [3ЧАС]NE | [3ЧАС]Пароксетин | [3ЧАС]5-HT |
| Кокаин[4] | 89.1 | 275 ср. 241 | 3300 (1990) | 119 ср. 161 | 1050 (45) | 177 ср. 112 |
| Тропарил | 23 | 49.8 | 920 (550) | 37.2 | 1960 (178) | 173 |
| ВЫИГРАТЬ 35428 | 13.9 | 23.0 | 835 (503) | 38.6 | 692 (63) | 101 |
| РТИ-31 | 1.1 | 3.68 | 37 (22) | 5.86 | 44.5 (4.0) | 5.00 |
| РТИ-113[5] | 1.98 | 5.25 | 2,926 | 242 | 2,340 | 391 |
| РТИ-51 | 1.7 | ? | 37.4 (23) | ? | 10.6 (0.96) | ? |
| РТИ-55 | 1.3 | 1.96 | 36 (22) | 7.51 | 4.21 (0.38) | 1.74 |
| РТИ-32 | 1.7 | 7.02 | 60 (36) | 8.42 | 240 (23) | 19.4 |
Данные в вышеприведенной таблице из мозга крыс (1995 г.). В более поздних работах предлагалось использовать клонированных переносчиков человека.
Дополнительные аналоги
RTI

- Нор-РТИ-31 называется РТИ-110.[7]
- Восстановленный эфир до спирта называется РТИ-93.
- Ацетилированный спирт называется РТИ-105.
- Бензоиловый спирт называется РТИ-123.
- РТИ-145 - метилкарбонат спирта.
Также возможно превращение сложного эфира в RTI-31 в гетероароматические ядра. RTI-470 был среди известных известных мощных DRI, 0,094 нМ.
Козиковский
Дальнейшая химическая модификация RTI-31 приводит к новым химическим соединениям; некоторые из них очень сильнодействующие, а действие одного из них длилось три дня (z-хлорвиниловый аналог).[8][9] 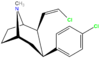

(i) 1 н. HCl, кипячение с обратным холодильником 15 ч; (ii) (a) POCl3, рефлюкс; (б) МеОН, 0 ° С; (iii) 4-ClPhMgBr, Et2О, –40 ° С; (b) –78 ° C, 1,1 экв. TFA; (c) хроматография на силикагеле; (iv) ДИБАЛ, толуол, –78 ° С; (v) ClCOCOCl, DCM, –78 ° C, ДМСО, 30 мин, TEA; (vi) Ph3п+CH2RBr−, n-BuLi, THF, комнатная температура; (vii) H2, Pt / C. 40 фунтов на кв. Дюйм, циклогексан.
| р | Икс | [3H] связывание мазиндола | [3H] поглощение дофамина |
| CO2Мне | Cl | 0.83 | 2.85 |
| CH = CH2 | Cl | 0.59 | 2.47 |
| (E) -CH = CHCl | Cl | 0.42 | 1.13 |
| (Z) -CH = CHCl | Cl | 0.22 | 0.88 |
| (E) -CH = CHPh | Cl | 0.31 | 0.66 |
| (Z) -CH = CHPh | Cl | 0.14 | 0.31 |
| CH2CH3 | Cl | 2.17 | 2.35 |
| (CH2)2CH3 | Cl | 0.94 | 1.08 |
| (CH2)2CH3 | ЧАС | 1.87 | 1.61 |
| (CH2)3CH3 | Cl | 1.21 | 0.84 |
| (CH2)5CH3 | Cl | 155.7 | 271 |
| CH2CH2Ph | Cl | 1.46 | 1.54 |
Это из-за повышенного содержания соединений липофильность. Обычно наблюдается акт изменения продолжительности действия лекарственного средства путем изменения его липофильности, но не ограничивается этим.
Если читать нокаин, интересно п-пропильная группа выбрана,
Хотя в настоящее время не было предпринято никаких усилий для «оптимизации» аффинности связывания в DAT, основная активность обнаружена для п-пропильное производное (-) - 9 из 3 нМ замечательно; это соединение только примерно в 10 раз менее активно, чем лучшие из высокоаффинных тропанов серии WIN.[10]
Смотрите также
Рекомендации
- ^ а б Ви С., Кэрролл ФИ, Вулвертон В.Л. (февраль 2006 г.). «Сниженная скорость связывания переносчика дофамина in vivo связана с более низкой относительной усиливающей эффективностью стимуляторов». Нейропсихофармакология. 31 (2): 351–62. Дои:10.1038 / sj.npp.1300795. PMID 15957006.
- ^ Daws LC (январь 2009 г.). «Неверные переносчики нейромедиаторов: акцент на поглощении серотонина и последствиях для эффективности антидепрессантов». Фармакология и терапия. 121 (1): 89–99. Дои:10.1016 / j.pharmthera.2008.10.004. ЧВК 2739988. PMID 19022290.
- ^ Кэрролл Ф.И., Котиан П., Дехгани А., Грей Дж. Л., Куземко М.А., Пархам К.А. и др. (Январь 1995 г.). «Кокаин и 3-бета (4'-замещенный фенил) тропан-2-бета-эфир карбоновой кислоты и аналоги амида. Новые высокоаффинные и селективные соединения для переносчика дофамина». Журнал медицинской химии. 38 (2): 379–88. Дои:10.1021 / jm00002a020. PMID 7830281.
- ^ Kozikowski AP, Johnson KM, Deschaux O, Bandyopadhyay BC, Araldi GL, Carmona G, et al. (Апрель 2003 г.). «Свойства смешанного агониста / антагониста кокаина (+) - метил 4бета (4-хлорфенил) -1-метилпиперидин-3альфа-карбоксилата, аналог кокаина на основе пиперидина». Журнал фармакологии и экспериментальной терапии. 305 (1): 143–50. Дои:10.1124 / jpet.102.046318. PMID 12649362.
- ^ Дамай М.И., Слеммер Дж. Э., Кэрролл ФИ, Мартин Б. Р. (июнь 1999 г.). «Фармакологическая характеристика взаимодействия никотина с кокаином и аналогами кокаина». Журнал фармакологии и экспериментальной терапии. 289 (3): 1229–36. PMID 10336510.
- ^ Кэрролл Ф.И., Ховард Дж. Л., Хауэлл Л. Л., Фокс Б. С., Кухар М. Дж. (Март 2006 г.). «Разработка селективного переносчика дофамина RTI-336 в качестве фармакотерапии при злоупотреблении кокаином». Журнал AAPS. 8 (1): E196-203. Дои:10.1208 / aapsj080124. ЧВК 2751440. PMID 16584128.
- ^ Spealman RD, Kelleher RT (март 1981). «Самостоятельное введение производных кокаина беличьими обезьянами». Журнал фармакологии и экспериментальной терапии. 216 (3): 532–6. PMID 7205634.
- ^ Козиковски, Алан П .; Роберти, Маринелла; Джонсон, Кеннет М .; Бергманн, Джон С .; Болл, Ричард Г. (1 июня 1993 г.). «SAR кокаина: дальнейшее исследование структурных изменений в центре C-2 обеспечивает соединения с субнаномолярной связывающей способностью». Письма по биоорганической и медицинской химии. 3 (6): 1327–1332. Дои:10.1016 / S0960-894X (00) 80341-8.
- ^ Козиковски А.П., Эддин Сайя М.К., Джонсон К.М., Бергманн Дж.С. (август 1995 г.). «Химия и биология 2-бета-алкил-3-бета-фенильных аналогов кокаина: субнаномолярные аффинные лиганды, которые предлагают новую модель фармакофоров в положении C-2». Журнал медицинской химии. 38 (16): 3086–93. Дои:10.1021 / jm00016a012. PMID 7636872.
- ^ Козиковски А.П., Аральди Г.Л., Боя Дж., Мейл В.М., Джонсон К.М., Флиппен-Андерсон Дж. Л. и др. (Май 1998 г.). «Химия и фармакология аналогов кокаина на основе пиперидина. Идентификация сильнодействующих ингибиторов DAT, лишенных тропанового скелета». Журнал медицинской химии. 41 (11): 1962–9. Дои:10,1021 / jm980028 +. PMID 9599245.
