Октопамин - Octopamine
 | |
 | |
| Клинические данные | |
|---|---|
| Другие имена | ОКТ, Норсимпатол, Норсинефрин, параграф-Октопамин, бета-гидрокситирамин, пара-гидроксифенилэтаноламин, α- (аминометил) -4 гидроксибензолметанол, 1- (п-гидроксифенил) -2-аминоэтанол |
| Маршруты администрация | Устный |
| Код УВД | |
| Физиологический данные | |
| Источник ткани | нервная система беспозвоночных; след амина у позвоночных |
| Целевые ткани | общесистемный у беспозвоночных |
| Рецепторы | TAAR1 (млекопитающие) OctαR, OctβR, TyrR (беспозвоночные), Oct-TyrR |
| Агонисты | Формамидины (амитраз (AMZ) и хлордимеформ (CDM)) |
| Антагонисты | эпинастин (3-амино-9, 13b-дигидро-1H-дибенз (c, f) имидазо (1,5a) азепин гидрохлорид) |
| Предшественник | тирамин |
| Биосинтез | тирамин-β-гидроксилаза; дофамин-β-гидроксилаза |
| Метаболизм | п-гидроксиминдельная кислота;[1][2] N-ацетилтрансферазы; фенилэтаноламин N-метилтрансфераза |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Биодоступность | 99.42 % |
| Метаболизм | п-гидроксиминдельная кислота;[1][2] N-ацетилтрансферазы; фенилэтаноламин N-метилтрансфераза |
| Устранение период полураспада | 15 минут в насекомых. От 76 до 175 минут у человека |
| Экскреция | До 93% попавшего внутрь октопамина выводится с мочой в течение 24 часов.[1] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.002.890 |
| Химические и физические данные | |
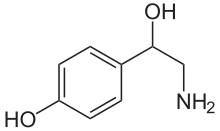
| Формула | C8ЧАС11NО2 |
| Молярная масса | 153.181 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Октопамин (молекулярная формула C8ЧАС11НЕТ2; также известный как параграф-октопамины и другие) является органический химикат тесно связан с норэпинефрин и синтезируется биологическим путем гомологичным путем. Его название происходит от того факта, что он был впервые обнаружен в слюнных железах осьминога.
Для многих видов беспозвоночных октопамин является важным нейротрансмиттер и гормон. В протостомы - членистоногие, моллюски и несколько типов червей - он заменяет норефинефрин и выполняет функции, очевидно похожие на функции норадреналина у млекопитающих, функции, которые были описаны как мобилизация организма и нервной системы для действий. У млекопитающих октопамин содержится только в следовых количествах, и его биологическая функция не установлена. В природе он также содержится во многих растениях, в том числе Горький апельсин.[3][4] Октопамин продается под торговыми марками, такими как Эпиренор, Norden, и Норфен для использования в качестве симпатомиметический препарат, отпускается по рецепту.
Функции
Клеточные эффекты
Октопамин оказывает свое действие, связываясь с рецепторами, расположенными на поверхности клеток, и активируя их. Эти рецепторы в основном изучались у насекомых, где их можно разделить на три типа: альфа-адренергические рецепторы (OctαR), которые структурно и функционально подобны норадренергическим рецепторам альфа-1 у млекопитающих; бета-адренорецепторы (OctβR), которые структурно и функционально подобны норадренергическим бета-рецепторам у млекопитающих; и смешанные рецепторы октопамина / тирамина (TyrR), которые структурно и функционально подобны норадренергическим альфа-2 рецепторам у млекопитающих.[5] Рецепторы в классе TyrR, однако, обычно сильнее активируются тирамин чем октопамином.[5]
У позвоночных рецепторов, специфичных для октопамина, не обнаружено. Октопамин слабо связывается с рецепторами норэпинефрин и адреналин, но неясно, имеет ли это какое-либо функциональное значение. Он сильнее связывается с следовые амино-ассоциированные рецепторы (TAAR), особенно TAAR1.[5]
Беспозвоночные
Октопамин был впервые открыт итальянским ученым Витторио Эрспамер в 1948 г.[6] в слюнных железах осьминог и с тех пор было обнаружено, что он действует как нейротрансмиттер, нейрогормон и нейромодулятор в беспозвоночные. Хотя Эрспамер обнаружил его естественное происхождение и назвал его, октопамин на самом деле существовал в течение многих лет как фармацевтический продукт.[7] Он широко используется всеми насекомыми, ракообразными (крабами, лобстерами, раками) и пауками для требовательного к энергии поведения. К такому поведению относятся полет,[8] кладка яиц,[9] и прыжки.[10][11]
Октопамин действует как насекомое эквивалент норэпинефрин и участвовал в регуляции агрессии у беспозвоночных, оказывая различное воздействие на разные виды. Исследования показали, что снижение уровня нейромедиатора октопамина и предотвращение кодирования тирамин-бета-гидроксилаза (фермент, преобразующий тирамин октопамину) снижает агрессию Дрозофила без влияния на другое поведение.[12]
У насекомых октопамин выделяется выбранным числом нейронов, но действует широко по всему центральному мозгу, на все органы чувств и на несколько ненейрональных тканей.[13][14] В грудных ганглиях октопамин в основном высвобождается нейронами DUM (дорсальная непарная медиана) и VUM (вентральная непарная медиана), которые выделяют октопамин на нервные, мышечные и периферические мишени.[15][16] Эти нейроны важны для обеспечения энергозатратного двигательного поведения, такого как прыжки и бегство, вызванные бегством. Например, нейрон саранчи DUMeti выделяет октопамин на разгибатель большеберцовой кости, чтобы увеличить мышечное напряжение и увеличить скорость расслабления. Эти действия способствуют эффективному сокращению мышц ног при прыжках.[13] Во время полета нейроны DUM также активны и выделяют октопамин по всему телу, чтобы синхронизировать энергетический обмен, дыхание, мышечную активность и активность полетных интернейронов.[8] Октопамин в саранча в четыре раза больше концентрируется в аксоне, чем в соме, и снижает миогенный ритм.[17]
в пчела и плодовая муха октопамин играет важную роль в обучении и памяти. в Светлячок, высвобождение октопамина приводит к образованию света в фонаре.[18][19]
У омаров октопамин, кажется, направляет и координирует нейрогормоны в некоторой степени в центральной нервной системе, и было замечено, что инъекции октопамина омарам и ракам приводили к растяжению конечностей и живота.[20]
Heberlein et al.[21] провели исследования переносимости алкоголя у плодовых мушек; они обнаружили, что мутация, вызывающая дефицит октопамина, также вызывает снижение толерантности к алкоголю.[22][23][24][25]
В изумрудный таракан оса ужалит хозяина за личинок (таракана) в головном ганглии (головном мозге). Яд блокирует рецепторы октопамина.[26] и таракан не проявляет нормальной реакции побега, чрезмерно ухаживая за собой. Он становится послушным, и оса ведет его к логову осы, натягивая его антенну, как поводок.[27]
в нематода октопамин обнаружен в высоких концентрациях у взрослых, снижая откладывание яиц и откачивание глотки с антагонистическим эффектом серотонин.[28]
Октопаминергические нервы в моллюск может присутствовать в сердце, с высокой концентрацией в нервной системе.[29]
У личинок восточный совок октопамин является иммунологически полезным, увеличивая выживаемость в популяциях с высокой плотностью населения.[30]
Позвоночные
В позвоночные, октопамин заменяет норэпинефрин в сочувствующий нейроны с хроническим употреблением ингибиторы моноаминоксидазы. Он может отвечать за общие побочный эффект из ортостатическая гипотензия с этими агентами, хотя есть также свидетельства того, что это фактически опосредовано повышенными уровнями N-ацетилсеротонин.
Одно исследование отметило, что октопамин может быть важным амином, который влияет на терапевтические эффекты ингибиторов, таких как ингибиторы моноаминоксидазы, особенно потому, что при лечении этим ингибитором наблюдалось значительное повышение уровня октопамина. Октопамин был положительно идентифицирован в образцах мочи млекопитающих, таких как люди, крысы и кролики, получавших ингибиторы моноаминоксидазы. В некоторых тканях животных также было обнаружено очень небольшое количество октопамина. Было замечено, что в теле кролика сердце и почки содержат самые высокие концентрации октопамина. Было обнаружено, что 93% октопамина элюируется с мочой в течение 24 часов после того, как он вырабатывается в организме кроликов в качестве побочного продукта ипрониазида.[7]
Фармакология
Октопамин продается под торговыми марками, такими как Эпиренор, Norden, и Норфен для использования в медицине как симпатомиметический препарат, отпускается по рецепту. Однако существует очень мало информации о его клинической полезности или безопасности.[31]
В млекопитающие октопамин может мобилизовать высвобождение толстый из адипоциты (жировые клетки), что привело к его продвижению на Интернет как средство для похудения. Тем не менее, высвобождаемый жир, вероятно, будет быстро поглощен другими клетками, и нет никаких доказательств того, что октопамин способствует похуданию. Октопамин также может увеличивать артериальное давление значительно в сочетании с другими стимуляторы, как в некоторых добавки для похудения.[32]
В Всемирное антидопинговое агентство перечисляет октопамин в качестве запрещенного вещества для использования на соревнованиях в качестве «указанного стимулятора».[33] в Запрещенном списке 2019 г.
Инсектициды
Рецептор октопамина является мишенью для инсектицидов, поскольку его блокировка приводит к снижению уровня цАМФ. Эфирные масла обладают таким нейроинсектицидным действием,[34] и этот механизм рецептора октопамина естественным образом используется растениями с активными инсектицидными фитохимическими веществами.[35]
Биохимические механизмы
Млекопитающие
Октопамин - один из четырех основных эндогенные агонисты человека следовой амин-ассоциированный рецептор 1.[36]
Беспозвоночные
Октопамин связывается со своими соответствующими рецепторами, связанными с G-белками (GPCR), чтобы инициировать путь передачи клеточного сигнала. Были определены по крайней мере три группы GPCR октопамина. OctαR (рецепторы OCTOPAMINE1) более тесно связаны с α-адренорецепторами, тогда как OctβR (рецепторы OCTOPAMINE2) более тесно связаны с β-адренорецепторами. Рецепторы октопамина / тирамина (включая Oct-TyrR) могут связывать оба лиганда и проявлять агонист-специфическое связывание. Oct-TyrR включен в группы генов как октопаминовых, так и тираминных рецепторов.[37]
Биосинтез
В людях
Смотрите также
Рекомендации
- ^ а б Hengstmann, J. H .; Конен, Вт; Конен, К; Эйхельбаум, М; Денглер, Х. Дж. (1974). «Физиологическое расположение п-октопамина в человеке». Архив фармакологии Наунин-Шмидеберг. 283 (1): 93–106. Дои:10.1007 / bf00500148. PMID 4277715. S2CID 35523412.
- ^ д’Андреа, Джованни; Нордера, Джанпьетро; Пиццолато, Жильберто; Болнер, Андреа; Колавито, Давиде; Флайбани, Рафаэлла; Леон, Альберта (2010). «Проследить метаболизм амина при болезни Паркинсона: низкие уровни октопамина в крови на ранних стадиях болезни». Письма о неврологии. 469 (3): 348–51. Дои:10.1016 / j.neulet.2009.12.025. PMID 20026245. S2CID 12797090.
- ^ Тан Ф, Тао Л., Ло Х, Дин Л., Го М., Не Л., Яо С. (сентябрь 2006 г.). «Определение октопамина, синефрина и тирамина в цитрусовых травах с помощью ионной жидкости с улучшенной« зеленой »хроматографией». Журнал хроматографии А. 1125 (2): 182–8. Дои:10.1016 / j.chroma.2006.05.049. PMID 16781718.
- ^ Ягелло-Войтович Э (1979). «Механизм центрального действия октопамина». Польский журнал фармакологии и фармации. 31 (5): 509–16. PMID 121158.
- ^ а б c Пфлюгер HJ, Стивенсонб PA (2005). «Эволюционные аспекты октопаминергических систем с акцентом на членистоногих». Строение и развитие членистоногих. 34 (3): 379–396. Дои:10.1016 / j.asd.2005.04.004.CS1 maint: использует параметр авторов (связь)
- ^ Эрспамер, В. (2009). «Активные вещества в задних слюнных железах осьминога. II. Тирамин и октопамин (оксиоктопамин)». Acta Pharmacologica et Toxicologica. 4 (3–4): 224–47. Дои:10.1111 / j.1600-0773.1948.tb03345.x.
- ^ а б Какимото Ю., Армстронг, доктор медицины (февраль 1962 г.). «Об идентификации октопамина у млекопитающих». Журнал биологической химии. 237: 422–7. PMID 14453200.
- ^ а б Орчард, я; Рамирес, Дж. М.; Ланге, АБ (январь 1993 г.). «Многофункциональная роль октопамина в полете саранчи». Ежегодный обзор энтомологии. 38 (1): 227–249. Дои:10.1146 / annurev.en.38.010193.001303. ISSN 0066-4170.
- ^ Ли, Хён-Гван; Сон, Чанг-Су; Ким, Ён-Чо; Дэвис, Рональд Л; Хан, Кён-Ан (1 декабря 2003 г.). «Рецептор октопамина OAMB необходим для овуляции у Drosophila melanogaster». Биология развития. 264 (1): 179–190. Дои:10.1016 / j.ydbio.2003.07.018. ISSN 0012-1606. PMID 14623240.
- ^ Поллак, Алан Дж .; Ритцманн, Рой Э .; Вестин, Джоанн (1988). «Активация интернейронов DUM-клеток с помощью вентральных гигантских интернейронов у таракана periplaneta americana». Журнал нейробиологии. 19 (6): 489–497. Дои:10.1002 / neu.480190602. ISSN 1097-4695. PMID 3171574.
- ^ Орчард, Ян (1 апреля 1982 г.). «Октопамин у насекомых: нейротрансмиттер, нейрогормон и нейромодулятор». Канадский журнал зоологии. 60 (4): 659–669. Дои:10.1139 / z82-095. ISSN 0008-4301.
- ^ Чжоу Ц., Рао Й, Рао Й (сентябрь 2008 г.). «Подмножество октопаминергических нейронов важны для агрессии дрозофилы». Природа Неврологии. 11 (9): 1059–67. Дои:10.1038 / №2164. PMID 19160504. S2CID 1134848.
- ^ а б Atwood, H.L .; Клозе, М. К. (1 января 2009 г.), «Модуляция нервно-мышечной передачи в нервно-мышечных соединениях беспозвоночных», в Сквайр, Ларри Р. (ред.), Энциклопедия неврологии, Oxford: Academic Press, стр. 671–690, ISBN 978-0-08-045046-9, получено 10 июля 2020
- ^ Рёдер, Т. (декабрь 1999 г.). «Октопамин у беспозвоночных». Прогресс в нейробиологии. 59 (5): 533–561. Дои:10.1016 / s0301-0082 (99) 00016-7. ISSN 0301-0082. PMID 10515667. S2CID 25654298.
- ^ Эккерт, Манфред; Рапус, Юрген; Нюрнбергер, Ася; Пензлин, Хайнц (1992). «Новое специфическое антитело показывает иммунореактивность, подобную октопамину, в брюшном нервном канатике тараканов». Журнал сравнительной неврологии (На французском). 322 (1): 1–15. Дои:10.1002 / cne.903220102. ISSN 1096-9861. PMID 1430305. S2CID 41099770.
- ^ Синакевич Ирина Григорьевна; Джеффард, Мишель; Пелате, Марсель; Лапьед, Бруно (апрель 1994). «Octopamine-подобная иммунореактивность в дорсальных непарных срединных (DUM) нейронах, иннервирующих добавочную железу самца таракана Periplaneta americana». Исследования клеток и тканей. 276 (1): 15–21. Дои:10.1007 / bf00354779. ISSN 0302-766X. S2CID 23485136.
- ^ Evans, P.D .; О'Ши, М. (апрель 1978 г.). «Идентификация октопаминергического нейрона и модуляция миогенного ритма у саранчи». Журнал экспериментальной биологии. 73: 235–260. ISSN 0022-0949. PMID 25941.
- ^ Гринфилд, доктор медицины (ноябрь 2001 г.). «Выявлено недостающее звено в биолюминесценции светлячков: НЕТ регуляции дыхания фотоцитов». BioEssays. 23 (11): 992–5. Дои:10.1002 / bies.1144. PMID 11746215.
- ^ Триммер Б.А., Априлле Дж. Р., Дудзински Д. М., Лагас С. Дж., Льюис С. М., Мишель Т. и др. (Июнь 2001 г.). «Оксид азота и борьба с вспышками светлячков». Наука. 292 (5526): 2486–8. Дои:10.1126 / science.1059833. PMID 11431567. S2CID 1095642.
- ^ Ливингстон М.С., Харрис-Уоррик Р.М., Кравиц Е.А. (апрель 1980 г.). «Серотонин и октопамин вызывают у омаров противоположные позы». Наука. 208 (4439): 76–9. Bibcode:1980Sci ... 208 ... 76L. Дои:10.1126 / science.208.4439.76. PMID 17731572. S2CID 32141532.
- ^ Heberlein U, Wolf FW, Rothenfluh A, Guarnieri DJ (август 2004 г.). «Молекулярно-генетический анализ интоксикации этанолом у Drosophila melanogaster». Интегративная и сравнительная биология. 44 (4): 269–74. CiteSeerX 10.1.1.536.262. Дои:10.1093 / icb / 44.4.269. PMID 21676709. S2CID 14762870.
- ^ Мур MS, DeZazzo J, Luk AY, Tully T, Singh CM, Heberlein U (июнь 1998 г.). «Интоксикация этанолом у дрозофилы: генетические и фармакологические доказательства регуляции сигнальным путем цАМФ». Клетка. 93 (6): 997–1007. Дои:10.1016 / S0092-8674 (00) 81205-2. PMID 9635429. S2CID 15312752.
- ^ Tecott LH, Heberlein U (декабрь 1998 г.). "Y мы пьем?". Клетка. 95 (6): 733–5. Дои:10.1016 / S0092-8674 (00) 81695-5. PMID 9865690.
- ^ Уильямс, Рут (22 июня 2005 г.). "Барные мухи: что наши сородичи-насекомые могут научить нас толерантности к алкоголю". Голый ученый.
- ^ Винс, Гайя (22 августа 2005 г.). "'Ген похмелья - ключ к толерантности к алкоголю ». Новый ученый.
- ^ Хопкин, Майкл (2007). «Как сделать таракана-зомби». Природа. Дои:10.1038 / новости.2007.312.
- ^ Гал Р., Розенберг Л.А., Либерзат Ф (декабрь 2005 г.). «Оса-паразитоид использует ядовитый коктейль, вводимый в мозг, чтобы управлять поведением и метаболизмом своей жертвы таракана». Архивы биохимии и физиологии насекомых. 60 (4): 198–208. Дои:10.1002 / arch.20092. PMID 16304619.
- ^ Horvitz, H.R .; Chalfie, M .; Трент, К .; Sulston, J.E .; Эванс, П. Д. (28 мая 1982 г.). «Серотонин и октопамин у нематоды Caenorhabditis elegans». Наука. 216 (4549): 1012–1014. Дои:10.1126 / science.6805073. ISSN 0036-8075. PMID 6805073.
- ^ Dougan, D. F. H .; Duffield, P.H .; Wade, D. N .; Даффилд, А. М. (1 января 1981 г.). «Возникновение и синтез октопамина в сердце и ганглиях моллюска Tapes watlingi». Сравнительная биохимия и физиология, часть C: Сравнительная фармакология. 70 (2): 277–280. Дои:10.1016/0306-4492(81)90064-2. ISSN 0306-4492.
- ^ Конг, Хайлун; Юань, Линь; Донг, Чуаньлей; Чжэн, Минъюань; Цзин, Ванхуи; Тянь, Чжэнь; Хоу, Цюли; Чэн, Юнься; Чжан, Лэй; Цзян, Синфу; Луо, Личжи (декабрь 2020 г.). «Иммунологическая регуляция β-адренергическим геном рецептора октопамина у густых личинок восточного сованного червя Mythmina separata». Развитие и сравнительная иммунология. 113: 103802. Дои:10.1016 / j.dci.2020.103802. ISSN 1879-0089. PMID 32712170.
- ^ Stohs SJ (январь 2015 г.). «Физиологические функции, фармакологические и токсикологические эффекты п-октопамина». Лекарственная и химическая токсикология. 38 (1): 106–12. Дои:10.3109/01480545.2014.900069. PMID 24654910. S2CID 21901553.
- ^ Галлер CA, Беновиц Н.Л., Джейкоб П. (сентябрь 2005 г.). «Гемодинамические эффекты добавок для похудения без эфедры у людей». Американский журнал медицины. 118 (9): 998–1003. Дои:10.1016 / j.amjmed.2005.02.034. PMID 16164886.
- ^ «Запрещено в соревнованиях - стимуляторы». ВАДА. Получено 6 мая 2019.
- ^ Энан, Эссам (1 ноября 2001 г.). «Инсектицидная активность эфирных масел: октопаминергические участки действия». Сравнительная биохимия и физиология, часть C: токсикология и фармакология. 130 (3): 325–337. Дои:10.1016 / S1532-0456 (01) 00255-1. ISSN 1532-0456.
- ^ Ротанг, Рамешвар Сингх (1 сентября 2010 г.). «Механизм действия инсектицидных вторичных метаболитов растительного происхождения». Защита урожая. 29 (9): 913–920. Дои:10.1016 / j.cropro.2010.05.008. ISSN 0261-2194.
- ^ Maguire JJ, Davenport AP (20 февраля 2018 г.). «Рецептор следовых аминов: TA1 рецептор ". IUPHAR / BPS Руководство по ФАРМАКОЛОГИИ. Международный союз фундаментальной и клинической фармакологии. Получено 16 июля 2018.
- ^ «Группа генов: рецепторы октопаминов», FlyBase, 16 октября 2018 г.
- ^ Бродли К.Дж. (март 2010 г.). «Сосудистые эффекты следовых аминов и амфетаминов». Фармакология и терапия. 125 (3): 363–375. Дои:10.1016 / j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (май 2005 г.). «Возрождение следовых аминов, вдохновленное новым семейством GPCR». Тенденции в фармакологических науках. 26 (5): 274–281. Дои:10.1016 / j.tips.2005.03.007. PMID 15860375.
- ^ Ван Х, Ли Дж, Донг Дж, Юэ Дж (февраль 2014 г.). «Эндогенные субстраты CYP2D мозга». Европейский журнал фармакологии. 724: 211–218. Дои:10.1016 / j.ejphar.2013.12.025. PMID 24374199.

