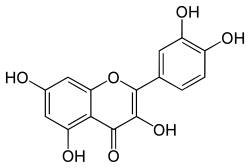
Кверцетин - Quercetin
 | |
 | |
| Имена | |
|---|---|
| Произношение | /ˈkшɜːrsɪтɪп/ |
| Название ИЮПАК 2- (3,4-дигидроксифенил) -3,5,7-тригидрокси-4ЧАС-хромен-4-он | |
| Другие имена 5,7,3′,4′-флавон-3-ол, Софоретин, мелетин, кверцетин, ксантаурин, кверцетол, кверцитин, квертин, флавин мелетин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.003.807 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C15ЧАС10О7 | |
| Молярная масса | 302,236 г / моль |
| Внешность | желтый кристаллический порошок[1] |
| Плотность | 1,799 г / см3 |
| Температура плавления | 316 ° С (601 ° F, 589 К) |
| Практически не растворим в воде; растворим в водных щелочных растворах[1] | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |

Кверцетин это растение флавонол от флавоноид группа полифенолы. Он содержится во многих фруктах, овощах, листьях, семенах и зернах; красный лук и капуста распространенные продукты, содержащие значительное количество кверцетина.[2] Кверцетин имеет горький вкус и используется в качестве ингредиента в пищевые добавки, напитки и продукты.
Вхождение
Кверцетин - это флавоноид широко распространен в природе.[2] Название используется с 1857 года и происходит от кверцетум (дубовый лес), по роду дубов Quercus.[3][4] Это естественный полярный транспорт ауксина ингибитор.[5]
Кверцетин - один из самых распространенных диетических флавоноидов,[2][6] при среднем дневном потреблении 25–50 миллиграммы.[7]
| Еда | Кверцетин (мг / 100 г) |
|---|---|
| каперсы, сырой | 234[6] |
| каперсы, консервы | 173[6] |
| любисток листья, сырые | 170[6] |
| гречневая крупа семена | 90 |
| док подобно щавель | 86[6] |
| редис листья | 70[6] |
| рожковое дерево волокно | 58[6] |
| укроп | 55[8] |
| кинза | 53[6] |
| Венгерский восковый перец | 51[6] |
| фенхель листья | 49[6] |
| лук красный | 32[6] |
| радиккио | 32[6] |
| кресс-салат | 30[6] |
| капуста | 23[6] |
| черноплодная рябина | 19[6] |
| болотная черника | 18[6] |
| клюква | 15[6] |
| брусника | 13[6] |
| сливы, черные | 12[6] |
У красного лука более высокие концентрации кверцетина встречаются в самых внешних кольцах и в части, ближайшей к корню, причем последняя является частью растения с самой высокой концентрацией.[9] Одно исследование показало, что органически выращенный помидоры содержал на 79% больше кверцетина, чем фрукты, выращенные неорганическим способом.[10] Кверцетин присутствует в различных видах медовый из разных растительных источников.[11]
Биосинтез
У растений фенилаланин конвертируется в 4-кумароил-КоА в серии шагов, известных как общие фенилпропаноид путь с использованием фенилаланин аммиак-лиаза, циннамат-4-гидроксилаза, и 4-кумароил-КоА-лигаза.[12] Одна молекула 4-кумароил-КоА добавляется к трем молекулам малонил-КоА с образованием тетрагидроксихалкона с использованием 7,2'-дигидрокси-4'-метоксиизофлаванолсинтазы. Затем тетрагидроксихалкон превращается в нарингенин с помощью халкон-изомераза.
Нарингенин превращается в эриодиктиол с использованием флаваноид-3'-гидроксилазы. Затем эриодиктиол превращается в дигидрокверцетин с флаванон-3-гидроксилазой, которая затем превращается в кверцетин с использованием флавонолсинтаза.[12]
Гликозиды

Кверцетин - это агликон форма ряда других флавоноидов гликозиды, Такие как рутин и кверцитрин, нашел в цитрусовые фрукты, гречневая крупа и лук.[2] Кверцетин образует гликозиды кверцитрин и рутин вместе с рамноза и рутиноза, соответственно. так же Guaijaverin это 3-О-арабинозид, гиперозид это 3-О-галактозид, изокверцитин это 3-О-глюкозид и спиреозид это 4'-О-глюкозид. CTN-986 является производным кверцетина, содержащимся в семенах хлопка и хлопковом масле. Микелианин это кверцетин 3-О-β-D-глюкуронопиранозид.[13]
Путь деградации рутина
Фермент кверцитриназа можно найти в Aspergillus flavus.[14] Этот фермент гидролизует гликозид кверцитрин выпустить кверцетин и L-рамноза. Это фермент в рутин катаболический путь.[15]
Фармакология
Фармакокинетика
В биодоступность кверцетина у людей низка и сильно варьирует (0–50%), и она быстро очищен с период полувыведения 1-2 часа после приема пищи или добавок кверцетина.[16] После приема с пищей кверцетин подвергается быстрому и обширному метаболизму, что вызывает биологические эффекты, предполагаемые от in vitro исследования вряд ли применимы in vivo.[17][18]
Добавки кверцетина в агликон форма намного меньше биодоступный чем кверцетин гликозид часто встречается в продуктах питания, особенно в красном луке.[2][19] Прием пищи с высоким содержанием жиров может увеличить биодоступность по сравнению с приемом пищи с низким содержанием жира.[19] и продукты, богатые углеводами, могут увеличить абсорбцию кверцетина, стимулируя перистальтика желудочно-кишечного тракта и толстая кишка ферментация.[2]
Метаболизм
У крыс кверцетин не претерпел значительных изменений. метаболизм I фазы.[20] Напротив, кверцетин подвергся обширному II этап (спряжение) производить метаболиты что больше полярный чем исходное вещество, и поэтому они быстрее выводятся из организма. Мета-гидроксильная группа из катехол метилируется катехол-O-метилтрансфераза. Четыре из пяти гидроксильных групп кверцетина являются глюкуронидированный к UDP-глюкуронозилтрансфераза. Исключением является 5-гидроксильная группа флавоноидного кольца, которая обычно не подвергается глюкуронизации. Основными метаболитами кверцетина, всасываемого перорально, являются: кверцетин-3-глюкуронид, 3'-метилкверцетин-3-глюкуронид, и кверцетин-3'-сульфат.[20][21]
Фармакология in vitro
Сообщается, что кверцетин ингибирует окисление других молекул и, следовательно, классифицируется как антиоксидант.[17][21] Он содержит полифенольный химическая субструктура, которая останавливает окисление, действуя как поглотитель свободные радикалы которые отвечают за цепные окислительные реакции.[22] Было показано, что кверцетин ингибирует Путь PI3K / AKT ведущий к подавление анти-апоптотический белок Bcl-w.[23][24]
Кверцетин также активирует или подавляет активность ряда белков.[25] Например, кверцетин неспецифический протеинкиназа ингибитор ферментов.[17][21] Также сообщалось, что кверцетин оказывает эстрогенный (женских половых гормонов) активности путем активации рецепторы эстрогена. Кверцетин активирует оба рецептор эстрогена альфа (ERα) и бета (ERβ)[26] с привязкой IC50 значения 1015 нМ и 113 нМ соответственно. Следовательно, кверцетин в некоторой степени селективен к ERβ (в 9 раз) и примерно на два-три порядка менее эффективен, чем эндогенный эстрогенный гормон. 17β-эстрадиол.[27][28] В клеточных линиях рака груди человека кверцетин также действует как агонист из G-протеиновый рецептор эстрогена (GPER).[29][30]
Заявления о здоровье
Кверцетин изучался в фундаментальные исследования и маленький клинические испытания.[2][31][32][33] Хотя добавки рекламировались для лечения рака и различных других заболеваний,[2][34] нет высококачественных доказательств того, что кверцетин (в виде добавок или в пище) полезен для лечения рака[35] или любое другое заболевание.[2][36]
Соединенные штаты Управление по контролю за продуктами и лекарствами выпустил предупреждающие письма нескольким производителям, рекламирующим на этикетках своих продуктов и веб-сайтах, что продукты с кверцетином можно использовать для лечения заболеваний.[37][38] FDA считает такую рекламу и продукты кверцетина неутвержденными - с неразрешенными заявления о здоровье в отношении продуктов против болезней - как определено в разделах 201 (g) (1) (B) и / или 201 (g) (1) (C) Закона [21 USC § 321 (g) (1) ( B) и / или 21 USC § 321 (g) (1) (C)], поскольку они предназначены для использования в диагностике, лечении, смягчении, лечении или профилактике заболеваний ",[37][38] условия, которые не выполнялись производителями.
Безопасность
В предварительных исследованиях на людях пероральный прием кверцетина в дозах до одного грамма в день в течение трех месяцев не вызывал побочные эффекты.[2] Безопасность использования кверцетина в БАД при беременности и кормление грудью не установлено.[2]
Смотрите также
|
|
|
Рекомендации
- ^ а б c «Паспорт безопасности дигидрата кверцетина». Архивировано из оригинал 16 сентября 2011 г.
- ^ а б c d е ж грамм час я j k «Флавоноиды (Обзор)». Информационный центр по микронутриентам, Институт Линуса Полинга, Университет штата Орегон, Корваллис, Орегон. Ноябрь 2015. Получено 1 апреля 2018.
- ^ «Кверцетин». Мерриам-Вебстер.
- ^ «Кверцетин (биохимия)». Encyclopdia Britannica.
- ^ Фишер К., Спет В., Флейг-Эберенц С., Нойхаус Г. (октябрь 1997 г.). «Индукция зиготических полиэмбрионов в пшенице: влияние полярного транспорта ауксина». Растительная клетка. 9 (10): 1767–1780. Дои:10.1105 / tpc.9.10.1767. ЧВК 157020. PMID 12237347.
- ^ а б c d е ж грамм час я j k л м п о п q р s «База данных Министерства сельского хозяйства США по содержанию флавоноидов в избранных пищевых продуктах, выпуск 3» (PDF). Министерство сельского хозяйства США. 2011 г.
- ^ Formica JV, Регельсон В. (1995). «Обзор биологии кверцетина и родственных биофлавоноидов». Пищевая и химическая токсикология. 33 (12): 1061–80. Дои:10.1016/0278-6915(95)00077-1. PMID 8847003.
- ^ Юстесен Ю., Кнутсен П. (май 2001 г.). «Состав флавоноидов в свежих травах и расчет потребления флавоноидов при использовании трав в традиционных датских блюдах». Пищевая химия. 73 (2): 245–50. Дои:10.1016 / S0308-8146 (01) 00114-5.
- ^ Слимстад Р., Фоссен Т., Воген И.М. (декабрь 2007 г.). «Лук: источник уникальных диетических флавоноидов». Журнал сельскохозяйственной и пищевой химии. 55 (25): 10067–80. Дои:10.1021 / jf0712503. PMID 17997520.
- ^ Mitchell AE, Hong YJ, Koh E, Barrett DM, Bryant DE, Denison RF, Kaffka S (июль 2007 г.). «Десятилетнее сравнение влияния органических и традиционных методов растениеводства на содержание флавоноидов в томатах». Журнал сельскохозяйственной и пищевой химии. 55 (15): 6154–9. Дои:10.1021 / jf070344 +. PMID 17590007.
- ^ Петрус К., Шварц Х, Зонтаг Г. (июнь 2011 г.). «Анализ флавоноидов в меде с помощью ВЭЖХ в сочетании с кулонометрическим обнаружением матрицы электродов и масс-спектрометрией с ионизацией электрораспылением». Аналитическая и биоаналитическая химия. 400 (8): 2555–63. Дои:10.1007 / s00216-010-4614-7. PMID 21229237. S2CID 24796542.
- ^ а б Винкель-Ширли Б. (июнь 2001 г.). «Биосинтез флавоноидов. Красочная модель для генетики, биохимии, клеточной биологии и биотехнологии». Физиология растений. 126 (2): 485–93. Дои:10.1104 / стр. 126.2.485. ЧВК 1540115. PMID 11402179.
- ^ Juergenliemk G, Boje K, Huewel S, Lohmann C, Galla HJ, Nahrstedt A (ноябрь 2003 г.). "Исследования in vitro показывают, что микелианин (кверцетин 3-О-бета-D-глюкуронопиранозид) способен достигать ЦНС из тонкого кишечника ». Planta Medica. 69 (11): 1013–7. Дои:10.1055 / с-2003-45148. PMID 14735439.
- ^ «Информация по EC 3.2.1.66 - кверцитриназа». БРЕНДА (BRaunschweig ENzyme DAtabase). Центр исследования инфекций им. Гельмгольца.
- ^ Транчиманд С., Брауант П., Якацио Г. (ноябрь 2010 г.). «Катаболический путь рутина с особым упором на кверцетиназу». Биоразложение. 21 (6): 833–59. Дои:10.1007 / s10532-010-9359-7. PMID 20419500. S2CID 30101803.
- ^ Graefe EU, Derendorf H, Veit M (1999). «Фармакокинетика и биодоступность флавонола кверцетина у человека» (PDF). (рассмотрение). Международный журнал клинической фармакологии и терапии. 37 (5): 219–33. PMID 10363620.
- ^ а б c Уильямс Р.Дж., Спенсер Дж. П., Райс-Эванс К. (апрель 2004 г.). «Флавоноиды: антиоксиданты или сигнальные молекулы?». (рассмотрение). Свободная радикальная биология и медицина. 36 (7): 838–49. Дои:10.1016 / j.freeradbiomed.2004.01.001. PMID 15019969.
- ^ Барнс С., Прасейн Дж., Д'Алессандро Т., Арабшахи А., Боттинг Н., Лила М.А., Джексон Дж., Джанле Э.М., Уивер К.М. (май 2011 г.). «Метаболизм и анализ изофлавонов и других пищевых полифенолов в пищевых продуктах и биологических системах». (рассмотрение). Еда и функции. 2 (5): 235–44. Дои:10.1039 / c1fo10025d. ЧВК 4122511. PMID 21779561.
- ^ а б Дабик В.М., Марра М.В. (2019). «Диетический кверцетин и кемпферол: биодоступность и потенциальная сердечно-сосудистая биологическая активность у людей». Питательные вещества. 11 (10): 2288. Дои:10.3390 / nu11102288. ЧВК 6835347. PMID 31557798.
- ^ а б День AJ, Ротвелл JA, Морган Р. (2004). «Характеристика метаболитов полифенолов». В Bao Y, Fenwick R (ред.). Фитохимические вещества для здоровья и болезней. Нью-Йорк, Нью-Йорк: Деккер. С. 50–67. ISBN 0-8247-4023-8.
- ^ а б c Руссо Г.Л., Руссо М., Спаньоло К., Тедеско I, Билотто С., Яннитти Р., Палумбо Р. (2014). «Кверцетин: ингибитор плейотропной киназы против рака». (рассмотрение). Лечение рака и исследования. 159: 185–205. Дои:10.1007/978-3-642-38007-5_11. ISBN 978-3-642-38006-8. PMID 24114481.
- ^ Мураками А, Ашида Х, Терао Дж (2008). «Многоцелевая профилактика рака кверцетином». (рассмотрение). Письма о раке. 269 (2): 315–25. Дои:10.1016 / j.canlet.2008.03.046. PMID 18467024.
- ^ Хартман МЛ, Чиж М (2020). «BCL-w: апоптотическая и неапоптотическая роль в здоровье и болезни». Смерть и болезнь клеток. 11 (4): 2260. Дои:10.1038 / s41419-020-2417-0. ЧВК 7174325. PMID 32317622.
- ^ Паес-Рибес М., Гонсалес-Гуальда Э, Доэрти Г. Дж., Муньос-Эспин Д. (2019). «Ориентация на стареющие клетки в трансляционной медицине». EMBO Молекулярная медицина. 11 (12): e10234. Дои:10.15252 / emmm.201810234. ЧВК 6895604. PMID 31746100.
- ^ Фейтельсон М.А., Арзуманян А., Кулатинал Р.Дж., Блейн С.В., Холкомб Р.Ф., Махаджна Дж., Марино М., Мартинес-Чантар М.Л., Наврот Р., Санчес-Гарсия I, Шарма Д., Саксена Н.К., Сингх Н., Влахостергиос П.Дж., Гуо С., Хоноки K, Fujii H, Georgakilas AG, Bilsland A, Amedei A, Niccolai E, Amin A, Ashraf SS, Boosani CS, Guha G, Ciriolo MR, Aquilano K, Chen S, Mohammed SI, Azmi AS, Bhakta D, Halicka D, Кейт WN, Nowsheen S (2015). «Устойчивое распространение рака: механизмы и новые терапевтические цели». (рассмотрение). Семинары по биологии рака. 35 Дополнение: S25–54. Дои:10.1016 / j.semcancer.2015.02.006. ЧВК 4898971. PMID 25892662.
- ^ Moutsatsou P (2007). «Спектр фитоэстрогенов в природе: наши знания расширяются». (рассмотрение). Гормоны (Афины, Греция). 6 (3): 173–93. PMID 17724002.
- ^ Маджолини М., Бонофильо Д., Марсико С., Панно М.Л., Ценни Б., Пикар Д., Андо С. (2001). «Рецептор эстрогена альфа опосредует пролиферативное, но не цитотоксическое дозозависимое действие двух основных фитоэстрогенов на клетки рака груди человека». (начальный). Молекулярная фармакология. 60 (3): 595–602. PMID 11502892.
- ^ ван дер Вуде Х., Тер Велд М.Г., Якобс Н., ван дер Сааг П.Т., Мерк А.Дж., Ритдженс И.М. (2005). «Стимуляция клеточной пролиферации кверцетином опосредована рецептором эстрогена». (начальный). Молекулярное питание и пищевые исследования. 49 (8): 763–71. Дои:10.1002 / mnfr.200500036. PMID 15937998.
- ^ Maggiolini M, Vivacqua A, Fasanella G, Recchia AG, Sisci D, Pezzi V, Montanaro D, Musti AM, Picard D, Andò S (2004). «Рецептор GPR30, связанный с G-белком, опосредует активацию c-fos с помощью 17-бета-эстрадиола и фитоэстрогенов в клетках рака груди». (начальный). Журнал биологической химии. 279 (26): 27008–16. Дои:10.1074 / jbc.M403588200. PMID 15090535.
- ^ Просниц Э. Р., Бартон М. (май 2014 г.). «Биология эстрогенов: новое понимание функции GPER и клинических возможностей». (рассмотрение). Молекулярная и клеточная эндокринология. 389 (1–2): 71–83. Дои:10.1016 / j.mce.2014.02.002. ЧВК 4040308. PMID 24530924.
- ^ Ян Ф, Сун Л., Ван Х, Ван Дж, Сюй З, Син Н. (июнь 2015 г.). «Кверцетин при раке простаты: химиотерапевтические и химиопрофилактические эффекты, механизмы и потенциал клинического применения (обзор)». Онкол. Представитель. 33 (6): 2659–68. Дои:10.3892 / или 2015.3886. PMID 25845380.
- ^ Gross P (1 марта 2009 г.), Новые роли полифенолов. Отчет из 3 частей о текущих положениях и состоянии науки, Мир нутрицевтиков
- ^ Майлз С.Л., МакФарланд М, Найлз Р.М. (2014). «Молекулярные и физиологические действия кверцетина: необходимость клинических испытаний для оценки его преимуществ при заболеваниях человека». Отзывы о питании. 72 (11): 720–34. Дои:10.1111 / nure.12152. PMID 25323953.
- ^ Д'Андреа Дж. (2015). «Кверцетин: флавонол с многогранным терапевтическим применением?». Фитотерапия. 106: 256–71. Дои:10.1016 / j.fitote.2015.09.018. PMID 26393898.
- ^ Адес ТБ, изд. (2009). Кверцетин. Полное руководство Американского онкологического общества по дополнительным и альтернативным методам лечения рака (2-е изд.). Американское онкологическое общество. ISBN 9780944235713.
- ^ Панель NDA Европейского агентства по безопасности пищевых продуктов (EFSA) (диетические продукты, питание и аллергия) (8 апреля 2011 г.). «Научное заключение по обоснованию заявлений о здоровье, связанных с кверцетином и защитой ДНК, белков и липидов от окислительного повреждения (ID 1647),« сердечно-сосудистой системой »(ID 1844),« психическим состоянием и работоспособностью »(ID 1845) и» печень, почки »(ID 1846) в соответствии со статьей 13 (1) Регламента (ЕС) № 1924/2006». Журнал EFSA. 9 (4): 2067–82. Дои:10.2903 / j.efsa.2011.2067. Получено 24 сентября 2014.
- ^ а б Дженис Л. Кинг (2 марта 2017 г.). «Предупреждающее письмо компании Cape Fear Naturals». Инспекции, соответствие, правоприменение и уголовные расследования, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 29 ноября 2018.
- ^ а б Рональд Пейс (17 апреля 2017 г.). "Предупреждающее письмо для DoctorVicks.com". Инспекции, соответствие, правоприменение и уголовные расследования, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 29 ноября 2018.
внешняя ссылка
 СМИ, связанные с Кверцетин в Wikimedia Commons
СМИ, связанные с Кверцетин в Wikimedia Commons
